Código do Estudante XX OLIMPÍADA IBEROAMERICANA DE QUÍMICA UNIVERSIDADE FEDERAL DO PIAUÍ UFPI MINISTÉRIO DA CIÊNCIA, TECNOLOGIA E INOVAÇÃO - MCTI
|
|
|
- Baltazar di Castro Amarante
- 7 Há anos
- Visualizações:
Transcrição
1 NOME: EXAME EXPERIMENTAL SETEMBRO DE
2 Instruções gerais para o exame prático (TOTAL DE PONTOS = 40) 1. Durante todo o tempo em que estiver no laboratório, você deverá estar equipado com a bata e óculos de segurança que lhe são fornecidos. Você pode usar a sua bata e os seus óculos se lhe derem autorização. Sugere-se a utilização de luvas, quando necessário. 2. Espera-se que os estudantes trabalhem de forma segura e ética e que conservem limpo o material e a bancada de trabalho. Pergunte ao assistente de laboratório se tiver alguma dúvida relativa às normas de segurança. 3. Este exame prático tem a duração de 4:30 horas e é constituído por 2 problemas experimentais (cada um valendo 20 pontos). Você pode realizar os problemas práticos na ordem que desejar. 4. Antes de iniciar o seu trabalho experimental leia cuidadosamente todo o exame prático e analise os espaços para respostas. Identifique onde está todo o material que vai utilizar. Você tem 30 minutos para ler o exame e planejar o trabalho experimental. 5. Comece a prova quando for dado o sinal de início. 6. Você tem 4 horas para executar todo o exame e registrar os seus resultados nos espaços reservados para respostas. 7. Para medir com as pipetas você deverá utilizar unicamente a pêra de borracha. 8. É proibido comer no laboratório. Você pode pedir autorização ao assistente de laboratório para ir ao banheiro ou para beber água. 9. Escreva todas as suas respostas com caneta esferográfica (Não use o lápis). 10. No cabeçalho de cada folha de respostas escreva o seu nome e o seu código de identificação (este está indicado no seu local de trabalho). 11. Você só poderá usar o material que lhe for fornecido e a sua calculadora. 12. Em caso de necessitar de mais reagentes ou de repor algum material de vidro ou outro dirija-se ao assistente de laboratório. Isto será penalizado com 1 (um) ponto por cada solicitação. 13. O número de algarismos significativos nas respostas numéricas deve estar de acordo com o erro experimental. 14. Você deverá escrever todas as suas respostas nos espaços reservados para esse fim. O que for escrito fora desses espaços não será qualificado. Também não escreva nada na parte de trás das folhas. Se necessitar de folhas de rascunho para cálculos ou substituir alguma(s) folha(s) de resposta por outra(s) solicite ao assistente de laboratório. 2
3 15. Será dado um aviso 15 minutos antes do final do tempo previsto para a prova. 16. Quando ouvir o sinal de terminar, você deverá parar de trabalhar imediatamente, caso contrário, o problema que estiver fazendo será anulado. 17. Quando terminar o exame você deve colocar todas as folhas no envelope que recebeu e somente deverá fechá-lo na presença do assistente de laboratório que lhe entregará um recibo. Só as folhas que estiverem dentro do envelope fechado serão corrigidas e classificadas. 18. Você não pode sair do laboratório sem que lhe seja dada autorização. 19. É imprescindível que entregue esse exame com o seu nome e o seu código. Resíduos químicos e material de vidro. 1. Os resíduos químicos devem ser colocados nos recipientes apropriados. 2. O material de vidro quebrado deve ser colocado no recipiente para descarte de vidro. Limpeza. 1. Ao terminar deixe o seu local de trabalho limpo e arrumado. SOLUÇÕES DISPONÍVEIS 01 Acido clorídrico ~ 0,1 mol/l ( HCl) 250 ml 02 Acido clorídrico 1 mol/l (HCl) 500mL 03 Hidróxido de sódio ~ 0,1 mol/l (NaOH) 250mL 04 Hidróxido de sódio 1 mol/l (NaOH) 250mL 05 Fenolftaleína 5mL 06 Verde de bromo cresol 5mL 07 4 tubos Falcon com NaOH(s) tubo Falcon com amostra desconhecida - 09 Cloreto de bário 10% 50mL 3
4 MATERIAL DISPONÍVEL NA BANCADA (1 kit completo para cada estudante) ITENS MATERIAL QUANTIDADE 01 Erlenmeyer de 250 ml Erlenmeyer de 125 ml Balão volumétrico de 250 ml Becker de 50 ml Funil analítico de 30 ml Funil analítico de 50 ml Pipeta volumétrica de 10 ml Pipeta volumétrica de 25 ml Pipeta volumétrica de 50 ml Proveta de 100 ml Bastão de vidro Bureta de 50 ml Suporte universal Garra dupla tipo borboleta Pipetador automático (pera) Garrafa térmica (calorímetro) Termômetro Pisseta para água destilada Conta gotas 02 4
5 EXPERIMENTO 1: VERIFICAÇÃO EXPERIMENTAL DA LEI DE HESS A Termoquímica é o ramo da Química que estuda a troca de energia que acompanha transformações, tais como: processos de misturas, transições de fases e reações químicas. Uma das grandezas calculadas e/ou medidas experimentalmente, em Termodinâmica, é a variação de entalpia (H), que corresponde à energia absorvida ou liberada numa transformação química sob pressão constante. Portanto, as medidas comuns de calor, realizadas em laboratório (em geral, sob pressão atmosférica), são variações de entalpia. A variação de entalpia é uma grandeza denominada função de estado. Em outras palavras, dizemos que a variação de entalpia de uma dada transformação independe do caminho sob o qual a transformação é realizada. Essa regra é conhecida como Lei de Hess. Nesta questão vamos fazer uma verificação experimental da Lei de Hess utilizando a entalpia de dissolução e a entalpia de neutralização. As medidas de calor são realizadas num calorímetro adiabático. Este dispositivo é um recipiente contendo o sistema sob transformação e que é perfeitamente isolado, de modo que não há escoamento nem de calor ou matéria, seja para dentro ou para fora do sistema. Para o calorímetro usado neste experimento considere que a capacidade calorífica, Ccal, é igual a 17,6 cal/ C. A entalpia é calculada pela variação de temperatura que será convenientemente medida com um termômetro adequado. 5
6 PARTE EXPERIMENTAL Procedimento experimental A) Determinação do calor (entalpia) de dissolução do NaOH(s) em água (realize o experimento em duplicata): - Medir com uma proveta 96 ml de água destilada à temperatura ambiente e despejar no calorímetro vazio. Após o sistema entrar em equilíbrio térmico, medir a temperatura da água no calorímetro; - Transfira quantitativamente a massa de NaOH, disponível em um dos frascos, para dentro do calorímetro com água e agitar levemente para dissolver todo o NaOH. Após o equilíbrio térmico, medir a temperatura do sistema Observação: anote o número do frasco e a massa correspondente de NaOH). QA1) Determine a variação de temperatura (Tdiss): (3 pontos) Número do Frasco Massa de NaOH / g T inicial / o C T final / o C T diss / o C QA2) Calcule a variação de entalpia de dissolução do hidróxido de sódio (vamos denominá-la Hdiss). (3 pontos) Fórmula: H diss = mc T diss + C cal T diss Onde m é a massa de solução, c é o calor específico da solução. Observações: Expresse esse valor em kcal/mol. 6
7 Calcule a média. Considere que o calor específico da solução é independente da temperatura e possui valor de 0,94 cal g -1 C -1. Utilize a massa de solução. Se por alguma razão você não obteve Tdiss, utilize o valor de 10 C. B) Determinação do calor (entalpia) de reação (neutralização) do NaOH(aq) e HCl(aq) (realize o experimento em duplicata) - Após esvaziar, lavar e secar convenientemente o calorímetro e o termômetro, medir com uma proveta 100 ml da solução de NaOH 1 mol/l e a seguir despejar dentro do calorímetro. Meça a temperatura após o sistema entrar em equilíbrio térmico. - Medir 100 ml da solução de HCl 1 mol/l com uma proveta, colocá-la num béquer e após o equilíbrio térmico, medir a temperatura. Faça a medida com o termômetro 7
8 previamente lavado e seco. - Adicionar a solução de HCl à solução de NaOH de dentro do calorímetro. Fechar o calorímetro imediatamente e medir a temperatura após o sistema entrar em equilíbrio térmico; QB1) Determine a variação de temperatura (Tneut): (3 pontos) T inicial / o C T final / o C T neut / o C QB2) Calcule a variação de entalpia de neutralização (vamos denominá-la Hneut). (3 pontos). Fórmula: H neut = m NaOH c NaOH T neut + m HCl c HCl T neut + C cal T neut Onde mnaoh é a massa de solução de NaOH, cnaoh é o calor específico da solução de NaOH, mhcl é a massa de solução de HCl, chcl é o calor específico da solução de HCl. Observações: Expresse esse valor em kcal/mol. Calcule a média. Considere que o calor específico das soluções são independentes da temperatura e possuem valor de 0,94 cal g -1 C -1 para a solução de NaOH e 1,00 cal g -1 C -1 para a solução de HCl. Considere que ambas as soluções possuem densidade igual a 1,00 g/ml. Se por alguma razão você não obteve Tneut, utilize o valor de 15 C. 8
9 C) Determinação do calor (entalpia) de reação (neutralização) entre o NaOH(s) e HCl(aq) (realize o experimento em duplicata): - Após esvaziar, lavar e secar convenientemente o calorímetro e o termômetro, medir com uma proveta 100 ml da solução de HCl 1 mol/l e a seguir despejar dentro do calorímetro. Meça a temperatura após o sistema entrar em equilíbrio térmico; - Transferir quantitativamente a massa de NaOH disponível para dentro do calorímetro com a solução de HCl e agitar levemente para dissolver todo o NaOH. Após atingir o equilíbrio térmico, medir a temperatura do sistema 9
10 QC1) Determine a variação de temperatura (Tdn): (1,5 pontos) Número do Frasco Massa de NaOH / g T inicial / o C T final / o C T dn / o C QC2) Calcule a variação de entalpia nesta transformação (vamos denominá-la Hdn). (1,5 pontos). Fórmula: H dn = mc T dn + C cal T dn Onde m é a massa de solução, c é o calor específico da solução. Observações: Expresse esse valor em kcal/mol. Calcule a média. Considere que o calor específico da solução final é independente da temperatura e possui valor de 1,00 cal g -1 C -1 Considere que a solução possui densidade igual a 1,00 g/ml. Se por alguma razão você não obteve Tdn, utilize o valor de 25 C. 10
11 QC3) Escreva abaixo as equações químicas envolvidas na parte A e B: (1,0 pontos) 11
12 QC4) Calcule a variação de entalpia que resulta da soma de HdisscomHneut (vamos denominá-la Hdncal): (1,0 ponto) QC5) Calcule o erro percentual associado à verificação experimental da lei de Hess pela fórmula: (1,0 pontos) Fórmula: erro = H dn H dncal H dn 100% QC6) Assinale V para verdadeiro e F para falso nas seguintes afirmações a respeito de detalhes do experimento e das possíveis fontes de erro: (2,0 pontos) ( ) A falta de homogeneidade na temperatura pode acontecer devido a uma troca rápida de calor dentro do calorímetro. ( ) Quanto maior o intervalo de tempo utilizado para a leitura do termômetro, após 12
13 cada procedimento, melhor será a precisão na medida do correto T. ( ) Um mau isolamento térmico do calorímetro ocasionando perdas de calor para o exterior é uma importante fonte de erro. ( ) Um mecanismo que permitisse uma leve de agitação do sistema poderia acelerar as trocas de calor e assim proporcionar medições mais adequadas para o correto T. 13
14 EXPERIMENTO 2: ANÁLISE DE UMA MISTURA DE CARBONATO E BICARBONATO Este procedimento envolve duas titulações. (a) Primeiro, a alcalinidade total (bicarbonato + carbonato) é medida titulando-se a mistura com HCl padrão até o ponto final verde, indicado pelo verde de bromocresol. (b) Uma alíquota é separada da amostra desconhecida e é tratada com NaOH padrão em excesso para converter bicarbonato em carbonato. A seguir todo o carbonato é precipitado com BaCl2. O excesso de NaOH é titulado imediatamente com HCl padrão para determinar quanto bicarbonato estava presente. A partir da alcalinidade total e da concentração de bicarbonato é possível calcular a concentração original de carbonato. Procedimento Transfira a quantidade total da mistura de carbonato e bicarbonato, contida no frasco rotulado Amostra desconhecida, para um balão volumétrico de 250 ml com o auxílio de um funil. Para uma transferência quantitativa, coloque um pouco de água contida na pisseta dentro do tubo e transfira para o balão volumétrico. Repita este procedimento por mais duas vezes. Lave o funil algumas vezes com pequenas porções de água para dissolver a amostra. Remova o funil, dilua até a marca de aferição e homogeneíze bem. Análise da alcalinidade total. Pipete uma alíquota de 25,00 ml de solução da amostra desconhecida para um erlenmeyer de 125 ml, adicione três gotas do indicador verde de bromocresol (contido no tubo plástico rotulado verde de bromocresol ) e titule com HCl padrão, (contido no frasco rotulado Solução HCl 0,094 mol/l) até mudança da cor do indicador para esverdeado. Repita este procedimento com pelo menos mais uma alíquota de 25,00 ml da amostra desconhecida (duplicata). Teor de bicarbonato. Pipete 25,00 ml da solução da amostra desconhecida e 14
15 50,00 ml de NaOH padrão (contido no frasco rotulado Solução NaOH 0,100 mol/l ) para um frasco de 250 ml. Misture e adicione, por meio de uma pipeta, 10,00 ml de BaCl2 10% m/m (contido no frasco rotulado Solução BaCl2 10%. Misture novamente de modo a precipitar o BaCO3. Em seguida, adicione duas gotas do indicador fenolftaleína (contido no tubo plástico rotulado fenolftaleína ) e titule imediatamente a mistura com solução HCl 0,094 mol/l. Repita este procedimento com pelo menos mais uma alíquota de 25,00 ml da amostra desconhecida (duplicata). Questionário: Escrever todas as equações químicas balanceadas, envolvidas nas duas titulações utilizadas, indicando os estados de agregação. (2 pontos) 15
16 Calcule a alcalinidade total média na amostra. (7 pontos) Volume/mL (5 pontos) Concentração/mol L -1 (1,5 pontos) Concentração média/ mol L -1 (0,5 ponto) 16
17 Calcule a concentração média de bicarbonato na amostra. (7 pontos) Volume/mL (5 pontos) Concentração/mol L -1 (1,5 pontos) Concentração média/ mol L -1 (0,5 ponto) 17
18 Calcule a concentração média de carbonato na amostra. (2 pontos) Concentração/mol L -1 (1,5 pontos) Concentração média/ mol L -1 (0,5 ponto) 18
19 Expresse a composição da amostra desconhecida, em % (m/m), para cada uma das espécies analisadas (bicarbonato de sódio, 84 g/mol e carbonato de sódio, 106 g/mol). (2 pontos) 19
Prática 4: Reações envolvendo trocas de calor
 Prática 4: Reações envolvendo trocas de calor Pretende-se com essa atividade dar ao aluno a oportunidade de fazer experiências que possibilitem calcular calores de reação e aplicação da Lei de Hess. Etapa
Prática 4: Reações envolvendo trocas de calor Pretende-se com essa atividade dar ao aluno a oportunidade de fazer experiências que possibilitem calcular calores de reação e aplicação da Lei de Hess. Etapa
Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações.
 EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES. CH3COOCH2CH3 + H2O CH3COOH + CH3CH2OH (1) Acetato de etila água ácido acético etanol
 PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES 1. Introdução Uma investigação experimental detalhada mostra que a maioria das reações químicas não avança até a realização completa, isto é, quantidades mensuráveis
PRÁTICA: EQUILÍBRIO QUÍMICO EM SOLUÇÕES 1. Introdução Uma investigação experimental detalhada mostra que a maioria das reações químicas não avança até a realização completa, isto é, quantidades mensuráveis
EXPERIÊNCIA 7 TITULAÇÃO
 CENTRO DE CIÊNCIAS TECNOLÓGICAS - CCT Departamento de Ciências Básicas e Sociais - DCBS Disciplina Química Experimental QEX Prof. Sivaldo Leite Correia EXPERIÊNCIA 7 TITULAÇÃO 1. INTRODUÇÃO Na ciência
CENTRO DE CIÊNCIAS TECNOLÓGICAS - CCT Departamento de Ciências Básicas e Sociais - DCBS Disciplina Química Experimental QEX Prof. Sivaldo Leite Correia EXPERIÊNCIA 7 TITULAÇÃO 1. INTRODUÇÃO Na ciência
Técnicas de Trabalho com Material Volumétrico
 Universidade Federal de Goiás Instituto de Química Curso Experimental de Transformações Químicas 2010 Prof. Dr. Anselmo (adaptado, Agustina) Técnicas de Trabalho com Material Volumétrico 1 Objetivo Nesta
Universidade Federal de Goiás Instituto de Química Curso Experimental de Transformações Químicas 2010 Prof. Dr. Anselmo (adaptado, Agustina) Técnicas de Trabalho com Material Volumétrico 1 Objetivo Nesta
QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier. Prática 04 Termoquímica Aplicação do ciclo de Born-Harber
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 04 Termoquímica Aplicação
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 04 Termoquímica Aplicação
Práticas de. Química Geral e Orgânica. para Engenharia Ambiental
 Práticas de Química Geral e Orgânica para Engenharia Ambiental INTRODUÇÂO A química é uma ciência experimental e se ocupa especialmente das transformações das substâncias, de sua composição e das relações
Práticas de Química Geral e Orgânica para Engenharia Ambiental INTRODUÇÂO A química é uma ciência experimental e se ocupa especialmente das transformações das substâncias, de sua composição e das relações
Figura 1: Equilíbrio químico entre as espécies glicose, manose e frutose em meio alcalino
 4º Módulo de Química - 2º Sem 2012 Procedimento de Prática Experimental Introdução Um açúcar redutor (AR) pode ser identificado pelo reagente de Benedict porque o grupo aldeído, presente no açúcar, reduz
4º Módulo de Química - 2º Sem 2012 Procedimento de Prática Experimental Introdução Um açúcar redutor (AR) pode ser identificado pelo reagente de Benedict porque o grupo aldeído, presente no açúcar, reduz
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE
 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
Prática de Laboratório 1
 Prática de Laboratório 1 12 pontos Preparação do ácido 2-iodobenzóico [Tempo aprox: 1 hr] Essa prática de laboratório envolve a preparação do acido 2-iodobenzóico a partir do acido 2-aminobenzóico. O procedimento
Prática de Laboratório 1 12 pontos Preparação do ácido 2-iodobenzóico [Tempo aprox: 1 hr] Essa prática de laboratório envolve a preparação do acido 2-iodobenzóico a partir do acido 2-aminobenzóico. O procedimento
Universidade Federal de Sergipe Departamento de Química Química Analítica Experimental Prof. Marcelo da Rosa Alexandre Alunos:
 Alunos: DETERMINAÇÃO DA ACIDEZ TOTAL EM BEBIDAS 1. Padronizar a solução de NaOH 0,1 mol.l -1 com biftalato de potássio (P.M. KHC8H4O4 = 204). Lembre-se de calcular a massa de biftalato de potássio para
Alunos: DETERMINAÇÃO DA ACIDEZ TOTAL EM BEBIDAS 1. Padronizar a solução de NaOH 0,1 mol.l -1 com biftalato de potássio (P.M. KHC8H4O4 = 204). Lembre-se de calcular a massa de biftalato de potássio para
1. PREPARO DE SOLUÇÕES E TITULAÇÃO
 1. PREPARO DE SOLUÇÕES E TITULAÇÃO I. INTRODUÇÃO Solução é uma mistura homogênea de uma ou mais substâncias. A substância presente em maior quantidade é denominada solvente, e as outras substâncias na
1. PREPARO DE SOLUÇÕES E TITULAÇÃO I. INTRODUÇÃO Solução é uma mistura homogênea de uma ou mais substâncias. A substância presente em maior quantidade é denominada solvente, e as outras substâncias na
FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS FCAV/ UNESP
 1 FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS FCAV/ UNESP Curso: Engenharia Agronômica Disciplina: Química Analítica Turma: TP3 Docente Responsável: Prof a. Dr a. Luciana Maria Saran Roteiro 6: Análise
1 FACULDADE DE CIÊNCIAS AGRÁRIAS E VETERINÁRIAS FCAV/ UNESP Curso: Engenharia Agronômica Disciplina: Química Analítica Turma: TP3 Docente Responsável: Prof a. Dr a. Luciana Maria Saran Roteiro 6: Análise
QUIO95 - Análises Volumétricas II semestre 2018
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO95 - Análises Volumétricas II semestre 2018 Prática 3 Preparo e padronização das soluções de HCl
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO95 - Análises Volumétricas II semestre 2018 Prática 3 Preparo e padronização das soluções de HCl
INTRODUÇÃO À TITULOMETRIA PADRONIZAÇÃO DE SOLUÇÕES. META Determinar a concentração de ácido clorídrico por titulometria de neutralização.
 Aula INTRODUÇÃO À TITULOMETRIA PADRONIZAÇÃO DE SOLUÇÕES META Determinar a concentração de ácido clorídrico por titulometria de neutralização. OBJETIVOS Ao final desta aula o aluno deverá: detectar o ponto
Aula INTRODUÇÃO À TITULOMETRIA PADRONIZAÇÃO DE SOLUÇÕES META Determinar a concentração de ácido clorídrico por titulometria de neutralização. OBJETIVOS Ao final desta aula o aluno deverá: detectar o ponto
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA
 Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE. Versão professor. Algumas notas prévias
 ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
Práticas de Química Geral QB71J
 PR UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ - UTFPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA / LICENCIATURA
PR UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ - UTFPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA / LICENCIATURA
Figura 1: Equilíbrio químico entre as espécies glicose, manose e frutose em meio alcalino
 Introducão Um açúcar redutor (AR) pode ser identificado pelo reagente de Benedict 1 porque o grupo aldeído, presente no açúcar, reduz o íon cúprico (Cu 2+ ) formando um precipitado de óxido de cobre (I),
Introducão Um açúcar redutor (AR) pode ser identificado pelo reagente de Benedict 1 porque o grupo aldeído, presente no açúcar, reduz o íon cúprico (Cu 2+ ) formando um precipitado de óxido de cobre (I),
FQE0001 Exp. 04. Físico-Química Experimental. Termoquímica. 1. Introdução
 1. Introdução Termoquímica Termoquímica é o ramo da termodinâmica que estuda o calor trocado entre o sistema e sua vizinhança devido à ocorrência de uma reação química ou transformação de fase. Desta maneira,
1. Introdução Termoquímica Termoquímica é o ramo da termodinâmica que estuda o calor trocado entre o sistema e sua vizinhança devido à ocorrência de uma reação química ou transformação de fase. Desta maneira,
Experiência nº 8: Titulações Ácido-Base
 Experiência nº 8: Titulações Ácido-Base 1. Questões de estudo - Como determinar com precisão a concentração de uma solução (ácida ou básica)? Explique detalhadamente. - Como determinar experimentalmente
Experiência nº 8: Titulações Ácido-Base 1. Questões de estudo - Como determinar com precisão a concentração de uma solução (ácida ou básica)? Explique detalhadamente. - Como determinar experimentalmente
PRÁTICA 01 - INTRODUÇÃO AO TRABALHO NO LABORATÓRIO DE QUÍMICA ANALÍTICA E PREPARO E PADRONIZAÇÃO DE SOLUÇÕES
 PRÁTICA 01 - INTRODUÇÃO AO TRABALHO NO LABORATÓRIO DE QUÍMICA ANALÍTICA E PREPARO E PADRONIZAÇÃO DE SOLUÇÕES METAS Apresentar o objetivo da parte prática da disciplina; apresentar as instruções de trabalho
PRÁTICA 01 - INTRODUÇÃO AO TRABALHO NO LABORATÓRIO DE QUÍMICA ANALÍTICA E PREPARO E PADRONIZAÇÃO DE SOLUÇÕES METAS Apresentar o objetivo da parte prática da disciplina; apresentar as instruções de trabalho
PRÁTICA 07: PADRONIZAÇÃO DE SOLUÇÕES
 PRÁTICA 07: PADRONIZAÇÃO DE SOLUÇÕES 1- INTRODUÇÃO Análise volumétrica refere-se a todo procedimento no qual o volume de um reagente necessário para reagir com um constituinte em análise é medido. - Em
PRÁTICA 07: PADRONIZAÇÃO DE SOLUÇÕES 1- INTRODUÇÃO Análise volumétrica refere-se a todo procedimento no qual o volume de um reagente necessário para reagir com um constituinte em análise é medido. - Em
Figura 2: Surgimento do menisco nos equipamentos volumétricos.
 1. Introdução Uso da Vidraria Volumétrica e Determinação de Densidade A medição de volumes líquidos é uma parte importante de muitos experimentos. Em alguns casos, os volumes medidos precisam de uma grande
1. Introdução Uso da Vidraria Volumétrica e Determinação de Densidade A medição de volumes líquidos é uma parte importante de muitos experimentos. Em alguns casos, os volumes medidos precisam de uma grande
Experimento 03: Cinética Química
 Experimento 03: Cinética Química 1 OBJETIVO - Verificar alguns fatores que influenciam na velocidade das reações químicas: temperatura, superfície de contato e efeito do catalisador. 2 INTRODUÇÃO A cinética
Experimento 03: Cinética Química 1 OBJETIVO - Verificar alguns fatores que influenciam na velocidade das reações químicas: temperatura, superfície de contato e efeito do catalisador. 2 INTRODUÇÃO A cinética
TITULAÇÃO ÁCIDO-BASE
 ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
Autora: Fernanda Neri. Solução; Ácido; Base; ph; Titulação; Calor de reação; Entalpia de reação; Capacidade térmica mássica.
 cha AL 2.3 -Determinação da entalpia de Neutralização da reação NaOH(aq) + HCl (aq) Autora: Fernanda Neri TI-Nspire Palavras-chave: Solução; Ácido; Base; ph; Titulação; Calor de reação; Entalpia de reação;
cha AL 2.3 -Determinação da entalpia de Neutralização da reação NaOH(aq) + HCl (aq) Autora: Fernanda Neri TI-Nspire Palavras-chave: Solução; Ácido; Base; ph; Titulação; Calor de reação; Entalpia de reação;
I) Comparação da precisão em medidas volumétricas
 EXPERIMENTO 1 PROCEDIMENTOS DE LABORATÓRIO MEDIDAS DE MASSA, VOLUME E TEMPERATURA I) Comparação da precisão em medidas volumétricas Procedimento Experimental Materiais necessários: bureta de 50 ml (1);
EXPERIMENTO 1 PROCEDIMENTOS DE LABORATÓRIO MEDIDAS DE MASSA, VOLUME E TEMPERATURA I) Comparação da precisão em medidas volumétricas Procedimento Experimental Materiais necessários: bureta de 50 ml (1);
QUI095 - Análise Volumétrica
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUI095 - Análise Volumétrica 2 semestre 2018 Prof. Renato Caamrgo Matos Download aulas: http://www.ufjf.br/nupis/
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUI095 - Análise Volumétrica 2 semestre 2018 Prof. Renato Caamrgo Matos Download aulas: http://www.ufjf.br/nupis/
Reconhecer as vidrarias volumétricas utilizadas no preparo de soluções;
 AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
TITULAÇÃO ÁCIDO-BASE. Versão aluno
 ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão aluno O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão aluno O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
EXPERIÊNCIA 8 TITULAÇÃO ÁCIDO-BASE
 EXPERIÊNCIA 8 TITULAÇÃO ÁCIDO-BASE 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: - Determinar a concentração de uma base por titulação. - Determinar a molécula-grama (Mol) de um
EXPERIÊNCIA 8 TITULAÇÃO ÁCIDO-BASE 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: - Determinar a concentração de uma base por titulação. - Determinar a molécula-grama (Mol) de um
Experiência nº 8: Titulações Ácido-Base
 1 UFSC Departamento de Química Área de Educação Química QMC 5119 Introdução ao Laboratório de Química 2011/1 Prof. Marcos Aires de Brito Prof. Fábio Peres Gonçalves Prof. José Carlos Gesser 1. Questões
1 UFSC Departamento de Química Área de Educação Química QMC 5119 Introdução ao Laboratório de Química 2011/1 Prof. Marcos Aires de Brito Prof. Fábio Peres Gonçalves Prof. José Carlos Gesser 1. Questões
Química Geral Experimental II. Experimento Nº2. Fatores que Favorecem uma Reação Química. Profª Maria da Rosa Capri Orientado: João Vitor S.
 Química Geral Experimental II Experimento Nº2 Fatores que Favorecem uma Reação Química Profª Maria da Rosa Capri Orientado: João Vitor S. Fogaça Este material pode ser utilizado exclusivamente para fins
Química Geral Experimental II Experimento Nº2 Fatores que Favorecem uma Reação Química Profª Maria da Rosa Capri Orientado: João Vitor S. Fogaça Este material pode ser utilizado exclusivamente para fins
UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química
 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015.1 1 EXPERIÊNCIA N 0 3: DETERMINAÇÃO DO CALOR DE REAÇÃO E CALOR DE SOLIDIFICAÇÃO 1. Introdução As transformações químicas
UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015.1 1 EXPERIÊNCIA N 0 3: DETERMINAÇÃO DO CALOR DE REAÇÃO E CALOR DE SOLIDIFICAÇÃO 1. Introdução As transformações químicas
Padronizar uma solução aquosa de hidróxido de sódio 0,1mol/L para posteriormente determinar a acidez de amostras.
 Pág. 1 de 6 I - OBJETIVOS Padronizar uma solução de ácido clorídrico 0,1mol/L para posterior determinação de pureza de amostras alcalinas. Padronizar uma solução aquosa de hidróxido de sódio 0,1mol/L para
Pág. 1 de 6 I - OBJETIVOS Padronizar uma solução de ácido clorídrico 0,1mol/L para posterior determinação de pureza de amostras alcalinas. Padronizar uma solução aquosa de hidróxido de sódio 0,1mol/L para
AULA 9. Determinação da entalpia de dissolução de sais. Laboratório de Química QUI OBJETIVOS. Compreender o conceito entalpia;
 AULA 9 Determinação da entalpia de dissolução de sais OBJETIVOS Compreender o conceito entalpia; Determinar a capacidade calorífica de um calorímetro; Determinar a entalpia de dissolução de alguns sais.
AULA 9 Determinação da entalpia de dissolução de sais OBJETIVOS Compreender o conceito entalpia; Determinar a capacidade calorífica de um calorímetro; Determinar a entalpia de dissolução de alguns sais.
TÍTULO: ANÁLISE TITRIMÉTRICA (Volumétrica)
 Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
Componente Curricular: Química dos Alimentos Prof. Barbosa e Prof. Daniel 4º Módulo de Química Procedimento de Prática Experimental Competências: Identificar as propriedades dos alimentos. Identificar
QMC 5119 II Semestre de 2014 EXPERIÊNCIA Nº1 MEDIDAS E TRATAMENTO DE DADOS
 EXPERIÊNCIA Nº1 MEDIDAS E TRATAMENTO DE DADOS 1. Introdução: Química é uma ciência experimental e por isso consideramos importante que você inicie a disciplina Introdução ao Laboratório de Química realizando
EXPERIÊNCIA Nº1 MEDIDAS E TRATAMENTO DE DADOS 1. Introdução: Química é uma ciência experimental e por isso consideramos importante que você inicie a disciplina Introdução ao Laboratório de Química realizando
Física e Química A. Nomes: N.º s : T.ª: Como neutralizar resíduos de ácidos/bases do laboratório de Química da escola?
 Física e Química A 11ºAno - Química AL.2.3. Neutralização: uma reacção de ácido-base Ano lectivo: 2010/2011 Nomes: N.º s : T.ª: PARTE I - Introdução Questão problema Como identificar se os resíduos são
Física e Química A 11ºAno - Química AL.2.3. Neutralização: uma reacção de ácido-base Ano lectivo: 2010/2011 Nomes: N.º s : T.ª: PARTE I - Introdução Questão problema Como identificar se os resíduos são
LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell
 LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell 1. Considere uma solução aquosa de NH 3, preparada na concentração de 0,100 mol L -1. Calcule o ph desta solução. Use K b = 1,8 10-5. 2. Uma alíquota
LISTA DE EXERCÍCIOS # 05 QUÍMICA ANALÍTICA PROF. Wendell 1. Considere uma solução aquosa de NH 3, preparada na concentração de 0,100 mol L -1. Calcule o ph desta solução. Use K b = 1,8 10-5. 2. Uma alíquota
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
02/05/2016. Normas de laboratório INTRODUÇÃO INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE SEGURANÇA NO LABORATÓRIO:
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE Disciplina: Análise de Alimentos Normas de laboratório INTRODUÇÃO Acidente de trabalho é todo evento: inesperado e indesejável que
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE Disciplina: Análise de Alimentos Normas de laboratório INTRODUÇÃO Acidente de trabalho é todo evento: inesperado e indesejável que
XVI Maratona Cearense de Química º Ano. Experiência 1
 - 2013 8º Ano Experiência 1 Material: 1. Erlenmeyer 500mL com tampa 2. Cinco béqueres de 150 ml 3. 100 ml de mel (Karo) 4. 100 ml de glicerina 5. 100 ml de água com corante 6. 100 ml de óleo de cozinha
- 2013 8º Ano Experiência 1 Material: 1. Erlenmeyer 500mL com tampa 2. Cinco béqueres de 150 ml 3. 100 ml de mel (Karo) 4. 100 ml de glicerina 5. 100 ml de água com corante 6. 100 ml de óleo de cozinha
QUIO95 - Análises Volumétricas II semestre 2018
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO95 - Análises Volumétricas II semestre 2018 Preparo e padronização da solução de NaOH Profa. Maria
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO95 - Análises Volumétricas II semestre 2018 Preparo e padronização da solução de NaOH Profa. Maria
Associação Brasileira de Química XIII Maratona Cearense de Química a Fase 1 o Ano 18/08/10. Experiência
 2 a Fase 1 o Ano 18/08/10 Material e Reagentes: Experiência Açúcar (sacarose) Bicarbonato de sódio Álcool etílico Recipiente com graduação (proveta ou seringa) Almofariz com pistilo Fósforo ou isqueiro
2 a Fase 1 o Ano 18/08/10 Material e Reagentes: Experiência Açúcar (sacarose) Bicarbonato de sódio Álcool etílico Recipiente com graduação (proveta ou seringa) Almofariz com pistilo Fósforo ou isqueiro
Laboratório de Análise Instrumental
 Laboratório de Análise Instrumental Prof. Renato Camargo Matos Tutora: Aparecida Maria http://www.ufjf.br/nupis PRÁTICA 10: Estudo da eficiência de uma resina de troca iônica Objetivo: Estudar a eficiência
Laboratório de Análise Instrumental Prof. Renato Camargo Matos Tutora: Aparecida Maria http://www.ufjf.br/nupis PRÁTICA 10: Estudo da eficiência de uma resina de troca iônica Objetivo: Estudar a eficiência
Experimento N 3 DETERMINAÇÃO EXPERIMENTAL DA MASSA MOLAR DO GÁS BUTANO E DO MAGNÉSIO
 Experimento N 3 DETERMINAÇÃO EXPERIMENTAL DA MASSA MOLAR DO GÁS BUTANO E DO MAGNÉSIO 1) INTRODUÇÃO A maioria dos gases reais mostra um comportamento aproximado ao de um gás ideal, especialmente se a pressão
Experimento N 3 DETERMINAÇÃO EXPERIMENTAL DA MASSA MOLAR DO GÁS BUTANO E DO MAGNÉSIO 1) INTRODUÇÃO A maioria dos gases reais mostra um comportamento aproximado ao de um gás ideal, especialmente se a pressão
AULA 10. Verificação da Lei de Hess. Laboratório de Química QUI OBJETIVOS. Determinar o calor envolvido em uma reação química;
 AULA 10 Verificação da Lei de Hess OBJETIVOS Determinar o calor envolvido em uma reação química; Verificar a aplicação da Lei de Hess. Esta aula tem relação com a aula da semana anterior, na qual discutimos
AULA 10 Verificação da Lei de Hess OBJETIVOS Determinar o calor envolvido em uma reação química; Verificar a aplicação da Lei de Hess. Esta aula tem relação com a aula da semana anterior, na qual discutimos
AULA 3. Soluções: preparo e diluição. Laboratório de Química QUI OBJETIVOS
 AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
Análise Volumétrica (Titrimétrica)
 7 (Titrimétrica) Material de Laboratório a) Material Individual (kit): localizado no armário identificado com um número. 1 bureta 25mL 1 proveta 100mL 1 becker 100 ml 1 pipeta volumétrica 10 ml 1 pipeta
7 (Titrimétrica) Material de Laboratório a) Material Individual (kit): localizado no armário identificado com um número. 1 bureta 25mL 1 proveta 100mL 1 becker 100 ml 1 pipeta volumétrica 10 ml 1 pipeta
23/03/2017 Química Licenciatura Prof. Udo Eckard Sinks PESAGEM, MEDIDAS DE TEMPERATURA E MANUSEIO COM RECIPIENTES VOLUMÉTRICOS
 PESAGEM, MEDIDAS DE TEMPERATURA E MANUSEIO COM RECIPIENTES VOLUMÉTRICOS 1. Objetivos No final desta experiência o aluno deverá: Reconhecer a importância das medidas em química. Usar corretamente e ler
PESAGEM, MEDIDAS DE TEMPERATURA E MANUSEIO COM RECIPIENTES VOLUMÉTRICOS 1. Objetivos No final desta experiência o aluno deverá: Reconhecer a importância das medidas em química. Usar corretamente e ler
Comprovação da Lei de Lavoisier
 CENTRO UNIVERSITÁRIO ESTÁCIO DA BAHIA DISCIPLINA: Química Geral CURSOS: Engenharias e Tecnólogo em Petróleo e Gás Prof.: Ederson Aula prática Nº.: 01 Data da realização do Experimento Dia da semana Nº
CENTRO UNIVERSITÁRIO ESTÁCIO DA BAHIA DISCIPLINA: Química Geral CURSOS: Engenharias e Tecnólogo em Petróleo e Gás Prof.: Ederson Aula prática Nº.: 01 Data da realização do Experimento Dia da semana Nº
4) Balão Volumétrico: Recipiente calibrado de precisão, utilizado no preparo de soluções de concentrações definidas. PROVETA OU CILINDRO GRADUADO 5) P
 QUÍMICA I AULA 03: MATÉRIA E MEDIDAS TÓPICO 01: MEDIDAS EM QUÍMICA: MASSA E VOLUME 1.1 MEDIDAS EM QUÍMICA: MASSA E VOLUME OBJETIVOS: 1. Identificar os principais equipamentos e recipientes volumétricos;
QUÍMICA I AULA 03: MATÉRIA E MEDIDAS TÓPICO 01: MEDIDAS EM QUÍMICA: MASSA E VOLUME 1.1 MEDIDAS EM QUÍMICA: MASSA E VOLUME OBJETIVOS: 1. Identificar os principais equipamentos e recipientes volumétricos;
VERIFICANDO A LEI DE LAVOISIER
 VERIFICANDO A LEI DE LAVOISIER Objetivo: Verificar experimentalmente a Lei de Lavoisier, ou seja, que a soma das massas dos reagentes é igual a soma das massas do produto em uma reação química (nessa experiência,
VERIFICANDO A LEI DE LAVOISIER Objetivo: Verificar experimentalmente a Lei de Lavoisier, ou seja, que a soma das massas dos reagentes é igual a soma das massas do produto em uma reação química (nessa experiência,
Relatório 7 Determinação do produto de solubilidade do AgBrO3
 UNIVERSIDADE DE SÃO PAULO QUÍMICA GERAL Prof. Maria Regina Alcântara Relatório 7 Determinação do produto de solubilidade do AgBrO3 Mayara Moretti Vieira Palmieri 7159862 Rodrigo Tonon 7993766 Outubro,
UNIVERSIDADE DE SÃO PAULO QUÍMICA GERAL Prof. Maria Regina Alcântara Relatório 7 Determinação do produto de solubilidade do AgBrO3 Mayara Moretti Vieira Palmieri 7159862 Rodrigo Tonon 7993766 Outubro,
1 Extração Líquido-Líquido
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
VOLUMETRIA DE NEUTRALIZAÇÃO.
 13 Técnica 1. VOLUMETRIA DE NEUTRALIZAÇÃO. PADRONIZAÇÃO DA SOLUÇÃO APROXIMADAMENTE 0,1 M DE HCl COM SOLUÇÃO PADRÃO 0,05 M DE Na 2 CO 3. Colocar no erlenmeyer exatamente 10 ml de solução padrão 0,05 M de
13 Técnica 1. VOLUMETRIA DE NEUTRALIZAÇÃO. PADRONIZAÇÃO DA SOLUÇÃO APROXIMADAMENTE 0,1 M DE HCl COM SOLUÇÃO PADRÃO 0,05 M DE Na 2 CO 3. Colocar no erlenmeyer exatamente 10 ml de solução padrão 0,05 M de
Concentração de soluções e diluição
 Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química. Medidas de Massa, Volume e Temperatura
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química Medidas de Massa, Volume e Temperatura São Carlos, 2019 1 Introdução 2 Introdução DEFINIÇÕES Comprimento: Metro
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química Medidas de Massa, Volume e Temperatura São Carlos, 2019 1 Introdução 2 Introdução DEFINIÇÕES Comprimento: Metro
Equilíbrio Químico (2)
 Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Equilíbrio Químico 1. Introdução Para a reação hipotética geral: aa + bb cc + dd (1) a constante de equilíbrio é dada pela expressão: K = a C c. a D d a A a. a B b (2) Se considerarmos que uma reação ocorra
Ministério da Educação Universidade Federal do Paraná Setor Palotina. Soluções e cálculos de soluções
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula Soluções e cálculos de soluções Prof. Isac G. Rosset Isac G. Rosset -UFPR Mistura vs Composto Mistura Os componentes podem ser
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula Soluções e cálculos de soluções Prof. Isac G. Rosset Isac G. Rosset -UFPR Mistura vs Composto Mistura Os componentes podem ser
Instruções de laboratório
 LCE0182 Química Analítica Quantitativa Instruções de laboratório Wanessa Melchert Mattos wanemelc@usp.br RECOMENDAÇÕES INICIAIS O curso de Química Analítica Quantitativa constará de aulas teóricas e trabalhos
LCE0182 Química Analítica Quantitativa Instruções de laboratório Wanessa Melchert Mattos wanemelc@usp.br RECOMENDAÇÕES INICIAIS O curso de Química Analítica Quantitativa constará de aulas teóricas e trabalhos
SUBSTÂNCIAS E MISTURAS
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
Prova de Química Analítica
 CPF/PASSAPORTE: 1 PROCESSO DE SELEÇÃO E ADMISSÃO AO CURSO DE PARA O SEMESTRE 2017/01 EDITAL PPGQ Nº 002/2016 Prova de Química Analítica Instruções: 1) O candidato deverá identificar-se apenas com o número
CPF/PASSAPORTE: 1 PROCESSO DE SELEÇÃO E ADMISSÃO AO CURSO DE PARA O SEMESTRE 2017/01 EDITAL PPGQ Nº 002/2016 Prova de Química Analítica Instruções: 1) O candidato deverá identificar-se apenas com o número
LABORATÓRIO DE QUÍMICA QUI126 1ª LISTA DE EXERCÍCIOS
 1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES. pv= nrt (01) Gás Ideal : obedece pv=n RT em qualquer condição de T e p.
 PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES 1. Introdução A matéria pode se apresentar nos estados sólido, líquido e gasoso. A temperatura e a pressão são as variáveis responsáveis pelo seu estado físico.
PRÁTICA: DETERMINAÇÃO DA CONSTANTE R DOS GASES 1. Introdução A matéria pode se apresentar nos estados sólido, líquido e gasoso. A temperatura e a pressão são as variáveis responsáveis pelo seu estado físico.
Professor: Melissa Kayser Unidade Curricular: CPGL Aluno: Turma: Data: / /
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CÂMPUS LAGES Professor: Melissa Kayser Unidade Curricular:
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CÂMPUS LAGES Professor: Melissa Kayser Unidade Curricular:
Química Exercícios complementares 1ª série 1º período/2017
 Química Exercícios complementares 1ª série 1º período/2017 Questão 1 - (UECE) A titulação é um procedimento laboratorial que permite determinar a concentração desconhecida de uma substância a partir de
Química Exercícios complementares 1ª série 1º período/2017 Questão 1 - (UECE) A titulação é um procedimento laboratorial que permite determinar a concentração desconhecida de uma substância a partir de
Preparação e padronização de soluções
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático nº 2 Preparação e padronização de soluções
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático nº 2 Preparação e padronização de soluções
Transformações Químicas A reação entre a solução de nitrato de prata e o fio de cobre
 Escola de Educação Básica Olavo Bilac Professora: Eliane Sandra H. Plucinscki Bolsistas: Fernanda Raulino e Solyane Fraga Transformações Químicas A reação entre a solução de nitrato de prata e o fio de
Escola de Educação Básica Olavo Bilac Professora: Eliane Sandra H. Plucinscki Bolsistas: Fernanda Raulino e Solyane Fraga Transformações Químicas A reação entre a solução de nitrato de prata e o fio de
RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D
 RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D QUESTÃO 27 O técnico do laboratório pesou uma pequena barra de alumínio em uma balança cuja incerteza é ± 0,1 g e o valor obtido
RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D QUESTÃO 27 O técnico do laboratório pesou uma pequena barra de alumínio em uma balança cuja incerteza é ± 0,1 g e o valor obtido
IQ-UFG. Curso Experimental de Química Geral e Inorgânica. Prof. Dr. Anselmo
 IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
MATERIAIS PARA FUNDIÇÃO - DETERMINAÇÃO DO FATOR DA SOLUÇÃO DE AZUL DE METILENO POR TITULAÇÃO COM SOLUÇÃO DE CLORETO TITANOSO (TiCl 3 )
 Padronização Folha : 1 de 6 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Aparelhagem 4_ Procedimento 1_ OBJETIVO 1.1_ Esta recomendação prescreve o método de fatoração da solução de azul de metileno utilizada
Padronização Folha : 1 de 6 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Aparelhagem 4_ Procedimento 1_ OBJETIVO 1.1_ Esta recomendação prescreve o método de fatoração da solução de azul de metileno utilizada
AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta
 3 AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta REAGENTES: Solução de permanganato de potássio 0,02 mol L -1,
3 AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta REAGENTES: Solução de permanganato de potássio 0,02 mol L -1,
MATERIAIS PARA FUNDIÇÃO - DETERMINAÇÃO DO ÓXIDO DE FERRO
 Folha : 1 de 5 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Padronização da solução de dicromato de potássio 0,05 N 7_ Resultados 1_ OBJETIVO
Folha : 1 de 5 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Padronização da solução de dicromato de potássio 0,05 N 7_ Resultados 1_ OBJETIVO
EQUIPAMENTO BÁSICO DE LABORATÓRIO
 1 EQUIPAMENTO BÁSICO DE LABORATÓRIO MATERIAL DE VIDRO: TUBO DE ENSAIO Utilizado principalmente para efetuar reações químicas em pequena escala. 2 BÉQUER ou BÉCKER Recipiente com ou sem graduação, utilizado
1 EQUIPAMENTO BÁSICO DE LABORATÓRIO MATERIAL DE VIDRO: TUBO DE ENSAIO Utilizado principalmente para efetuar reações químicas em pequena escala. 2 BÉQUER ou BÉCKER Recipiente com ou sem graduação, utilizado
UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1
 1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 01: Algarismos significativos, medidas e tratamento de dados. Calibração de equipamentos volumétricos 1.
1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química 2015/1 Experiência 01: Algarismos significativos, medidas e tratamento de dados. Calibração de equipamentos volumétricos 1.
Relatório: Volumétrica
 Universidade Tecnológica Federal do Paraná Departamento Acadêmico De Química E Biologia Bacharelado em Química Tecnológica Licenciatura Química Relatório: Preparação, Padronização e Análise Volumétrica
Universidade Tecnológica Federal do Paraná Departamento Acadêmico De Química E Biologia Bacharelado em Química Tecnológica Licenciatura Química Relatório: Preparação, Padronização e Análise Volumétrica
Titulação de cálcio e magnésio no leite com EDTA. Ilustrar: Titulação por retorno Titulação complexométrica, com EDTA
 TRABALHO PRÁTICO Titulação de cálcio e magnésio no leite com Ilustrar: Titulação por retorno Titulação complexométrica, com PARTE EXPERIMENTAL Procedimento para determinação do teor de cálcio mais magnésio
TRABALHO PRÁTICO Titulação de cálcio e magnésio no leite com Ilustrar: Titulação por retorno Titulação complexométrica, com PARTE EXPERIMENTAL Procedimento para determinação do teor de cálcio mais magnésio
Cargo: D-43 - Tecnólogo Laboratório Meio ambiente
 da Prova Prática QUESTÃO 1: Cargo: D-43 - Tecnólogo Laboratório Meio ambiente A titulometria volumétrica envolve a medida de volume de uma solução de concentração conhecida, necessária para reagir essencial
da Prova Prática QUESTÃO 1: Cargo: D-43 - Tecnólogo Laboratório Meio ambiente A titulometria volumétrica envolve a medida de volume de uma solução de concentração conhecida, necessária para reagir essencial
Volumetria. Procedimentos gerais
 Volumetria Procedimentos gerais Métodos volumétricos de análise Consistem na medida do volume de uma solução de concentração conhecida (titulante), necessário para reagir completamente com o a espécie
Volumetria Procedimentos gerais Métodos volumétricos de análise Consistem na medida do volume de uma solução de concentração conhecida (titulante), necessário para reagir completamente com o a espécie
The 44 th IChO Exame Experimental. Versão oficial Brasileira
 1 Instruções (Experimento 1) O caderno do experimento 1 desta prova e suas folhas de resposta é constituído por 10 páginas. Você tem 15 minutos para ler esta prova antes de iniciar a realização das experiências.
1 Instruções (Experimento 1) O caderno do experimento 1 desta prova e suas folhas de resposta é constituído por 10 páginas. Você tem 15 minutos para ler esta prova antes de iniciar a realização das experiências.
UFPB Universidade Federal da Paraíba CCEN Centro de Ciências Exatas e da Natureza Departamento de Química Química Geral e Inorgânica Experimental
 Aula Prática Nº 02 PESAGEM, MEDIDAS DE TEMPERATURA E MANUSEIO COM RECIPIENTES VOLUMÉTRICOS Objetivos No final desta experiência o aluno deverá: Reconhecer a importância das medidas em química. Usar corretamente
Aula Prática Nº 02 PESAGEM, MEDIDAS DE TEMPERATURA E MANUSEIO COM RECIPIENTES VOLUMÉTRICOS Objetivos No final desta experiência o aluno deverá: Reconhecer a importância das medidas em química. Usar corretamente
CQ136 Química Experimental I. Água Dura e Halogênios - Diagrama de Latimer
 1 CQ136 Química Experimental I Água Dura e Halogênios - Diagrama de Latimer Introdução: Os elementos do grupo 2 são tipicamente metálicos, porém menos reativos que os metais alcalinos. Magnésio é um elemento
1 CQ136 Química Experimental I Água Dura e Halogênios - Diagrama de Latimer Introdução: Os elementos do grupo 2 são tipicamente metálicos, porém menos reativos que os metais alcalinos. Magnésio é um elemento
Aula 4 PREPARO DE SOLUÇÕES. META Introduzir técnicas básicas de preparo de soluções.
 PREPARO DE SOLUÇÕES META Introduzir técnicas básicas de preparo de soluções. OBJETIVOS Ao final desta aula o aluno deverá: Fornecer conhecimento necessário para o preparo de soluções. Calcular a concentração
PREPARO DE SOLUÇÕES META Introduzir técnicas básicas de preparo de soluções. OBJETIVOS Ao final desta aula o aluno deverá: Fornecer conhecimento necessário para o preparo de soluções. Calcular a concentração
Qual a quantidade de halogenetos que existe na água do mar?
 20 Qual a quantidade de halogenetos que existe na água do mar? E20-1 o que necessitas cloreto de sódio sólido com grau de pureza analítico cromato de potássio sólido um balão de diluição de 100 ml dois
20 Qual a quantidade de halogenetos que existe na água do mar? E20-1 o que necessitas cloreto de sódio sólido com grau de pureza analítico cromato de potássio sólido um balão de diluição de 100 ml dois
30/03/2017 Química Licenciatura Prof. Udo Eckard Sinks SOLUÇÕES E SOLUBILIDADE
 SOLUÇÕES E SOLUBILIDADE 1. Objetivos Aprender a preparar soluções usando balão volumétrico Reconhecer soluções diluídas, saturadas e supersaturadas Observar a termodinâmica do processo de dissolução 2.
SOLUÇÕES E SOLUBILIDADE 1. Objetivos Aprender a preparar soluções usando balão volumétrico Reconhecer soluções diluídas, saturadas e supersaturadas Observar a termodinâmica do processo de dissolução 2.
Associação Brasileira de Química XI Maratona Cearense de Química a Fase 1 o Ano 22/08/08. Experiência 1
 Associação Brasileira de Química XI Maratona Cearense de Química 2008 2 a Fase 1 o Ano Experiência 1 8 tubos de ensaio. Solução de Ba(OH) 2. Pipeta graduada. 4 conjuntos de mangueiras e rolhas. 1 estante
Associação Brasileira de Química XI Maratona Cearense de Química 2008 2 a Fase 1 o Ano Experiência 1 8 tubos de ensaio. Solução de Ba(OH) 2. Pipeta graduada. 4 conjuntos de mangueiras e rolhas. 1 estante
PRÁTICA 05 - DETERMINAÇÃO DE CLORO ATIVO EM ÁGUA SANITÁRIA E DETERMINAÇÃO IODOMÉTRICA DE ÁCIDO ASCÓRBICO
 PRÁTICA 05 - DETERMINAÇÃO DE CLORO ATIVO EM ÁGUA SANITÁRIA E DETERMINAÇÃO IODOMÉTRICA DE ÁCIDO ASCÓRBICO Aula 15 METAS Familiarizar com as técnicas de preparo e padronização de solução de tiossulfato de
PRÁTICA 05 - DETERMINAÇÃO DE CLORO ATIVO EM ÁGUA SANITÁRIA E DETERMINAÇÃO IODOMÉTRICA DE ÁCIDO ASCÓRBICO Aula 15 METAS Familiarizar com as técnicas de preparo e padronização de solução de tiossulfato de
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA. Tópicos de Química Experimental. Débora Alvim/ Willian Miguel
 MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
CRONOGRAMA DE RECUPERAÇÃO ATIVIDADE DE RECUPERAÇÃO
 CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
CRONOGRAMA DE RECUPERAÇÃO SÉRIE: 2ª série do EM DISCIPLINA: QUÍMICA 1 Caderno Número(s) da(s) Assuntos aula(s) 06 15, 16 e 17 Misturas de soluções com reação e titulação. 06 18 e 19 Termoquímica 07 28
BC-1302 QUÍMICA DOS ELEMENTOS
 PRÁTICA 5: Oxigênio e Enxofre Objetivos Preparar o gás oxigênio, por método laboratorial e estudar algumas de suas propriedades. Estudar o enxofre nas suas variações alotrópicas e algumas de suas reações.
PRÁTICA 5: Oxigênio e Enxofre Objetivos Preparar o gás oxigênio, por método laboratorial e estudar algumas de suas propriedades. Estudar o enxofre nas suas variações alotrópicas e algumas de suas reações.
EXAME PRÁTICO QUÍMICA ORGÂNICA QUÍMICA VERDE
 EXAME PRÁTICO QUÍMICA ORGÂNICA QUÍMICA VERDE O objetivo da Química verde é desenvolver procedimentos químicos que não provoquem a poluição do meio ambiente, utilizando as matérias primas de uma forma eficiente
EXAME PRÁTICO QUÍMICA ORGÂNICA QUÍMICA VERDE O objetivo da Química verde é desenvolver procedimentos químicos que não provoquem a poluição do meio ambiente, utilizando as matérias primas de uma forma eficiente
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
Química. APL 2.3 Determinação da entalpia de neutralização da reação NaHO (aq) + HCl (aq)
 Química APL 2.3 Determinação da entalpia de neutralização da reação NaHO (aq) + HCl (aq) Luísa Neves, 12ºCT 20 de abril de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento 4 Perigos específicos
Química APL 2.3 Determinação da entalpia de neutralização da reação NaHO (aq) + HCl (aq) Luísa Neves, 12ºCT 20 de abril de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento 4 Perigos específicos
Nome:... Escola:... Prova Prática
 Nome:.... Escola:....... Prova Prática Leia atentamente o protocolo antes de iniciar a experiência. Deve ser capaz de o realizar em 50 min, incluindo a lavagem e arrumação do material. Questão 1 2 Total
Nome:.... Escola:....... Prova Prática Leia atentamente o protocolo antes de iniciar a experiência. Deve ser capaz de o realizar em 50 min, incluindo a lavagem e arrumação do material. Questão 1 2 Total
Determinação da Entalpia de uma Reacção
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR
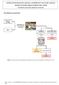 EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
RESINA FENÓLICA PARA FUNDIÇÃO - DETERMINAÇÃO DO TEOR DE FENOL LIVRE
 SUMÁRIO Método de Ensaio Folha : 1 de 5 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Resultados 7_ Anexo A 1_ OBJETIVO 1.1_ Esta recomendação prescreve
SUMÁRIO Método de Ensaio Folha : 1 de 5 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Resultados 7_ Anexo A 1_ OBJETIVO 1.1_ Esta recomendação prescreve
