PROPRIEDADES DA MATÉRIA
|
|
|
- Ana Luísa Leão Marreiro
- 8 Há anos
- Visualizações:
Transcrição
1 PROPRIEDADES DA MATÉRIA Profª Marcelly da Silva Sampaio
2 RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção delimitada de matéria. Objeto- Corpo usado como utensílio ou ferramenta pelo homem.
3 RESUMINDO... Podemos dizer que o ferro é matéria, uma barra de ferro é um corpo e um portão de ferro é um objeto.
4 RELEMBRANDO Molécula- Trata-se da menor porção de uma substância, que conserva as propriedades e a composição da substância. oxigênio Peróxido de oxigênio
5 RELEMBRANDO Átomo- Partículas minúsculas que constituem as moléculas.
6 PROPRIEDADES GERAIS DA MATÉRIA
7 PROPRIEDADES GERAIS DA MATÉRIA São comuns a toda e qualquer espécie de matéria, independentemente da substância de que ela é feita. As principais são: impenetrabilidade, divisibilidade, compressibilidade, elasticidade, massa e volume. IMPENETRABILIDADE: Dois corpos não podem ocupar, simultaneamente o mesmo lugar no espaço.
8 PROPRIEDADES GERAIS DA MATÉRIA DIVISIBILIDADE: Propriedade que a matéria tem se reduzir-se em partículas extremamente pequenas.
9 PROPRIEDADES GERAIS DA MATÉRIA INDESTRUTIBILIDADE: A matéria não pode ser criada nem destruída, apenas transformada.
10 PROPRIEDADES GERAIS DA MATÉRIA COMPRESSIBILIDADE: propriedade da matéria que consiste em ter volume reduzido quando submetida a determinada pressão.
11 PROPRIEDADES GERAIS DA MATÉRIA ELASTICIDADE: Propriedade que a matéria tem de retornar seu volume inicial - após cessada a força que causa a compressão.
12 PROPRIEDADES GERAIS DA MATÉRIA MASSA- Os corpos tem massa! Minha massa é 30 quilos! Massa = Grandeza que pode ser ser medida com balanças. PESO = Calculado P = m x g
13 PROPRIEDADES GERAIS DA MATÉRIA MASSA- QUEM TEM A MAIOR MASSA? ou Faustão, é claro! Ele pesa bem mais que o Leo!
14 PROPRIEDADES GERAIS DA MATÉRIA VOLUME - Todo corpo ocupa um lugar no espaço. A medida que o corpo ocupa no espaço é chamada de VOLUME. Um volume pode ser grande ou pequeno. INDEPENDENTE DA MASSA!
15 PROPRIEDADES DA MATÉRIA
16 PROPRIEDADES DA MATÉRIA Considera-se propriedades, as qualidades da matéria que podem ser medidas. A diversas propriedades dos materiais podem ser classificadas em duas categorias: Propriedades Funcionais da Matéria Propriedades Específicas da Matéria
17 PROPRIEDADES DA MATÉRIA Propriedades Funcionais da Matéria São propriedades particulares de cada matéria e possuem uma classificação de acordo com a sua composição ou com suas características. Esses grupos são chamados funções químicas, e as principais são: ácidos, bases, sais e óxidos que serão estudados oportunamente.
18 PROPRIEDADES DA MATÉRIA Propriedades Funcionais da Matéria ACIDEZ BASICIDADE SALINIDADE OXIDAÇÃO
19 PROPRIEDADES DA MATÉRIA Propriedades Específicas da Matéria São propriedades que permitem identificar uma determinada espécie de matéria. Dentre as propriedades específicas, podemos citar: Propriedades físicas: são propriedades que podem ser observadas e medidas sem alterar a composição de uma substancia. Propriedades organolépticas: odor, sabor. Propriedades químicas: reações químicas.
20 PROPRIEDADES ORGANOLÉPTICAS Cor, sabor, odor... (propriedades organolépticas) Audição Visão Tato Olfato Paladar
21 PROPRIEDADES FÍSICAS São as propriedades que variam conforme as substâncias de que a matéria é feita. Você reconhece seus amigos pela aparência física: altura, peso, cor dos olhos e do cabelo. As principais propriedades físicas são: Ponto de Fusão Ponto de Ebulição Estado da matéria Densidade Solubilidade Condutividade elétrica Maleabilidade Magnetismo Ductibilidade Dureza Brilho Viscosidade
22 PROPRIEDADES FÍSICAS PONTO DE FUSÃO: a que temperatura o sólido se funde? Ponto de fusão é a temperatura constante na qual um sólido se transforma num líquido. PONTO DE EBULIÇÃO: A que temperatura o líquido ferve? Ponto de ebulição é a temperatura constante na qual um líquido passa para o estado gasoso.
23 BRILHO PROPRIEDADES FÍSICAS É a propriedade que faz com que os corpos reflitam a luz de modo diferente. VISCOSIDADE Com que facilidade um liquido escoa?
24 PROPRIEDADES FÍSICAS SOLUBILIDADE: Que massa da substância pode ser dissolvida em determinado volume de água ou em outro solvente? Solubilidade é a quantidade máxima de soluto que pode ser dissolvido no solvente. ESTADO DA MATÉRIA: É um sólido, líquido ou um gás?
25 PROPRIEDADES FÍSICAS CONDUTIVIDADE Certas matérias conduzem bem o calor e a eletricidade, como é o caso dos metais. O mesmo não acontece com outras substâncias, como o iodo, a água e o fósforo, que se apresentam resistentes na condução do calor e da eletricidade.
26 PROPRIEDADES FÍSICAS MAGNETISMO Quando uma determinada matéria tem a propriedade de atrair o ferro, significa que ela apresenta propriedade magnética. Um exemplo de substância magnética natural é a magnetita (pedra imã natural), um minério de ferro. Imã atraindo prego e limalha de ferro.
27 PROPRIEDADES FÍSICAS DUREZA É a resistência que uma espécie de matéria apresenta ao ser riscada por outra. Quanto maior a resistência ao risco, mais dura é a matéria. O diamante é a matéria mais dura que se conhece, é utilizado em brocas que cortam o mármore e em estiletes de cortar vidro.
28 PROPRIEDADES FÍSICAS MALEABILIDADE A matéria que pode ser facilmente transformada em lâminas é considerada maleável. Exemplos: ferro, alumínio, prata, ouro e chumbo.
29 PROPRIEDADES FÍSICAS DUCTIBILIDADE É a propriedade que permite a matéria ser transformada em fio. É o que acontece com os metais: os fios de cobre, por exemplo, são usados para conduzir a eletricidade que chega em nossa casa. Por ser um bom condutor de eletricidade, o cobre é usado como fio que conecta os aparelhos as tomadas
30 PROPRIEDADES FÍSICAS DENSIDADE- É a razão da massa de uma amostra e o seu respectivo volume. Quando dizemos que um material é mais denso que o outro, significa que, comparando-se volumes iguais de ambos, o mais denso é o que possui maior massa
31 DENSIDADE UMA PROPRIEDADE FÍSICA IMPORTANTE E ÚTIL massa (g) Densidade volume (cm 3 ) Mercúrio Platina Alumínio 13,6 g/cm 3 21,5 g/cm 3 2,7 g/cm 3
32 PROPRIEDADES FÍSICAS EX: Compare um isopor e um tijolo. Qual dos dois possui a maior densidade? Isopor Tijolo massa (g) Densidade 3 volume (cm )
33 Problema: Um pedaço de cobre tem uma massa de 57,54 g. Ela tem 9,36 cm de comprimento, 7,23 cm de largura e 0,95 mm de espessura. Calcule a densidade (g/cm 3 ). massa (g) Densidade 3 volume (cm )
34 SOLUÇÃO 1. Coloque as dimensões em unidades iguais mm 1cm 10 mm = cm 2. Calcule o volume em centímetros cúbicos. (9.36 cm)(7.23 cm)(0.095 cm) = 6.4 cm 3 Note que há apenas 2 algarismos significativos na resposta! 3. Calcule a densidade. massa (g) Densidade 3 volume (cm ) g = 9.0 g/ cm3 6.4 cm 3
35 DEPENDÊNCIA DAS PROPRIEDADES FÍSICAS COM TEMPERATURA A TEMPERATURA A temperatura de uma amostra de matéria afeta freqüentemente os valores numéricos de suas propriedades. A densidade é um exemplo importante. Se a água é resfriada a 0ºC, forma-se o gelo sólido. Como o gelo é bem menos denso que a água liquida, então ele flutua.
36 DEPENDÊNCIA DAS PROPRIEDADES FÍSICAS COM TEMPERATURA A TEMPERATURA Devemos especificar a temperatura quando fazemos medidas exatas de volume, uma vez que a densidade dos líquidos varia conforme a temperatura. Portanto, as vidrarias de laboratório devem ser utilizadas para realizar medidas especificas, sempre à temperatura em que foram calibrados.
37 PROPRIEDADES QUÍMICAS São as propriedades que se relacionam com as transformações químicas, existindo a formação de novas substâncias a partir daquilo que existia inicialmente.
38 PROPRIEDADES QUÍMICAS São as propriedades que se relacionam com as transformações químicas, existindo a formação de novas substâncias a partir daquilo que existia inicialmente.
39 PROPRIEDADES QUÍMICAS O QUE É UMA REAÇÃO QUIMICA? Uma reação química é uma alteração química onde matéria (um reagente ou reagentes) se convertem em uma nova substância ou substâncias (um produto ou produtos).
40 PROPRIEDADES QUÍMICAS O QUE É UMA REAÇÃO QUIMICA? Algumas reações ocorrem somente sob determinadas circuntâncias (ex., fornecimento de calor, presença de luz ou eletricidade). Algumas reações são acompanhadas de indicações externas (ex., mudança de cor, desprendimento de gás, calor ou luz).
41 FENÔMENOS FÍSICOS X QUÍMICOS - Fenômenos Físicos: não há mudança na NATUREZA da matéria. -Fenômenos Químicos: há formação de NOVAS substâncias. FÍSICO QUÍMICO
42 ESTADOS FÍSICOS DA MATÉRIA
43 ESTADOS FÍSICOS DA MATÉRIA SÓLIDOS- Matéria possui forma e volume bem definidos Ex: Barra de ouro. LÍQUIDOS- Matéria Possui volume definido e se conforma de acordo com o recipiente em que ela está. Ex: água etc. GASES- Estado onde a matéria não possui volume nem forma definidos..
44 ESTADOS FÍSICOS DA MATÉRIA
45 MUDANÇAS NO ESTADO DA MATÉRIA ÁGUA 0 C 100 C SÓLIDO LÍQUIDO GASOSO Tudo isso a 1 atm de pressão!!!
46 MUDANÇAS NO ESTADO DA MATÉRIA O Monte Everest tem uma altitude de 8836 m acima do mar e pressão atmosférica de 260 mmhg ou 0,34 atm. Nesta pressão a água ferverá a 71 C. Quanto maior a altitude, menor a temperatura de ebulição da água, por isso é importante a panela de pressão para as grandes altitudes.
47 MUDANÇA DE ESTADOS FÍSICOS Fusão Vaporização SÓLIDO LÍQUIDO GASOSO Solidificação Liquefação Sublimação
48 Estados Físicos da Matéria endotérmicos exotérmicos
49 MUDANÇA DE ESTADOS FÍSICOS FUSÃO- Passagem do estado sólido para o estado líquido. Ex: Gelo VAPORIZAÇÃO- Passagem do estado líquido para o estado gasoso. Essa passagem pode ocorrer de três maneiras: O líquido passa para o estado gasoso abaixo da temperatura de ebulição num processo chamado de evaporação. Ex:roupa no varal O líquido passa para o estado gasoso na temperatura de ebulição num processo chamado de ebulição.ex: panela fervendo O líquido passa para o estado gasoso acima da temperatura de ebulição num processo chamado de calefação.ex: Aquecimento de ambientes
50 MUDANÇA DE ESTADOS FÍSICOS LIQUEFAÇÃO- Também chamado de condensação, trata-se do estado gasoso para o estado líquido.ex: tampa da panela SOLIDIFICAÇÃO- Passagem do estado líquido para o estado sólido.ex: formação de gelo SUBLIMAÇÃO- Passagem direta do estado sólido para o estado gasoso. O processo inverso também é chamado de sublimação ou, ressublimação. Ex: naftalina no armário
51 CLASSIFICAÇÃO DA MATÉRIA
52 CLASSIFICAÇÃO DA MATÉRIA SISTEMAS HOMOGÊNEOS SISTEMAS HETEROGÊNEOS SUBSTÂNCIAS PURAS MISTURAS DE UMA FASE MISTURAS DE MAIS DE UMA FASE SUBSTÂNCIAS EM MUDANÇA DE ESTADO SIMPLES COMPOSTA
53 SUBSTÂNCIAS MISTURAS- É todo tipo de matéria cuja fusão e/ou ebulição não ocorrem em temperaturas constantes. A temperatura varia durante a fusão ou durante a ebulição, ou durante ambas. As misturas não possuem ponto de fusão e ponto de ebulição, e sim intervalo de fusão e intervalo de ebulição. A composição é variável. Podem ser classificadas em homogêneas e heterogêneas.
54 SUBSTÂNCIAS Misturas Homogêneas (soluções)- São misturas que se apresentam como um todo uniforme. Elas apresentam as mesmas propriedades físicas e a mesma composição química em toda sua extensão. Apresentam um aspecto único (uma única fase). AR Exemplo: água e álcool, ar atmosférico filtrado, ouro 18 quilates (75% ouro; 12,5% cobre e 12,5% prata). HOMOGÊNEA solução
55 SUBSTÂNCIAS Misturas Heterogêneas- São misturas que não apresentam as mesmas propriedades em toda sua extensão. ÁGUA + AREIA Apresentam mais de uma fase. Exemplo: água e areia, água e óleo, granito, etc. HETEROGÊNEA
56 SUBSTÂNCIAS Fase: corresponde a cada porção uniforme de uma matéria. Componente: corresponde a cada substância que participa da mistura. Mistura de dois ou mais sólidos será sempre heterogênea e cada sólido corresponde a uma fase. Exemplos: Sal e serragem: 2 componentes e 2 fases. Granito: 3 componentes (mica, feldspato e quartzo) e 3 fases.
57 Um material heterogêneo é uma mistura e cada porção homogênea da mesma substância, constituindo, do ponto de vista químico, uma fase. GRANITO mica - partículas escuras e brilhantes; quartzo - fragmentos transparentes e duros; feldspato - cristais oblíquos, translúcidos e acinzentados. Cada fase de uma mistura apresenta propriedades características.
58 SUBSTÂNCIAS SUBSTÂNCIA PURA- É todo tipo de matéria cuja fusão e ebulição ocorrem em temperaturas constantes. Elas possuem propriedades específicas bem definidas, como, por exemplo, cor, cheiro, estado físico, ponto de fusão, ponto de ebulição, etc., e composição química constante. Exemplo: água.
59 SUBSTÂNCIAS SUBSTÂNCIA PURA SIMPLES- São aquelas constituídas por um único elemento químico ex: O 2 para oxigênio e O 3 para ozônio. SUBSTÂNCIA PURA COMPOSTA- São aquelas constituídas por dois ou mais elementos químicos ex: CO 2, H 2 O, NaCl etc. SIMPLES COMPOSTA
60 SUBSTÂNCIAS Substância pura ÁGUA PURA Mistura ÁGUA + SAL
61 ALOTROPIA Fenômeno no qual um elemento químico forma diversas substâncias simples DIFERENTES. Oxigênio e Ozônio Enxofre rômbico e monoclínico Grafita e diamante
62 Matéria (Sistemas Materiais) Sistemas Heterogêneos (as propriedades intrínsecas variam ao longo de sua extensão) Sistemas Homogêneos Processos mecânicos ou físicos As fases podem ser separadas umas das outras por meios mecânicos ou físicos como a centrifugação, catação, filtração, decantação e outros.
63 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS Para a separação de misturas heterogêneas, utilizamos processos mecânicos. Normalmente, esses processos não exigem mudança de estado físico. Exemplos: Sifonação- É um processo usado para separar as fases da mistura heterogênea sólido/líquido e líquido/líquido.
64 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS Flotação- É um processo usado para separar as fases da mistura entre dois sólidos. Consiste em adicionar à mistura a ser desdobrada, um líquido que não reaja e não dissolva nenhum dos componentes e que tenha densidade intermediária à dos mesmos. A fase de menor densidade flutua e a de maior densidade sedimenta.
65 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS Filtração Simples- É o processo de separação das fases de uma mistura heterogênea (sólido-líquido ou sólidogasoso) por meio de uma superfície porosa denominada filtro. Este retém a fase sólida em sua superfície, permitindo somente a passagem da fase líquida ou gasosa. Exemplo: água e areia. A areia fica retida no papel de filtro e é denominada resíduo. A água que atravessa o filtro é o filtrado.
66 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS Decantação- É o processo usado para separar as fases de misturas heterogêneas constituídas por um sólido e um líquido, por líquidos imiscíveis (não se misturam) ou por sólido em um gás. Exemplo 1: mistura água/areia Ao deixarmos a mistura heterogênea sólido-líquido em repouso, lentamente o componente sólido (mais denso), pela ação da gravidade, deposita-se no fundo do frasco, ocorrendo a sedimentação. Quando a sedimentação do componente sólido for completa, inclina-se o recipiente para escoar a fase líquida (decantação).
67 Separação de Misturas Heterogêneas Sistemas Sólido/sólido: Catação Peneiração ou Tamisação Ventilação Levigação Separação Magnética Dissolução Fracionada Flotação Fusão Fracionada
68 Separação de Misturas Heterogêneas Sistemas Sólido/líquido: Sistemas Líquido/líquido: Filtração Destilação Decantação Centrifugação Cristalização Fracionada Sistemas Sólido/gás: Filtração Decantação Câmara de Poeira
69 Matéria (Sistemas Materiais) Sistemas Heterogêneos (as propriedades intrínsecas variam ao longo de sua extensão) Sistemas Homogêneos Misturas Homogêneas ou Soluções (composição variável dentro de certos limites) Substâncias Puras (composição fixa e propriedades intrínsecas invariáveis) Processos Físicos Os componentes de uma solução podem ser separados através de processos físicos como a destilação, a cristalização, a dissolução fracionada, etc.
70 Matéria (Sistemas Materiais) Sistemas Heterogêneos (as propriedades intrínsecas variam ao longo de sua extensão) Sistemas Homogêneos Misturas Homogêneas ou Soluções (composição variável dentro de certos limites) Substâncias Puras (composição fixa e propriedades intrínsecas invariáveis) Substâncias Compostas Substâncias Simples Substâncias compostas só podem ser separadas em outras mais simples através de processos químicos como a decomposição térmica, a eletrólise, a fotólise e outros.
71 ENERGIA
72 ENERGIA É A CAPACIDADE QUE OS CORPOS TÊM PARA REALIZAR TRABALHO. Eu preciso de energia para velejar!
73 Energia do movimento ou cinética: Energia dos corpos em movimento. Exemplo: A energia de usinas hidrelétricas vem do movimento da água. Para velejar, nós usamos a energia do vento ( o ar em movimento). Energia elétrica: É a energia que usamos no dia-a-dia para fazer funcionar muitos aparelhos. Energia luminosa: É a energia da luz. Pode ser natural ou artificial. Energia química: É a energia dos combustíveis e dos alimentos. Energia térmica: Energia que se transfere de um corpo para o outro em forma de calor.
74 MATÉRIA E ENERGIA Durante os fenômenos físicos e químicos,há a liberação ou absorção de energia Energia térmica (CALOR): é a liberação na queima do carvão é absorvida para evaporar a água Energia luminosa (LUZ): é liberada na combustão de uma vela é absorvida na fotossíntese dos vegetais Energia elétrica (ELETRICIDADE): é liberada numa pilha elétrica comum é absorvida na carga de uma bateria de automóvel. OS FENÔMENOS QUÍMICOS LIBERAM OU ABSORVEM MAIS ENERGIA QUE OS FENÔMENOS FÍSICOS.
75 Tipos de substâncias Cada esfera = 1 átomo Átomos: 23 Elementos: 3 Moléculas: 9 Substâncias simples: 3 Substâncias compostas: 2 Cada tipo de esfera = 1 elemento químico
76 Tipos de substâncias Átomos: 31 Elementos químicos: 3 Moléculas: 9 Substâncias simples: 1 Substâncias compostas: 2
77 EXERCÍCIOS DE FIXAÇÃO 1. Considere os sistemas a seguir, em que os átomos são representados por esferas: I II III IV Determine onde encontramos: a) Substância pura; b) Mistura; c) Somente substância pura simples; d) Somente substância pura composta. Considere apenas o sistema III, determine: a) O número de átomos presentes; b) O número de moléculas;
78 2. Considere o sistema representado abaixo. Pode-se descrever o sistema em questão como constituido por: a) Três fases e um componente. b) Duas fases e dois componentes. c) Três fases e dois componentes. d) Três fases e três componentes.
79 3. Observe os seguintes fatos: I Uma pedra de naftalina deixada no armário. II Uma vasilha com água deixada no freezer. III Uma vasilha com água deixada no fogo. IV O derretimento de um pedaço de chumbo quando aquecido. Nestes fatos estão relacionados corretamente os seguintes fenômenos: a) I sublimação, II solidificação, III vaporização, IV fusão. b) I sublimação, II solidificação, III fusão, IV vaporização. c) I fusão, II sublimação, III vaporização, IV solidificação. d) I vaporização, II- solidificação, III fusão, IV sublimação. e) I vaporização, II sublimação, II fusão, IV solidificação.
80 4) Em cinco recipientes encontramos misturas distintas, a saber: Em quais recipientes encontraremos uma mistura homogênea? a) I, II, III e V. b) II, III e V. c) I e V. d) II, III, IV e V. e) II, III e IV.
81 5) Análise os sistemas matérias abaixo, estando ambos em temperatura ambiente. Sistema (I): Mistura de 10g de sal de cozinha, 30g de areia fina, 20 ml de óleo e 100 ml de água. Sistema (II): Mistura de 2,0 L de gás carbônico, 3,0 L de gás nitrogênio e 1,5 L de gás oxigênio. Sobre esses sistemas, é correto afirmar que: a) Ambos são heterogêneos, pois apresentam mais de uma fase. b) Em I, o sistema é bifásico, após forte agitação, e, em II, o sistema é monofásico. c) Em I, o sistema é trifásico, após forte agitação, e, em II, o sistema é monofásico. d) Ambos apresentam uma única fase, formando sistemas homogêneos. e) Em I, o sistema é trifásico, independentemente da ordem de adição dos componentes, e, em II, o sistema é bifásico.
82 UNIDADES DE MEDIDA
83 TIPOS DE OBSERVAÇÕES E MEDIDAS Fazemos observações QUALITATIVAS de reações mudanças de cor e estado físico. Também fazemos MEDIDAS QUANTITATIVAS, que envolvem números. Usamos unidades SI baseadas no sistema métrico.
84 UNIDADE DE MEDIDA Usamos unidades SI baseadas no sistema métrico Comprimento Massa Tempo Temperatura Metro, m Quilograma, kg Segundo, s Graus Celsius, C kelvins, K
85
86 UNIDADES DE COMPRIMENTO 1 quilômetro (km) =? metros (m) 1 metro (m) =? centímetros (cm) 1 centímetro (cm) =? milímetro (mm) 1 nanômetro (nm) = 1,0 x 10-9 metro distância O H = 9,4 x m 9,4 x 10-9 cm 0,094 nm
87
88 TRANSFORMAÇÃO DE UNIDADES Unidade de massa Mg = T Kg g mg X 10 3 X 10 3 X 10 3 Unidade de Volume L ml dm 3 cm 3 X 10 3 X 10 3
89 FIM
PROPRIEDADES DA MATÉRIA
 Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
Propriedades da matéria e mudanças de estado físico
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
QUÍMICA POR QUE ESTUDAR QUÍMICA?
 QUÍMICA POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química
QUÍMICA POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química
ESTUDO DA MATÉRIA. QUÍMICA - Prof. Marcelo Uchida -
 ESTUDO DA MATÉRIA QUÍMICA - Prof. Marcelo Uchida - Matéria Material ou matéria é tudo aquilo que tem massa e ocupa lugar no espaço. Água Ar Madeira Ouro Corpo Porção limitada da matéria Barra de Ouro Tronco
ESTUDO DA MATÉRIA QUÍMICA - Prof. Marcelo Uchida - Matéria Material ou matéria é tudo aquilo que tem massa e ocupa lugar no espaço. Água Ar Madeira Ouro Corpo Porção limitada da matéria Barra de Ouro Tronco
www.professormazzei.com Propriedades da Matéria Folha 1 Prof.: João Roberto Mazzei
 www.professormazzei.com Propriedades da Matéria Folha 1 Prof.: João Roberto Mazzei 01. Classifique cada uma das propriedades específicas referentes ao hidróxido de sódio em: física, química ou organoléptica.
www.professormazzei.com Propriedades da Matéria Folha 1 Prof.: João Roberto Mazzei 01. Classifique cada uma das propriedades específicas referentes ao hidróxido de sódio em: física, química ou organoléptica.
1 Separação de Misturas.
 1 Separação de Misturas. VII. Análise Imediata: Conjunto de processos físicos de separação de substâncias puras presentes nas misturas. A figura abaixo ilustra um procedimento mais completo. Algumas considerações:
1 Separação de Misturas. VII. Análise Imediata: Conjunto de processos físicos de separação de substâncias puras presentes nas misturas. A figura abaixo ilustra um procedimento mais completo. Algumas considerações:
SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES
 SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES PROPRIEDADES DA MATÉRIA 1 - GERAIS: inerentes à toda matéria. São: massa, extensão, impenetrabilidade, divisibilidade, compressibilidade e elasticidade.
SISTEMAS DISPERSOS SOLUÇÕES COLÓIDES SUSPENSÕES PROPRIEDADES DA MATÉRIA 1 - GERAIS: inerentes à toda matéria. São: massa, extensão, impenetrabilidade, divisibilidade, compressibilidade e elasticidade.
MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I
 PROPRIEDADES DA MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I Química É a ciência que estuda a constituição da matéria; ESTRUTURA INTERNA RELAÇÕES ENTRE OS DIVERSOS TIPOS DE MATERIAIS
PROPRIEDADES DA MATÉRIA Mestranda Daniele Potulski Disciplina Química da Madeira I Química É a ciência que estuda a constituição da matéria; ESTRUTURA INTERNA RELAÇÕES ENTRE OS DIVERSOS TIPOS DE MATERIAIS
ESTUDO DA MATÉRIA. QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações.
 QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações. MATÉRIA: é tudo que tem massa e ocupa lugar no espaço. Exemplo: O ar Um balão de festas (bexiga) aumenta
QUÍMICA: é o ramo da ciência que estuda a matéria, suas propriedades, estruturas e transformações. MATÉRIA: é tudo que tem massa e ocupa lugar no espaço. Exemplo: O ar Um balão de festas (bexiga) aumenta
LISTA 1 NÍVEL 1. Material Extra
 LISTA 1 NÍVEL 1 01. (UEMA) Das três fases de uma substância, a que possui menor energia cinética é a fase, cuja característica é apresentar. Os termos que preenchem corretamente as lacunas são: a) Sólida
LISTA 1 NÍVEL 1 01. (UEMA) Das três fases de uma substância, a que possui menor energia cinética é a fase, cuja característica é apresentar. Os termos que preenchem corretamente as lacunas são: a) Sólida
1 - Etapas do método científico.
 1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
AULA 1: MATÉRIAS E SUAS PROPRIEDADES
 AULA 1: MATÉRIAS E SUAS PROPRIEDADES Prof.Me Elayne Química-Aula 1 MATÉRIA Tudo que ocupa lugar no espaço e tem massa é matéria. Energia tudo aquilo que pode modificar a estrutura da matéria, provocar
AULA 1: MATÉRIAS E SUAS PROPRIEDADES Prof.Me Elayne Química-Aula 1 MATÉRIA Tudo que ocupa lugar no espaço e tem massa é matéria. Energia tudo aquilo que pode modificar a estrutura da matéria, provocar
3. Elemento Químico Elemento Químico é um conjunto de átomos iguais (do mesmo tipo). E na linguagem dos químicos eles são representados por Símbolos.
 Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
Box 2. Estado da solução Estado do solvente Estado do soluto Exemplos
 MISTURA E SOLUBILIDADE Box 2 Grande parte das substancias encontradas no dia-a-dia são misturas que sob o aspecto macroscópico apresentam-se com o aspecto homogêneo (uma única fase) ou heterogêneo (mais
MISTURA E SOLUBILIDADE Box 2 Grande parte das substancias encontradas no dia-a-dia são misturas que sob o aspecto macroscópico apresentam-se com o aspecto homogêneo (uma única fase) ou heterogêneo (mais
Introdução. Gerais. Funcionais. Propriedades. da Matéria Organolépticas. Específicas. Químicas. Físicas. Química. Rômulo
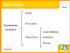 Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
Exercícios para a Prova 1 de Química - 1 Trimestre
 Exercícios para a Prova 1 de Química - 1 Trimestre 1. Seja o esquema: Entre as alternativas abaixo, indique as corretas sobre o esquema: a) Temos 5 componentes. b) É formado por 2 substâncias simples.
Exercícios para a Prova 1 de Química - 1 Trimestre 1. Seja o esquema: Entre as alternativas abaixo, indique as corretas sobre o esquema: a) Temos 5 componentes. b) É formado por 2 substâncias simples.
Separação de Misturas
 Separação de Misturas Misturas que possuem propriedades diferentes em sua extensão. Pode-se notar superfície de separação entre os componentes. O componente mais denso encontra-se na parte inferior numa
Separação de Misturas Misturas que possuem propriedades diferentes em sua extensão. Pode-se notar superfície de separação entre os componentes. O componente mais denso encontra-se na parte inferior numa
UFU 2014 VESTIBULAR DE MAIO 1ª FASE
 UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
Vazamento cria dúvidas sobre futuro da energia nuclear
 Educadora: Daiana de Oliveira Componente Curricular: Ciências Data: / /2012 Estudante: 9º ano Vazamento cria dúvidas sobre futuro da energia nuclear Tragédia na usina de Fukushima, no Japão, faz com que
Educadora: Daiana de Oliveira Componente Curricular: Ciências Data: / /2012 Estudante: 9º ano Vazamento cria dúvidas sobre futuro da energia nuclear Tragédia na usina de Fukushima, no Japão, faz com que
O interesse da Química é analisar as...
 O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
SEPARAÇÃO DE MISTURAS. Pr ofª Tatiana Lima
 SEPARAÇÃO DE MISTURAS Pr ofª Tatiana Lima As separações de misturas estão baseadas nas diferenças de propriedades entre os componentes de uma mistura. Soluções são misturas homogêneas, onde o solvente
SEPARAÇÃO DE MISTURAS Pr ofª Tatiana Lima As separações de misturas estão baseadas nas diferenças de propriedades entre os componentes de uma mistura. Soluções são misturas homogêneas, onde o solvente
Química - Profa. GRAÇA PORTO
 Disciplina: Química Química - Profa. GRAÇA PORTO ESTUDO DAS SUBSTÂNCIAS E MISTURAS Você sabe caracterizar a quanto ao sabor, a cor e ao cheiro? E o sal? Quais são as características do açúcar? Agora, tente
Disciplina: Química Química - Profa. GRAÇA PORTO ESTUDO DAS SUBSTÂNCIAS E MISTURAS Você sabe caracterizar a quanto ao sabor, a cor e ao cheiro? E o sal? Quais são as características do açúcar? Agora, tente
Texto: QUÍMICA NO COTIDIANO. Outras disciplinas que são citadas com frequência são a química molecular, a eletroquímica, a
 Texto: QUÍMICA NO COTIDIANO Outras disciplinas que são citadas com frequência são a química molecular, a eletroquímica, a química nuclear, a radioquímica e a estereoquímica. É de costume incluir a química
Texto: QUÍMICA NO COTIDIANO Outras disciplinas que são citadas com frequência são a química molecular, a eletroquímica, a química nuclear, a radioquímica e a estereoquímica. É de costume incluir a química
Equipe de Química QUÍMICA
 Aluno (a): Série: 3ª Turma: TUTORIAL 11R Ensino Médio Equipe de Química Data: QUÍMICA SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas
Aluno (a): Série: 3ª Turma: TUTORIAL 11R Ensino Médio Equipe de Química Data: QUÍMICA SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas
FORTALECENDO SABERES CONTEÚDO E HABILIDADES DINÂMICA LOCAL INTERATIVA CIÊNCIAS DESAFIO DO DIA. Conteúdo: - Como as substâncias são formadas
 CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Conteúdo: - Como as substâncias são formadas CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Habilidades: - Descobrir que as substâncias
CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Conteúdo: - Como as substâncias são formadas CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Habilidades: - Descobrir que as substâncias
SISTEMAS MATERIAIS - 2012
 SISTEMAS MATERIAIS - 2012 1- (UFV) A obtenção de gasolina a partir do petróleo é feita por: A) destilação fracionada; B) destilação simples; C) filtração simples; D) filtração sob pressão reduzida; E)
SISTEMAS MATERIAIS - 2012 1- (UFV) A obtenção de gasolina a partir do petróleo é feita por: A) destilação fracionada; B) destilação simples; C) filtração simples; D) filtração sob pressão reduzida; E)
03/04/2016 AULAS 11 E 12 SETOR A
 AULAS 11 E 12 SETOR A 1 Propriedade coligativa das soluções: são aquelas que depende unicamente do número de partículas dissolvidas. Ou seja: a adição de um soluto não-volátil a uma solução provoca mudanças
AULAS 11 E 12 SETOR A 1 Propriedade coligativa das soluções: são aquelas que depende unicamente do número de partículas dissolvidas. Ou seja: a adição de um soluto não-volátil a uma solução provoca mudanças
CADERNO DE EXERCÍCIOS 1D
 CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
Química Geral Materiais Homogêneos e Heterogêneos
 Química Geral Materiais Homogêneos e Heterogêneos 1. (Uepg 2013) Quanto às características das substâncias puras e das misturas, assinale o que for correto. 01) Misturas sólidas homogêneas não podem ser
Química Geral Materiais Homogêneos e Heterogêneos 1. (Uepg 2013) Quanto às características das substâncias puras e das misturas, assinale o que for correto. 01) Misturas sólidas homogêneas não podem ser
Ciências E Programa de Saúde
 Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 18 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE SP Grandes realizações são possíveis quando se dá atenção aos pequenos
Governo do Estado de São Paulo Secretaria de Estado da Educação Ciências E Programa de Saúde 18 CEEJA MAX DADÁ GALLIZZI PRAIA GRANDE SP Grandes realizações são possíveis quando se dá atenção aos pequenos
CONVERSÃO DE TEMPERATURA
 CONVERSÃO DE TEMPERATURA Caro(a) e estimado(a) aluno(a), entre neste link e observe um interessante programa de conversão de temperaturas. Mas não o utilize para resolver esta lista. Não tente enganar
CONVERSÃO DE TEMPERATURA Caro(a) e estimado(a) aluno(a), entre neste link e observe um interessante programa de conversão de temperaturas. Mas não o utilize para resolver esta lista. Não tente enganar
Disciplina de Físico Química I - Tipos de Soluções Propriedades Coligativas. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.
 Disciplina de Físico Química I - Tipos de Soluções Propriedades Coligativas. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br Misturas - soluções A grande maioria dos sistemas encontrados
Disciplina de Físico Química I - Tipos de Soluções Propriedades Coligativas. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br Misturas - soluções A grande maioria dos sistemas encontrados
DISPERSÕES. Profa. Kátia Aquino
 DISPERSÕES Profa. Kátia Aquino O que é uma dispersão do ponto de vista químico? Mistura de duas ou mais substâncias, em que as partículas de uma fase a fase dispersa se encontram distribuidas em outra
DISPERSÕES Profa. Kátia Aquino O que é uma dispersão do ponto de vista químico? Mistura de duas ou mais substâncias, em que as partículas de uma fase a fase dispersa se encontram distribuidas em outra
Exercícios Sobre LigaÇões iônicas
 Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
n 1 L 1 n 2 L 2 Supondo que as ondas emergentes podem interferir, é correto afirmar que
 QUESTÃO 29 QUESTÃO 27 Uma escada de massa m está em equilíbrio, encostada em uma parede vertical, como mostra a figura abaixo. Considere nulo o atrito entre a parede e a escada. Sejam µ e o coeficiente
QUESTÃO 29 QUESTÃO 27 Uma escada de massa m está em equilíbrio, encostada em uma parede vertical, como mostra a figura abaixo. Considere nulo o atrito entre a parede e a escada. Sejam µ e o coeficiente
Leonnardo Cruvinel Furquim TERMOQUÍMICA 2
 Leonnardo Cruvinel Furquim TERMOQUÍMICA 2 Calorimetria Os reagentes são colocados num recipiente de aço de paredes resistentes chamado bomba, o qual está imerso numa quantidade de água contida num recipiente
Leonnardo Cruvinel Furquim TERMOQUÍMICA 2 Calorimetria Os reagentes são colocados num recipiente de aço de paredes resistentes chamado bomba, o qual está imerso numa quantidade de água contida num recipiente
Aulas 13 e 14. Soluções
 Aulas 13 e 14 Soluções Definição Solução é a denominação ao sistema em que uma substância está distribuída, ou disseminada, numa segunda substância sob forma de pequenas partículas. Exemplos Dissolvendo-se
Aulas 13 e 14 Soluções Definição Solução é a denominação ao sistema em que uma substância está distribuída, ou disseminada, numa segunda substância sob forma de pequenas partículas. Exemplos Dissolvendo-se
ESTADOS FÍSICOS DA MATÉRIA
 ESTADOS FÍSICOS DA MATÉRIA A matéria pode se apresentar em diferentes estados físicos, como sólido, líquido e gasoso. Algumas propriedades da matéria dependem de seu estado físico. O estado sólido Em determinada
ESTADOS FÍSICOS DA MATÉRIA A matéria pode se apresentar em diferentes estados físicos, como sólido, líquido e gasoso. Algumas propriedades da matéria dependem de seu estado físico. O estado sólido Em determinada
7 PARTÍCULAS SÓLIDAS
 7 PARTÍCULAS SÓLIDAS O CONHECIMENTO DAS PROPRIEDADES DAS PARTÍCULAS SÓLIDAS É FUNDAMENTAL PARA AS OPERAÇÕES LISTADAS ABAIXO: FRAGMENTAÇÃO PENEIRAMENTO FLUIDIZAÇÃO MISTURA ARMAZENAMENTO SEPARAÇÕES MECÂNICAS
7 PARTÍCULAS SÓLIDAS O CONHECIMENTO DAS PROPRIEDADES DAS PARTÍCULAS SÓLIDAS É FUNDAMENTAL PARA AS OPERAÇÕES LISTADAS ABAIXO: FRAGMENTAÇÃO PENEIRAMENTO FLUIDIZAÇÃO MISTURA ARMAZENAMENTO SEPARAÇÕES MECÂNICAS
Tecnologia Mecânica MATERIAIS. Roda de aço. Mapa do Brasil em cobre. Prof. Marcio Gomes
 Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Potência elétrica. 06/05/2011 profpeixinho.orgfree.com pag.1
 1. (Unicamp) Um aluno necessita de um resistor que, ligado a uma tomada de 220 V, gere 2200 W de potência térmica. Ele constrói o resistor usando fio de constante N. 30 com área de seção transversal de
1. (Unicamp) Um aluno necessita de um resistor que, ligado a uma tomada de 220 V, gere 2200 W de potência térmica. Ele constrói o resistor usando fio de constante N. 30 com área de seção transversal de
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
A Matéria Química Geral
 Química Geral A Matéria Tudo o que ocupa lugar no espaço e tem massa. A matéria nem sempre é visível Noções Preliminares Prof. Patrícia Andrade Mestre em Agricultura Tropical Massa, Inércia e Peso Massa:
Química Geral A Matéria Tudo o que ocupa lugar no espaço e tem massa. A matéria nem sempre é visível Noções Preliminares Prof. Patrícia Andrade Mestre em Agricultura Tropical Massa, Inércia e Peso Massa:
muito gás carbônico, gás de enxofre e monóxido de carbono. extremamente perigoso, pois ocupa o lugar do oxigênio no corpo. Conforme a concentração
 A UU L AL A Respiração A poluição do ar é um dos problemas ambientais que mais preocupam os governos de vários países e a população em geral. A queima intensiva de combustíveis gasolina, óleo e carvão,
A UU L AL A Respiração A poluição do ar é um dos problemas ambientais que mais preocupam os governos de vários países e a população em geral. A queima intensiva de combustíveis gasolina, óleo e carvão,
SOLUÇÕES SOLUÇÕES MISTURAS
 MISTURAS SOLUÇÕES Quando juntamos duas espécies químicas diferentes e, não houver reação química entre elas, isto é, não houver formação de nova(s) espécie(s), teremos uma mistura. Exemplos: Mistura de
MISTURAS SOLUÇÕES Quando juntamos duas espécies químicas diferentes e, não houver reação química entre elas, isto é, não houver formação de nova(s) espécie(s), teremos uma mistura. Exemplos: Mistura de
SEPARAÇÃO DE MISTURAS HETEROGÊNEAS. (Processos mecânicos de separação) Sistema sólido - sólido
 SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas
SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas
Química na cozinha: www.interaulaclube.com.br
 Química na cozinha: funções químicas Na Aula 43, você estudou um processo chamado fermentação, que determinados seres vivos promovem para sobreviver. Você aprendeu qual a importância da fermentação para
Química na cozinha: funções químicas Na Aula 43, você estudou um processo chamado fermentação, que determinados seres vivos promovem para sobreviver. Você aprendeu qual a importância da fermentação para
Introdução à Química Inorgânica
 Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE
 A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE Matéria é tudo em que você puder pensar, destas páginas que você está lendo até a cadeira que você está sentado, a água que
A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE Matéria é tudo em que você puder pensar, destas páginas que você está lendo até a cadeira que você está sentado, a água que
23-05-2012. Sumário. Materiais. Algumas propriedades físicas e químicas dos materiais
 Sumário Correção do TPC. Algumas propriedades físicas características de substâncias. Os estados físicos da matéria e as mudanças de estado; Temperatura de fusão e temperatura de ebulição; Densidade. Estados
Sumário Correção do TPC. Algumas propriedades físicas características de substâncias. Os estados físicos da matéria e as mudanças de estado; Temperatura de fusão e temperatura de ebulição; Densidade. Estados
Exercícios de Revisão
 Exercícios de Revisão a) I, II, III b) II, III, I c) II, I, III d) III, I, II e) I, III, II 01) (PUC - SP) O conceito de elemento químico está mais relacionado com a idéia de: a) átomo. b) molécula. c)
Exercícios de Revisão a) I, II, III b) II, III, I c) II, I, III d) III, I, II e) I, III, II 01) (PUC - SP) O conceito de elemento químico está mais relacionado com a idéia de: a) átomo. b) molécula. c)
Aula 5: Minerais e Rochas Prof. Daniel Caetano
 Geologia para Engenharia 1 Aula 5: Minerais e Rochas Prof. Daniel Caetano Objetivo: Compreender o que são minerais, suas propriedades e sua identificação e classificação. INTRODUÇÃO - "Pedras Preciosas"
Geologia para Engenharia 1 Aula 5: Minerais e Rochas Prof. Daniel Caetano Objetivo: Compreender o que são minerais, suas propriedades e sua identificação e classificação. INTRODUÇÃO - "Pedras Preciosas"
CAPÍTULO 6 Termologia
 CAPÍTULO 6 Termologia Introdução Calor e Temperatura, duas grandezas Físicas bastante difundidas no nosso dia-a-dia, e que estamos quase sempre relacionando uma com a outra. Durante a explanação do nosso
CAPÍTULO 6 Termologia Introdução Calor e Temperatura, duas grandezas Físicas bastante difundidas no nosso dia-a-dia, e que estamos quase sempre relacionando uma com a outra. Durante a explanação do nosso
Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello
 Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
(J/gºC) Água 4,19 Petróleo 2,09 Glicerin a 2,43. Leite 3,93 Mercúri o 0,14. a) a água. b) o petróleo. c) a glicerina. d) o leite.
 COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
TERMOQUÍMICA. Desta forma podemos dizer que qualquer mudança química geralmente envolve energia.
 TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
Aluno: Série:_2º Data: Matéria: Fisica Turno: Valor: Nota: Supervisoras: Rejane/Betânia
 ESCOLA ESTADUAL DR JOSÉ MARQUES DE OLIVEIRA TRABALHO DE PROGRESSÃO PARCIAL ENSINO MÉDIO - 2012 ESCOLA REFERENCIA Aluno: Série:_2º Data: Matéria: Fisica Turno: Valor: Nota: Supervisoras: Rejane/Betânia
ESCOLA ESTADUAL DR JOSÉ MARQUES DE OLIVEIRA TRABALHO DE PROGRESSÃO PARCIAL ENSINO MÉDIO - 2012 ESCOLA REFERENCIA Aluno: Série:_2º Data: Matéria: Fisica Turno: Valor: Nota: Supervisoras: Rejane/Betânia
ELETRODINÂMICA: ASSOCIAÇÃO DE RESISTORES E EFEITO JOULE¹
 ELETRODINÂMICA: ASSOCIAÇÃO DE RESISTORES E EFEITO JOULE¹ Ana Célia Alves dos Santos² Débora da Cruz Alves² Gustavo Gomes Benevides² Júlia Fabiana de Oliveira Barboza² Stefanie Esteves da Silva² Stephanye
ELETRODINÂMICA: ASSOCIAÇÃO DE RESISTORES E EFEITO JOULE¹ Ana Célia Alves dos Santos² Débora da Cruz Alves² Gustavo Gomes Benevides² Júlia Fabiana de Oliveira Barboza² Stefanie Esteves da Silva² Stephanye
TERMOLOGIA. Parte da Física que estudar a relação de troca de calor entre os corpos.
 TERMOLOGIA Parte da Física que estudar a relação de troca de calor entre os corpos. DIVISÕES TERMOMETRIA CALORIMETRIA TERMODINÂMICA TERMOMETRIA Estuda a temperatura dos corpos Temperatura: Agitação das
TERMOLOGIA Parte da Física que estudar a relação de troca de calor entre os corpos. DIVISÕES TERMOMETRIA CALORIMETRIA TERMODINÂMICA TERMOMETRIA Estuda a temperatura dos corpos Temperatura: Agitação das
Magnetismo: Campo Magnético
 INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA PARAÍBA Campus Princesa Isabel Magnetismo: Campo Magnético Disciplina: Física III Professor: Carlos Alberto Aurora Austral Polo Sul Aurora Boreal Polo
INSTITUTO FEDERAL DE EDUCAÇÃO CIÊNCIA E TECNOLOGIA PARAÍBA Campus Princesa Isabel Magnetismo: Campo Magnético Disciplina: Física III Professor: Carlos Alberto Aurora Austral Polo Sul Aurora Boreal Polo
Química Geral PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1
 Química Geral AULA 1 PROPRIEDADES GERAIS DA MATÉRIA E CONCEITOS INICIAIS PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1 Tópicos Matéria Energia Diagrama de Mudança de Fases Ciclo da Água Universo e
Química Geral AULA 1 PROPRIEDADES GERAIS DA MATÉRIA E CONCEITOS INICIAIS PROF. LARISSA ROCHA ALMEIDA - CURSINHO VITORIANO 1 Tópicos Matéria Energia Diagrama de Mudança de Fases Ciclo da Água Universo e
ESTADOS DA MATÉRIA. O átomo é composto por outras partículas ainda menores.
 ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
Química SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS
 SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
Prova de Química Resolvida Segunda Etapa Vestibular UFMG 2011 Professor Rondinelle Gomes Pereira
 QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
Prof. André Motta - mottabip@hotmail.com_ C) O calor contido em cada um deles é o mesmo. D) O corpo de maior massa tem mais calor que os outros dois.
 Exercícios de Termometria 1-Calor é: A) Energia que aumenta em um corpo quando ele se aquece. B) Energia que sempre pode ser convertida integralmente em trabalho. C) O agente físico responsável pelo aquecimento
Exercícios de Termometria 1-Calor é: A) Energia que aumenta em um corpo quando ele se aquece. B) Energia que sempre pode ser convertida integralmente em trabalho. C) O agente físico responsável pelo aquecimento
IX Olimpíada Catarinense de Química 2013. Etapa I - Colégios
 I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
A PILHA ELÉTRICA VOLTAGEM CORRENTE ELÉTRICA
 VOLTAGEM A PILHA ELÉTRICA 3.1- A PILHA ELÉTRICA Fizeram muita coisa conosco. Construíram máquinas que nos tiravam dos átomos da superfície de um corpo e nos colocavam na superfície de um outro corpo. Com
VOLTAGEM A PILHA ELÉTRICA 3.1- A PILHA ELÉTRICA Fizeram muita coisa conosco. Construíram máquinas que nos tiravam dos átomos da superfície de um corpo e nos colocavam na superfície de um outro corpo. Com
Conteúdo: Aula: 12 assíncrona. Ciclo da água e dos nutrientes. Ciclo do nitrogênio, carbono e oxigênio. CONTEÚDO E HABILIDADES
 CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA DINÂMICA LOCAL INTERATIVA Aula: 12 assíncrona Conteúdo: Ciclo da água e dos nutrientes. Ciclo do nitrogênio, carbono e oxigênio. 2 CONTEÚDO E
CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA DINÂMICA LOCAL INTERATIVA Aula: 12 assíncrona Conteúdo: Ciclo da água e dos nutrientes. Ciclo do nitrogênio, carbono e oxigênio. 2 CONTEÚDO E
CA 6 - Apropriar-se de conhecimentos da Física para, em situações problema, interpretar, avaliar ou planejar intervenções científico-tecnológicas.
 COMPETÊNCIAS E HABILIDADES CADERNO 9 PROF.: Célio Normando CA 6 - Apropriar-se de conhecimentos da Física para, em situações problema, interpretar, avaliar ou planejar intervenções científico-tecnológicas.
COMPETÊNCIAS E HABILIDADES CADERNO 9 PROF.: Célio Normando CA 6 - Apropriar-se de conhecimentos da Física para, em situações problema, interpretar, avaliar ou planejar intervenções científico-tecnológicas.
Propriedades físicas e químicas das substâncias
 Propriedades físicas e químicas das substâncias Na Natureza há uma grande diversidade de materais. Muitos desses materais são substâncias mas será que são puras? Há substâncias que, mesmo misturadas com
Propriedades físicas e químicas das substâncias Na Natureza há uma grande diversidade de materais. Muitos desses materais são substâncias mas será que são puras? Há substâncias que, mesmo misturadas com
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos
 Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
MATÉRIA E SUAS PROPRIEDADES
 01- Conceitue matéria. Exemplifique. MATÉRIA E SUAS PROPRIEDADES 02- Do que é constituída a matéria? 03- Qual a finalidade do estudo da Química? 04- Como a matéria, provavelmente, foi originada? 05- O
01- Conceitue matéria. Exemplifique. MATÉRIA E SUAS PROPRIEDADES 02- Do que é constituída a matéria? 03- Qual a finalidade do estudo da Química? 04- Como a matéria, provavelmente, foi originada? 05- O
SOLUÇÕES. As misturas homogêneas possuem uma fase distinta. As misturas heterogêneas possuem duas ou mais fases distintas.
 QUÍMICA PROF - 3C13 SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas heterogêneas possuem duas ou mais fases distintas. Solução é
QUÍMICA PROF - 3C13 SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas heterogêneas possuem duas ou mais fases distintas. Solução é
As Propriedades das Misturas (Aulas 18 a 21)
 As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
BOLETIM TÉCNICO LAMINADOS
 A BOLETIM TÉCNICO LAMINADOS Última atualização Maio/2011 CLASSIFICAÇÃO DAS FOLHAS DE ALUMÍNIO A folha de Alumínio é um produto resultante do processo de laminação a frio com secção transversal variando
A BOLETIM TÉCNICO LAMINADOS Última atualização Maio/2011 CLASSIFICAÇÃO DAS FOLHAS DE ALUMÍNIO A folha de Alumínio é um produto resultante do processo de laminação a frio com secção transversal variando
 SEGURANÇA E TÉCNICA DE LABORATÓRIO AULA 01: ORGANIZANDO O LABORATÓRIO TÓPICO 03: ORGANIZAÇÃO LABORATORIAL O laboratório, seja de uma indústria, de um centro de pesquisa ou de uma instituição de ensino
SEGURANÇA E TÉCNICA DE LABORATÓRIO AULA 01: ORGANIZANDO O LABORATÓRIO TÓPICO 03: ORGANIZAÇÃO LABORATORIAL O laboratório, seja de uma indústria, de um centro de pesquisa ou de uma instituição de ensino
DILATAÇÃO TÉRMICA. A figura mostra uma barra metálica, em duas temperaturas diferentes: Verifica-se, experimentalmente, que:
 DILATAÇÃO TÉRMICA Uma variação de temperatura pode alterar o valor das grandezas de um corpo, tais como: a pressão de um gás, cor e um metal, a resistência elétrica de um condutor de eletricidade, a altura
DILATAÇÃO TÉRMICA Uma variação de temperatura pode alterar o valor das grandezas de um corpo, tais como: a pressão de um gás, cor e um metal, a resistência elétrica de um condutor de eletricidade, a altura
GOVERNO DO ESTADO DE MATO GROSSO DO SUL SECRETARIA DE ESTADO DE EDUCAÇÃO
 Conteúdos curriculares de química: 2. ano - 1. bimestre: Dispersões (definição, classificação, características); Soluções (conceito e regra da solubilidade, curva de solubilidade, classificação); Concentração
Conteúdos curriculares de química: 2. ano - 1. bimestre: Dispersões (definição, classificação, características); Soluções (conceito e regra da solubilidade, curva de solubilidade, classificação); Concentração
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS
 TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
Exemplos de condutores: cobre, alumínio, ferro, grafite, etc. Exemplos de isolantes: vidro, mica, fenolite, borracha, porcelana, água pura, etc.
 Condutores e Isolantes Condutores: São materiais caracterizados por possuírem no seu interior, portadores livres de cargas elétricas (elétrons livres), desta forma, permitindo a passagem de uma corrente
Condutores e Isolantes Condutores: São materiais caracterizados por possuírem no seu interior, portadores livres de cargas elétricas (elétrons livres), desta forma, permitindo a passagem de uma corrente
-2013- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE
 -2013- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
-2013- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
Profa. Maria Fernanda - Química nandacampos.mendonc@gmail.com
 Profa. Maria Fernanda - Química nandacampos.mendonc@gmail.com Estudo de caso Reúnam-se em grupos de máximo 5 alunos e proponha uma solução para o seguinte caso: A morte dos peixes ornamentais. Para isso
Profa. Maria Fernanda - Química nandacampos.mendonc@gmail.com Estudo de caso Reúnam-se em grupos de máximo 5 alunos e proponha uma solução para o seguinte caso: A morte dos peixes ornamentais. Para isso
Disciplina de Físico Química I - Gases Ideais- Lei de Boyle-Charles. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.
 Disciplina de Físico Química I - Gases Ideais- Lei de Boyle-Charles. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br A físico-química é a disciplina que estuda as propriedades físicas e
Disciplina de Físico Química I - Gases Ideais- Lei de Boyle-Charles. Prof. Vanderlei Inácio de Paula contato: vanderleip@anchieta.br A físico-química é a disciplina que estuda as propriedades físicas e
Ensaio de impacto. Os veículos brasileiros têm, em geral, suspensão
 A UU L AL A Ensaio de impacto Os veículos brasileiros têm, em geral, suspensão mais reforçada do que a dos similares europeus. Não é à toa. As condições de nossas estradas e ruas requerem esse reforço,
A UU L AL A Ensaio de impacto Os veículos brasileiros têm, em geral, suspensão mais reforçada do que a dos similares europeus. Não é à toa. As condições de nossas estradas e ruas requerem esse reforço,
Nome:...N o...turma:... Data: / / ESTUDO DOS GASES E TERMODINÂMICA
 Ensino Médio Nome:...N o...turma:... Data: / / Disciplina: Física Dependência Prof. Marcelo Vettori ESTUDO DOS GASES E TERMODINÂMICA I- ESTUDO DOS GASES 1- Teoria Cinética dos Gases: as moléculas constituintes
Ensino Médio Nome:...N o...turma:... Data: / / Disciplina: Física Dependência Prof. Marcelo Vettori ESTUDO DOS GASES E TERMODINÂMICA I- ESTUDO DOS GASES 1- Teoria Cinética dos Gases: as moléculas constituintes
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 24
 AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 24 9º NO DO ENSINO FUNDAMENTAL - 1º ANO DO ENSINO MÉDIO OBJETIVO Diversos experimentos, usando principalmente água e materiais de fácil obtenção, são
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 24 9º NO DO ENSINO FUNDAMENTAL - 1º ANO DO ENSINO MÉDIO OBJETIVO Diversos experimentos, usando principalmente água e materiais de fácil obtenção, são
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Estudo das dispersões Definição, classificação, estudo dos coloides, coeficiente de solubilidade... 1 Módulo 2 Concentração de soluções... 3 Módulo 3 Propriedades
Resoluções das Atividades Sumário Módulo 1 Estudo das dispersões Definição, classificação, estudo dos coloides, coeficiente de solubilidade... 1 Módulo 2 Concentração de soluções... 3 Módulo 3 Propriedades
1 a QUESTÃO Valor 1,0
 1 a QUESTÃO Valor 1,0 Um esquimó aguarda a passagem de um peixe sob um platô de gelo, como mostra a figura abaixo. Ao avistá-lo, ele dispara sua lança, que viaja com uma velocidade constante de 50 m/s,
1 a QUESTÃO Valor 1,0 Um esquimó aguarda a passagem de um peixe sob um platô de gelo, como mostra a figura abaixo. Ao avistá-lo, ele dispara sua lança, que viaja com uma velocidade constante de 50 m/s,
Separação de Misturas
 1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
1. Introdução Separação de Misturas As misturas são comuns em nosso dia a dia. Como exemplo temos: as bebidas, os combustíveis, e a própria terra em que pisamos. Poucos materiais são encontrados puros.
Programa de Retomada de Conteúdo 1º Bimestre
 Educação Infantil, Ensino Fundamental e Ensino Médio Regular. Rua Cantagalo 313, 325, 337 e339 Tatuapé Fones: 2293-9393 e 2293-9166 Diretoria de Ensino Região LESTE 5 Programa de Retomada de Conteúdo 1º
Educação Infantil, Ensino Fundamental e Ensino Médio Regular. Rua Cantagalo 313, 325, 337 e339 Tatuapé Fones: 2293-9393 e 2293-9166 Diretoria de Ensino Região LESTE 5 Programa de Retomada de Conteúdo 1º
De repente sua bateria LiPO fica grávida. O que fazer?
 De repente sua bateria LiPO fica grávida. O que fazer? Você sabia que denominamos bateria ao conjunto de pilhas associadas em série ou paralelo? Dessa forma, podemos dizer que bateria é o coletivo de pilhas,
De repente sua bateria LiPO fica grávida. O que fazer? Você sabia que denominamos bateria ao conjunto de pilhas associadas em série ou paralelo? Dessa forma, podemos dizer que bateria é o coletivo de pilhas,
Associação Catarinense das Fundações Educacionais ACAFE PARECER RECURSO DISCIPLINA QUÍMICA
 33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
Preparação de Soluções
 Colégio Paulo VI Preparação de Soluções TÉCNICAS LABORATORIAIS DE QUÍMICA I Ana Filipa Sousa nº2 10ºA Abril 2002 2 ÍNDICE Nomenclatura 4 1. Introdução x 2. Teoria e Método x 3. Material x 4. Produtos x
Colégio Paulo VI Preparação de Soluções TÉCNICAS LABORATORIAIS DE QUÍMICA I Ana Filipa Sousa nº2 10ºA Abril 2002 2 ÍNDICE Nomenclatura 4 1. Introdução x 2. Teoria e Método x 3. Material x 4. Produtos x
MATÉRIA- PROPRIEDADES DA MATÉRIA- SUBSTÂNICAS (Pura e Composta)- MISTURAS- ANÁLISE IMEDIATA.
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
LABORATÓRIO DE QUÍMICA ATIVIDADES LABORATORIAIS
 LABORATÓRIO DE QUÍMICA ATIVIDADES LABORATORIAIS EMENTA QUÍMICA APLICADA À ENGENHARIA Elementos químicos e as propriedades periódicas; ligações químicas; algumas funções orgânicas e inorgânicas; reações
LABORATÓRIO DE QUÍMICA ATIVIDADES LABORATORIAIS EMENTA QUÍMICA APLICADA À ENGENHARIA Elementos químicos e as propriedades periódicas; ligações químicas; algumas funções orgânicas e inorgânicas; reações
Ensaios Mecânicos de Materiais. Aula 12 Ensaio de Impacto. Prof. MSc. Luiz Eduardo Miranda J. Rodrigues
 Ensaios Mecânicos de Materiais Aula 12 Ensaio de Impacto Tópicos Abordados Nesta Aula Ensaio de Impacto. Propriedades Avaliadas do Ensaio. Tipos de Corpos de Prova. Definições O ensaio de impacto se caracteriza
Ensaios Mecânicos de Materiais Aula 12 Ensaio de Impacto Tópicos Abordados Nesta Aula Ensaio de Impacto. Propriedades Avaliadas do Ensaio. Tipos de Corpos de Prova. Definições O ensaio de impacto se caracteriza
EXERCÍCIOS ON LINE DE CIÊNCIAS - 9 ANO
 EXERCÍCIOS ON LINE DE CIÊNCIAS - 9 ANO 1- Com a finalidade de diminuir a dependência de energia elétrica fornecida pelas usinas hidroelétricas no Brasil, têm surgido experiências bem sucedidas no uso de
EXERCÍCIOS ON LINE DE CIÊNCIAS - 9 ANO 1- Com a finalidade de diminuir a dependência de energia elétrica fornecida pelas usinas hidroelétricas no Brasil, têm surgido experiências bem sucedidas no uso de
Noções de química. Conceitos Química molécula substância mistura solução diluição fórmula I NTROD U ÇÃO AO M Ó DULO DE S E RV I Ç O S GE R A I S
 I NTROD U ÇÃO AO M Ó DULO DE S E RV I Ç O S GE R A I S Noções de química Conceitos Química molécula substância mistura solução diluição fórmula ficha10_al_serv_gerais_educador_01a.indd 1 5/4/2011 16:11:32
I NTROD U ÇÃO AO M Ó DULO DE S E RV I Ç O S GE R A I S Noções de química Conceitos Química molécula substância mistura solução diluição fórmula ficha10_al_serv_gerais_educador_01a.indd 1 5/4/2011 16:11:32
Por exemplo a água salgada é uma substância ou uma mistura? A água salgada é uma mistura de duas substâncias: a água e o cloreto de sódio.
 Sumário Correção do TPC. Soluto, solvente e solução. Composição qualitativa e quantitativa de soluções concentração de uma solução. saturadas. Exercícios de aplicação. Ficha de Trabalho Soluto, solvente
Sumário Correção do TPC. Soluto, solvente e solução. Composição qualitativa e quantitativa de soluções concentração de uma solução. saturadas. Exercícios de aplicação. Ficha de Trabalho Soluto, solvente
