Efeito da Concentração do Cloreto de Sódio na Eclosão de Dáfnias
|
|
|
- Luzia Pacheco Andrade
- 6 Há anos
- Visualizações:
Transcrição
1 Efeito da Concentração do Cloreto de Sódio na Eclosão de Dáfnias Nuno Lapa e Rui Barbosa Universidade Nova de Lisboa (UNL) Faculdade de Ciências e Tecnologia (FCT) Unidade de Biotecnologia Ambiental (UBiA) Campus da Caparica, Ed. Departamental, piso 3, gab. 377-B, Caparica, Portugal 1. Objectivo O objectivo deste protocolo de trabalho é a determinação do efeito de diferentes concentrações de Cloreto de Sódio (NaCl) na eclosão do organismo Daphnia magna. Um conjunto de efípios de D. magna é exposto a concentrações crescentes de NaCl, durante 72 h, em condições controladas de luz e temperatura. Será registado o número de indivíduos que eclodiram e que apresentam mobilidade e o número de indivíduos que eclodiram mas que não apresentam mobilidade, após 72 h de incubação. Por comparação com o ensaio em que os efípios foram colocados em água com características padronizadas para a eclosão das dáfnias, determinar-se-ão as percentagens de redução no número de dáfnias eclodidas. 2. Materiais e Equipamentos 1) Dois tubos com efípios de dáfnias; 2) Um micro-crivo; 3) Dois tubos com Spirulina para alimentar as dáfnias; 4) Treze placas de Petri, de plástico, de 15 ml; 5) Seis balões volumétricos de 100 ml; 6) Cinco balões volumétricos de 1000 ml; 7) Bomba de arejamento de aquário; 8) Balanças para pesar reagentes sólidos (precisão: ±0,01 g); 9) Pipetas de vidro graduadas (5 ml, 10 ml, 25 ml, 50 ml); 10) Câmara de incubação com controlo de temperatura e iluminação; 11) Pinças ou espátulas; 12) Folha de cartolina preta; 13) Etiquetas para identificar os balões com as soluções que neles estão contidas. 3. Reagentes 1) Hidrogenocarbonato de sódio (NaHCO 3 ); 1
2 2) Cloreto de cálcio dihidratado (CaCl 2.2H 2 O); 3) Sulfato de magnésio heptahidratado (MgSO 4.7H 2 O); 4) Cloreto de potássio (KCl); 5) Cloreto de sódio (NaCl). É necessária, ainda, água desionizada. Se forem utilizados reagentes com outros níveis de hidratação, as preparações indicadas na Tarefa 4 (Dia 1) terão que ser corrigidas em conformidade. 4. Programa de Trabalho para o Dia 1 Tarefa 1 Apresentação dos docentes e dos estagiários Ciência Viva Tarefa 2 Apresentação do programa de trabalho Tarefa 3 Apresentação dos laboratórios onde o trabalho será realizado Tarefa 4 Preparação da solução de eclosão das dáfnias, designada por Água de Diluição A Água de Diluição é uma solução que contém um conjunto de sais essenciais à eclosão das dáfnias. Esta solução é composta por hidrogenocarbonato de sódio, cloreto de cálcio, sulfato de magnésio e cloreto de potássio. Devem ser preparadas quatro soluções individuais, contendo, cada uma delas, cada um destes sais. Estas quatro soluções são preparadas do seguinte modo: 1) Preparação das soluções individuais a. Solução de hidrogenocarbonato de sódio (NaHCO 3 ): Identificar um balão volumétrico de um litro com a indicação 2,59 g NaHCO 3 /L. Dissolver 2,59 g de NaHCO 3 em água desionizada e perfazer esta solução a um litro. Agitar esta solução (Solução 1); b. Solução de cloreto de cálcio dihidratado (CaCl 2.2H 2 O): Identificar um balão volumétrico de um litro com a indicação 11,76 g CaCl 2.2H 2 O/L. Dissolver 11,76 g de CaCl 2.2H 2 O em água desionizada e perfazer esta solução a um litro. Agitar esta solução (Solução 2); c. Solução de sulfato de magnésio heptahidratado (MgSO 4.7H 2 O): Identificar um balão volumétrico de um litro com a indicação 4,93 g MgSO 4.7H 2 O/L. Dissolver 4,93 g de MgSO 4.7H 2 O em água desionizada e perfazer esta solução a um litro. Agitar esta solução (Solução 3); d. Solução de cloreto de potássio (KCl): Identificar um balão volumétrico de um litro com a indicação 0,23 g KCl/L. Dissolver 0,23 g de KCl em água desionizada e perfazer esta solução a um litro. Agitar esta solução (Solução 4). 2
3 Após se ter preparado estas quatro soluções, deve ser preparada a Água de Diluição, do seguinte modo: 1) Identificar um balão volumétrico de um litro com a indicação Água de Diluição ; 2) Adicionar água desionizada ao balão volumétrico identificado em 1) até, cerca de, metade da sua capacidade. Adicionar 25 ml da Solução 1 a esse balão volumétrico e agitar de modo a dissolver esta solução; 3) Adicionar 25 ml da Solução 2 ao balão volumétrico e agitar de modo a dissolver esta solução; 4) Adicionar 25 ml da Solução 3 a esse balão volumétrico e agitar de modo a dissolver esta solução; 5) Adicionar 25 ml da Solução 4 a esse balão volumétrico e agitar de modo a dissolver esta solução; 6) Perfazer com água desionizada. Agitar esta solução. Tarefa 5 Arejamento da Água de Diluição A Água de Diluição deve ser arejada durante, pelo menos, 30 minutos, antes de ser colocada em contacto com os efípios. O arejamento pode ser efectuado através de uma bomba de arejamento de um aquário, à qual se encontra ligado um tubo de plástico. Na ponta do tubo de plástico deverá ser ligada uma pipeta. Esta deverá ser introduzida no balão que contém a Água de Diluição e a bomba de aquário deverá ser colocada em funcionamento, com um arejamento suficientemente forte, mas evitando que a água seja expelida para fora do balão. Tarefa 6 Conservação da Água de Diluição A Água de Diluição pode ser conservada num frigorífico, na ausência de luz. Nestas condições de conservação, esta solução mantém-se estável durante cerca de 3 a 4 dias. Sempre que a Água de Diluição for conservada no frio, ela deve ser retirada do frigorífico algumas horas antes do início do teste, de modo a garantir que a sua temperatura atinja, gradualmente, a temperatura ambiente. Tarefa 7 Preparação das soluções de NaCl Sugere-se a preparação, em balões de 100 ml, das concentrações de NaCl indicadas no Quadro 1. C0 (g NaCl/L) Quadro 1. Concentrações de NaCl que serão testadas C1 C2 C3 C4 (g NaCl/L) (g NaCl/L) (g NaCl/L) (g NaCl/L) C5 (g NaCl/L) 0 0,137 0,547 2,188 8,
4 Metodologia para a preparação das soluções da NaCl: 1. Identificar seis balões volumétricos, de 100 ml, com os códigos C0 a C5; 2. Perfazer o balão C0 com Água de Diluição até à marca de 100 ml; 3. Dissolver 3,5 g de NaCl com Água de Diluição no balão volumétrico C5. Perfazer com Água de Diluição a 100 ml. Agitar até se atingir a dissolução completa do NaCl; 4. Transferir 25 ml da solução do balão C5 para o balão volumétrico C4. Perfazer com Água de Diluição a 100 ml. Agitar; 5. Transferir 25 ml da solução do balão C4 para o balão volumétrico C3. Perfazer com Água de Diluição a 100 ml. Agitar; 6. Transferir 25 ml da solução do balão C3 para o balão volumétrico C2. Perfazer com Água de Diluição a 100 ml. Agitar; 7. Transferir 25 ml da solução do balão C2 para o balão volumétrico C1. Perfazer com Água de Diluição a 100 ml. Agitar. 5. Programa de Trabalho para o Dia 2 Tarefa 8 Preparação das placas de Petri destinadas à incubação dos efípios Identificar 12 placas de Petri, de plástico, de 15 ml, tal como indicado no Quadro 2. Quadro 2. Códigos que deverão ser atribuídos às placas de Petri onde os efípios serão incubados Ensaio Concentração de NaCl C0 C1 C2 C3 C4 C5 1 C0/1 C1/1 C2/1 C3/1 C4/1 C5/1 2 C0/2 C1/2 C2/2 C3/2 C4/2 C5/2 Transferir, dos balões volumétricos de 100 ml que contêm as soluções da NaCl com as concentrações C0 a C5, cerca de 15 ml para as respectivas placas de Petri, de acordo com as indicações do Quadro 3. Quadro 3. Volumes das soluções de NaCl (C0 a C5) que deverão ser colocados nas placas de Petri de incubação dos efípios (C0/1 a C5/2) Placa de Petri Solução de NaCl (balão volumétrico) Volume da solução de NaCl (ml) C0/1 C0 15 C0/2 C0 15 C1/1 C1 15 C1/2 C1 15 C2/1 C2 15 C2/2 C2 15 C3/1 C3 15 C3/2 C3 15 4
5 Quadro 3. (cont.) Placa de Petri Solução de NaCl (balão volumétrico) Volume da solução de NaCl (ml) C4/1 C4 15 C4/2 C4 15 C5/1 C5 15 C5/2 C5 15 Tarefa 9 Lavagem dos efípios A lavagem dos efípios deve realizar-se do seguinte modo: a) Colocar, no microcrivo, todo o conteúdo dos dois recipientes onde se encontram os efípios; b) Lavar os efípios com água da torneira, de modo a remover o meio de conservação. O caudal de água deve ser regulado, de modo a não serem expelidos efípios para fora do microcrivo; c) Identificar uma placa de Petri, de 15 ml, com a seguinte denominação Lavagem de Efípios; Data: DD/MM/AAAA; Hora: hh:min ; d) Transferir os efípios para a placa de lavagem, fazendo passar 15 ml de Água de Diluição, previamente arejada, pelo fundo do crivo, em sentido contrário ao que se fez passar a água da torneira. O objectivo é o de libertar os efípios na placa de lavagem, com o auxílio da água de diluição. Tarefa 10 Transferência dos efípios para as placas de Petri que contém as soluções de NaCl Com o auxílio de uma espátula ou de uma pinça, transferir cinco efípios para cada uma das placas de Petri (C0/1 a C5/2) que contêm as soluções de NaCl. Deverá evitar-se a transferência de uma grande quantidade de água do meio onde os efípios foram lavados. Tarefa 11 Incubação dos efípios Efectuar a incubação dos efípios do seguinte modo: a) Tapar as doze placas de Petri com as tampas; b) Incubar, durante 72 h, entre 20 e 22ºC, sob luz contínua, numa câmara de incubação. Os primeiros efípios deverão nascer um pouco antes das 72 h de incubação. A maioria deles nascerá entre as 72 e as 80h. Tarefa 12 Pesquisa bibliográfica Iniciar uma pesquisa bibliográfica sobre Que organismos são as dáfnias, qual é o seu ciclo de vida e como é que o NaCl as afecta. 5
6 Esta pesquisa deverá permitir que os estagiários preparem a Introdução para o trabalho. 6. Programa de Trabalho para o Dia 3 Tarefa 13 Pesquisa bibliográfica Continuar a pesquisa bibliográfica sobre Que organismos são as dáfnias, qual é o seu ciclo de vida e como é que o NaCl as afecta. Tarefa 14 Discussão sobre a informação recolhida na pesquisa bibliográfica Os estagiários deverão reunir-se para darem a conhecer, uns aos outros, quais foram os resultados das suas pesquisas bibliográficas. Devem trocar a informação obtida e todos devem ler a informação que os colegas lhes forneceram. 7. Programa de Trabalho para o Dia 4 Tarefa 15 Preparação de slides para uma apresentação oral do trabalho realizado no estágio Os estagiários deverão dar início à preparação de slides que irão suportar uma apresentação oral (em grupo) do trabalho realizado no estágio e dos resultados obtidos. A apresentação deverá ser, no máximo, de 20 minutos e deverá incluir os seguintes aspectos: a) Introdução ao tema estudado; b) Material utilizado; c) Procedimento experimental; d) Resultados obtidos; e) Conclusões; f) Propostas para trabalhos futuros; g) Bibliografia. 8. Programa de Trabalho para o Dia 5 Tarefa 16 Leitura e registo do número de dáfnias eclodidas 72 h após o início da incubação dos efípios, deve proceder-se à leitura e registo, em cada uma das placas de Petri, da seguinte informação: 6
7 a) Número de dáfnias com mobilidade (Dm); b) Número de dáfnias sem mobilidade (Dim). A soma de Dm com Dim dará o número total de dáfnias que eclodiram. Dim representará as dáfnias que eclodiram, mas que foram afectadas pela concentração de NaCl no meio de cultura. A contagem das dáfnias móveis e imóveis, em cada uma das placas de Petri, será facilitada se se colocar uma folha de cartolina preta debaixo das placas. O registo dos números de dáfnias móveis e imóveis poderá ser feito num quadro semelhante ao Quadro 4. Quadro 4. Exemplo de um quadro de registo de resultados Placa de Petri Nº de dáfnias móveis Nº de dáfnias imóveis C0/1 C0/2 C1/1 C1/2 C2/1 C2/2 C3/1 C3/2 C4/1 C4/2 C5/1 C5/2 Tarefa 17 Tratamento dos resultados Os estagiários deverão proceder ao tratamento dos resultados obtidos, preferencialmente numa folha de cálculo (por exemplo, Microsoft Excel). Deverão incluir: a) O cálculo do número total de dáfnias eclodidas para cada concentração de NaCl; b) O cálculo da percentagem de dáfnias não eclodidas (percentagem de efeito do NaCl na eclosão de dáfnias); c) O cálculo da percentagem de dáfnias eclodidas, mas que não apresentam mobilidade (percentagem de efeito do NaCl na mobilidade das dáfnias juvenis); d) Qualquer outro cálculo que julguem ser pertinente. Os resultados deverão ser apresentados preferencialmente sob a forma de gráficos, que demonstrem a relação entre as concentrações de NaCl testadas e as percentagens de efeito do sal na eclosão e na mobilidade das dáfnias. Continuação da Tarefa 15 Preparação de slides para uma apresentação oral do trabalho realizado no estágio 7
8 Após o tratamento dos resultados estar completo, os estagiários deverão continuar a preparar os slides para a apresentação oral. 9. Programa de Trabalho para o Dia 6 Conclusão da Tarefa 15 Preparação de slides para uma apresentação oral do trabalho realizado no estágio Os estagiários deverão concluir a preparação dos slides para a apresentação oral. 10. Programa de Trabalho para o Dia 7 Tarefa 18 Apresentação oral do trabalho realizado e dos resultados obtidos No último dia do estágio, os estagiários irão efectuar a apresentação oral do trabalho realizado e dos resultados obtidos. Tal como foi indicado na Tarefa 15, a apresentação oral deve ser apoiada nos slides que foram preparados pelos estagiários, devendo incluir os pontos que se encontram indicados na Tarefa 15 (Programa de Trabalho para o Dia 4). A apresentação oral não deverá exceder 20 minutos. Tratando-se de uma apresentação em grupo, todos os estagiários deverão comunicar uma parte da apresentação oral, isto é, todos devem falar durante a apresentação oral. Após a apresentação, os orientadores do estágio têm disponível um período de 10 minutos para a colocação de questões/comentários/sugestões. Tarefa 19 Entrega dos Diplomas de Realização de Estágio Ciência Viva No final da apresentação oral, o investigador responsável pelos estágios procederá à entrega dos Diplomas de Realização de Estágio Ciência Viva. Tarefa 20 Resposta aos inquéritos Ciência Viva Os estagiários e o investigador responsável pelos estágios deverão responder ao inquérito Ciência Viva sobre a qualidade do estágio. Com esta tarefa, o estágio encontra-se concluído. 8
Bioadsorção com serradura de pinheiro de poluentes presentes em águas
 Bioadsorção com serradura de pinheiro de poluentes presentes em águas Coordenador do estágio: Professor Nuno Lapa Colaboração: Aluna de doutoramento Maria Bernardo Instituição de acolhimento: Universidade
Bioadsorção com serradura de pinheiro de poluentes presentes em águas Coordenador do estágio: Professor Nuno Lapa Colaboração: Aluna de doutoramento Maria Bernardo Instituição de acolhimento: Universidade
Actividade nº 2. Actividade laboratorial: Preparação de soluções e sua diluição
 Escola Básica e Secundária Gonçalves Zarco Física e Química A, 10º ano Ano lectivo 2008/2009 Actividade nº 2 Protocolo Experimental Data: 9/10/2008 Duração: 135 min Actividade laboratorial: Preparação
Escola Básica e Secundária Gonçalves Zarco Física e Química A, 10º ano Ano lectivo 2008/2009 Actividade nº 2 Protocolo Experimental Data: 9/10/2008 Duração: 135 min Actividade laboratorial: Preparação
Preparação e padronização de soluções
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático nº 2 Preparação e padronização de soluções
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático nº 2 Preparação e padronização de soluções
Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações.
 EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
EXPERIMENTO 2 Preparação e Padronização de Soluções OBJETIVOS Rever os conceitos de concentração de soluções. Aprender a preparar soluções aquosas, realizar diluições e determinar suas concentrações. Exercitar
SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS
 EXPERIMENTO 4 SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS OBJETIVOS Observar soluções insaturadas, saturadas e supersaturadas; Construir a curva de solubilidade de um sal inorgânico. INTRODUÇÃO Os depósitos naturais
EXPERIMENTO 4 SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS OBJETIVOS Observar soluções insaturadas, saturadas e supersaturadas; Construir a curva de solubilidade de um sal inorgânico. INTRODUÇÃO Os depósitos naturais
Agrupamento de Escolas de Bobadela Escola EBI de Bobadela. Preparação de soluções aquosas de sulfato de cobre
 Agrupamento de Escolas de Bobadela Escola EBI de Bobadela Ano letivo 2013/2014 C. Físico-Químicas 7º ano Relatório da actividade experimental: Preparação de soluções aquosas de sulfato de cobre Elaborado
Agrupamento de Escolas de Bobadela Escola EBI de Bobadela Ano letivo 2013/2014 C. Físico-Químicas 7º ano Relatório da actividade experimental: Preparação de soluções aquosas de sulfato de cobre Elaborado
Síntese do acetato de n-butilo ou etanoato de n-butilo
 Síntese do acetato de n-butilo ou etanoato de n-butilo Realização experimental a microescala (baseado no protocolo de Williamson 1 ) A reacção entre o butan-1-ol e o ácido acético glacial (ou ácido etanoico)
Síntese do acetato de n-butilo ou etanoato de n-butilo Realização experimental a microescala (baseado no protocolo de Williamson 1 ) A reacção entre o butan-1-ol e o ácido acético glacial (ou ácido etanoico)
Titulação de cálcio e magnésio no leite com EDTA. Ilustrar: Titulação por retorno Titulação complexométrica, com EDTA
 TRABALHO PRÁTICO Titulação de cálcio e magnésio no leite com Ilustrar: Titulação por retorno Titulação complexométrica, com PARTE EXPERIMENTAL Procedimento para determinação do teor de cálcio mais magnésio
TRABALHO PRÁTICO Titulação de cálcio e magnésio no leite com Ilustrar: Titulação por retorno Titulação complexométrica, com PARTE EXPERIMENTAL Procedimento para determinação do teor de cálcio mais magnésio
Alexandra Silva Fernandes
 Alexandra Silva Fernandes APL 2.1. 1ª parte Soluções como se preparam? Problema: Como preparar 50,0 cm 3 de um solução aquosa de tiossulfato de sódio 0,030 mol.dm 3? Como preparar uma solução, a partir
Alexandra Silva Fernandes APL 2.1. 1ª parte Soluções como se preparam? Problema: Como preparar 50,0 cm 3 de um solução aquosa de tiossulfato de sódio 0,030 mol.dm 3? Como preparar uma solução, a partir
MF-0407.R-2 - MÉTODO DE DETERMINAÇÃO DE COLÔNIAS DE BACTÉRIAS QUE PRECIPITAM O FERRO (FERROBACTÉRIAS), PELA TÉCNICA "POUR PLATE"
 MF-0407.R-2 - MÉTODO DE DETERMINAÇÃO DE COLÔNIAS DE BACTÉRIAS QUE PRECIPITAM O FERRO (FERROBACTÉRIAS), PELA TÉCNICA "POUR PLATE" Notas: Aprovado pela Deliberação CECA n 3.966, de 16 de janeiro de 2001
MF-0407.R-2 - MÉTODO DE DETERMINAÇÃO DE COLÔNIAS DE BACTÉRIAS QUE PRECIPITAM O FERRO (FERROBACTÉRIAS), PELA TÉCNICA "POUR PLATE" Notas: Aprovado pela Deliberação CECA n 3.966, de 16 de janeiro de 2001
AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta
 3 AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta REAGENTES: Solução de permanganato de potássio 0,02 mol L -1,
3 AULA PRÁTICA N 15: DETERMINAÇÃO DE PERÓXIDO DE HIDROGÊNIO NA ÁGUA OXIGENADA Volumetria de oxirredução permanganimetria volumetria direta REAGENTES: Solução de permanganato de potássio 0,02 mol L -1,
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO. Ano de Escolaridade : 11
 Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.5 Solubilidade: solutos e solventes Apesar da água
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.5 Solubilidade: solutos e solventes Apesar da água
SUBSTÂNCIAS E MISTURAS
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
E SE UM BLOOM DE CIANOBACTÉRIAS TE BATESSE À PORTA?
 E SE UM BLOOM DE CIANOBACTÉRIAS TE BATESSE À PORTA? Com a colaboração de: Piedade Barros Maria do Rosário Martins Escola Superior Tecnologias da Saúde do Porto - Porto TRABALHOS Efectuar uma cultura laboratorial
E SE UM BLOOM DE CIANOBACTÉRIAS TE BATESSE À PORTA? Com a colaboração de: Piedade Barros Maria do Rosário Martins Escola Superior Tecnologias da Saúde do Porto - Porto TRABALHOS Efectuar uma cultura laboratorial
Determinação da densidade relativa das soluções de sacarose e dos açucares a estudar
 Determinação da densidade relativa das soluções de sacarose e dos açucares a estudar 1. Densidade relativa A densidade relativa é uma propriedade física característica de cada substância e a sua determinação
Determinação da densidade relativa das soluções de sacarose e dos açucares a estudar 1. Densidade relativa A densidade relativa é uma propriedade física característica de cada substância e a sua determinação
Dureza da Água e Problemas de Lavagem
 Dureza da Água e Problemas de Lavagem O que se pretende Classificar uma água quanto à sua dureza, como dura ou macia, a partir do seu comportamento em testes de lavagem. Para além disso, e a partir das
Dureza da Água e Problemas de Lavagem O que se pretende Classificar uma água quanto à sua dureza, como dura ou macia, a partir do seu comportamento em testes de lavagem. Para além disso, e a partir das
Protocolo experimental
 Protocolo experimental As Artémias também precisam de higiene diária? Enquadramento Teórico Ao longo dos tempos, a contaminação química de origem antropogénica tem vindo sucessivamente a aumentar nos ecossistemas
Protocolo experimental As Artémias também precisam de higiene diária? Enquadramento Teórico Ao longo dos tempos, a contaminação química de origem antropogénica tem vindo sucessivamente a aumentar nos ecossistemas
I) Comparação da precisão em medidas volumétricas
 EXPERIMENTO 1 PROCEDIMENTOS DE LABORATÓRIO MEDIDAS DE MASSA, VOLUME E TEMPERATURA I) Comparação da precisão em medidas volumétricas Procedimento Experimental Materiais necessários: bureta de 50 ml (1);
EXPERIMENTO 1 PROCEDIMENTOS DE LABORATÓRIO MEDIDAS DE MASSA, VOLUME E TEMPERATURA I) Comparação da precisão em medidas volumétricas Procedimento Experimental Materiais necessários: bureta de 50 ml (1);
Qual a quantidade de halogenetos que existe na água do mar?
 20 Qual a quantidade de halogenetos que existe na água do mar? E20-1 o que necessitas cloreto de sódio sólido com grau de pureza analítico cromato de potássio sólido um balão de diluição de 100 ml dois
20 Qual a quantidade de halogenetos que existe na água do mar? E20-1 o que necessitas cloreto de sódio sólido com grau de pureza analítico cromato de potássio sólido um balão de diluição de 100 ml dois
Determinação da Entalpia de uma Reacção
 INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
INSTITUTO POLITÉCNICO DE TOMAR ESCOLA SUPERIOR DE TECNOLOGIA Departamento de Engenharia Química e do Ambiente QUÍMICA I (1º Ano 1º Semestre) Trabalho Prático n.º 6 Determinação da Entalpia de uma Reacção
Protocolo experimental
 Protocolo experimental E se a salinidade se alterar? Enquadramento Teórico Todos os animais necessitam de condições ambientais favoráveis à sua sobrevivência e manutenção. Parâmetros como por exemplo a
Protocolo experimental E se a salinidade se alterar? Enquadramento Teórico Todos os animais necessitam de condições ambientais favoráveis à sua sobrevivência e manutenção. Parâmetros como por exemplo a
R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L
 1 R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L ACTIVIDADE LABORATORIAL 1.3 Efeitos da temperatura e da concentração na progressão global de uma reacção de equilíbrio com iões de cobalto
1 R E L A T Ó R I O D A A C T I V I D A D E L A B O R A T O R I A L ACTIVIDADE LABORATORIAL 1.3 Efeitos da temperatura e da concentração na progressão global de uma reacção de equilíbrio com iões de cobalto
Reconhecer as vidrarias volumétricas utilizadas no preparo de soluções;
 AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
BIOENSAIOS COM ORGANISMOS AQUÁTICOS... Ecotoxicologia Ana Morbey - 16/06/04 Instituto do Ambiente
 Bioensaios COM ORGANISMOS AQUÁTICOS... 2 ORGANISMOS-TESTE Vibrio fischeri (bactéria) Daphnia magna (microcrustáceo) Thamnocephalus platyurus (microcrustáceo) Artemia franciscana (no caso de amostras salinas)
Bioensaios COM ORGANISMOS AQUÁTICOS... 2 ORGANISMOS-TESTE Vibrio fischeri (bactéria) Daphnia magna (microcrustáceo) Thamnocephalus platyurus (microcrustáceo) Artemia franciscana (no caso de amostras salinas)
MF-459.R-1 - MÉTODO DE DETERMINAÇÃO DO EFEITO AGUDO LETAL CAUSADO POR EFLUENTES LÍQUIDOS EM CRUSTÁCEOS DA ESPÉCIE ARTEMIA SALINA MÉTODO ESTÁTICO
 MF-459.R-1 - MÉTODO DE DETERMINAÇÃO DO EFEITO AGUDO LETAL CAUSADO POR EFLUENTES LÍQUIDOS EM CRUSTÁCEOS DA ESPÉCIE ARTEMIA SALINA MÉTODO ESTÁTICO Notas: Aprovada pela Deliberação CECA nº 3.480, de 25 de
MF-459.R-1 - MÉTODO DE DETERMINAÇÃO DO EFEITO AGUDO LETAL CAUSADO POR EFLUENTES LÍQUIDOS EM CRUSTÁCEOS DA ESPÉCIE ARTEMIA SALINA MÉTODO ESTÁTICO Notas: Aprovada pela Deliberação CECA nº 3.480, de 25 de
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA
 Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
Experiência 7. PREPARO DE SOLUÇÃO A PARTIR DE SUBSTÂNCIAS SÓLIDAS, LIQUIDAS E DE SOLUÇÃO CONCENTRADA 1. Objetivos Após a realização desta aula experimental, espera-se que o graduando do curso de Química
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:3º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:3º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE. Versão professor. Algumas notas prévias
 ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão professor O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
Física e Química A. Nomes: N.º s : T.ª: Como neutralizar resíduos de ácidos/bases do laboratório de Química da escola?
 Física e Química A 11ºAno - Química AL.2.3. Neutralização: uma reacção de ácido-base Ano lectivo: 2010/2011 Nomes: N.º s : T.ª: PARTE I - Introdução Questão problema Como identificar se os resíduos são
Física e Química A 11ºAno - Química AL.2.3. Neutralização: uma reacção de ácido-base Ano lectivo: 2010/2011 Nomes: N.º s : T.ª: PARTE I - Introdução Questão problema Como identificar se os resíduos são
ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO
 ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO DETERMINAR O PONTO DE SOLIDIFICAÇÃO DA ÁGUA DESTILADA. DETERMINAR O PONTO DE FUSÃO DA ÁGUA DESTILADA. VERIFICAR QUE UMA SOLUÇÃO AQUOSA DE CLORETO
ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO DETERMINAR O PONTO DE SOLIDIFICAÇÃO DA ÁGUA DESTILADA. DETERMINAR O PONTO DE FUSÃO DA ÁGUA DESTILADA. VERIFICAR QUE UMA SOLUÇÃO AQUOSA DE CLORETO
MATERIAIS PARA FUNDIÇÃO - DETERMINAÇÃO DO FATOR DA SOLUÇÃO DE AZUL DE METILENO POR TITULAÇÃO COM SOLUÇÃO DE CLORETO TITANOSO (TiCl 3 )
 Padronização Folha : 1 de 6 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Aparelhagem 4_ Procedimento 1_ OBJETIVO 1.1_ Esta recomendação prescreve o método de fatoração da solução de azul de metileno utilizada
Padronização Folha : 1 de 6 SUMÁRIO 1_ Objetivo 2_ Princípio do método 3_ Aparelhagem 4_ Procedimento 1_ OBJETIVO 1.1_ Esta recomendação prescreve o método de fatoração da solução de azul de metileno utilizada
Detecção de IL-1 por ELISA sanduíche. Andréa Calado
 Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Detecção de IL-1 por ELISA sanduíche Andréa Calado andreabelfort@hotmail.com ELISA O teste identifica e quantifica Ag ou Ac, utilizando um dos dois conjugados com enzimas; PRINCIPAIS TIPOS: INDIRETO:
Síntese do acetato de n-butilo ou etanoato de n-butilo
 Projeto Ciência Viva INTRODUÇÃO À QUÍMICA VERDE, COMO SUPORTE DA SUSTENTABILIDADE, NO ENSINO SECUNDÁRIO PL 3.4 Identificação e síntese de substâncias com aromas e sabores especiais Síntese do acetato de
Projeto Ciência Viva INTRODUÇÃO À QUÍMICA VERDE, COMO SUPORTE DA SUSTENTABILIDADE, NO ENSINO SECUNDÁRIO PL 3.4 Identificação e síntese de substâncias com aromas e sabores especiais Síntese do acetato de
LABORATÓRIO DE QUÍMICA QUI126 1ª LISTA DE EXERCÍCIOS
 1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
1. Soluções básicas servem para a dissolução de gorduras sólidas que obstruem tubulações das cozinhas. O hidróxido de sódio é um exemplo, pois reage com gorduras e gera produtos solúveis. Qual a massa
MÉTODO DE ANÁLISE LL-HARDWALL F. Determinação Potenciométrica de F -
 Determinação Potenciométrica de F - Comentários: O LL - Hardwall F contém 7,5% de F -, isto é, adicionando-se 1 g/lt aumenta-se o F - contido no tanque em cerca de 75 ppm Quando o equipamento Dosing Cad
Determinação Potenciométrica de F - Comentários: O LL - Hardwall F contém 7,5% de F -, isto é, adicionando-se 1 g/lt aumenta-se o F - contido no tanque em cerca de 75 ppm Quando o equipamento Dosing Cad
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE
 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO BASE O que se pretende Determinar a concentração desconhecida de uma solução aquosa de um ácido forte por titulação com uma base forte através de dois métodos. Num dos
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR
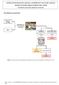 EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
Nesta actividade laboratorial não existe nenhum factor que leve a alguma
 REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o carbonato de cálcio do giz e o ácido acético do vinagre medindo o tempo de formação de um determinado volume de gás dióxido
REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre o carbonato de cálcio do giz e o ácido acético do vinagre medindo o tempo de formação de um determinado volume de gás dióxido
APARELHAGEM DE LABORATÓRIO 1. BICO DE BÜNSEN
 APARELHAGEM DE LABORATÓRIO 1. BICO DE BÜNSEN Aparelho ligado ao gás, utilizado para aquecimento de materiais não inflamáveis. Possui em sua base um regulador de entrada de ar para controlar o tipo de chama:
APARELHAGEM DE LABORATÓRIO 1. BICO DE BÜNSEN Aparelho ligado ao gás, utilizado para aquecimento de materiais não inflamáveis. Possui em sua base um regulador de entrada de ar para controlar o tipo de chama:
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO. Ano de Escolaridade : 11
 Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.2 Chuva normal e chuva ácida A classificação em chuva
Escola Secundária / 3º CEB da Batalha ACTIVIDADE LABORATORIAL DE FÍSICA E QUÍMICA A FORMAÇÃO ESPECÍFICA ENSINO SECUNDÁRIO Ano de Escolaridade : 11 AL 2.2 Chuva normal e chuva ácida A classificação em chuva
RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D
 RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D QUESTÃO 27 O técnico do laboratório pesou uma pequena barra de alumínio em uma balança cuja incerteza é ± 0,1 g e o valor obtido
RESPOSTAS AOS RECURSOS AO CARGO DE TÉCNICO DE LABORATÓRIO Área: QUÍMICA D QUESTÃO 27 O técnico do laboratório pesou uma pequena barra de alumínio em uma balança cuja incerteza é ± 0,1 g e o valor obtido
QUÍMICA 12º ANO ACTIVIDADE DE PROJECTO CONSTRUÇÃO DE UMA PILHA PROPOSTA DA METODOLOGIA 2010/ º Período
 QUÍMICA 12º ANO ACTIVIDADE DE PROJECTO CONSTRUÇÃO DE UMA PILHA PROPOSTA DA METODOLOGIA Henrique Fernandes, número 9 Ricardo Cunha, número 20 Jéssica Lopes, número 26 Professor Ângelo Fernandes Turma B
QUÍMICA 12º ANO ACTIVIDADE DE PROJECTO CONSTRUÇÃO DE UMA PILHA PROPOSTA DA METODOLOGIA Henrique Fernandes, número 9 Ricardo Cunha, número 20 Jéssica Lopes, número 26 Professor Ângelo Fernandes Turma B
ACÇÃO DE FORMAÇÃO GUIÃO DE ACTIVIDADE PRÁTICA. (Versão Professor)
 Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
Microbiologia alimentar Medronho. Maria João de Almeida Pessoa Trigo. Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014
 Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO
 MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO Notas: Revisão aprovada pela Deliberação CECA nº 0102, de 04 de setembro de 1980. Publicada no DOERJ de 18 de setembro de 1980. 1. OBJETIVO
MF-431.R-1 - MÉTODO TURBIDIMÉTRICO PARA DETERMINAÇÃO DE SULFATO Notas: Revisão aprovada pela Deliberação CECA nº 0102, de 04 de setembro de 1980. Publicada no DOERJ de 18 de setembro de 1980. 1. OBJETIVO
Estudo Estudo da Química
 Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
Estudo Estudo da Química Prof. Railander Borges Fale com o Professor: Email: rayllander.silva.borges@gmail.com Instagram: @rayllanderborges Facebook: Raylander Borges Aula 16 CONCENTRAÇÃO DE SOLUÇÕES 1.
RESINA FENÓLICA PARA FUNDIÇÃO - DETERMINAÇÃO DO TEOR DE FENOL LIVRE
 SUMÁRIO Método de Ensaio Folha : 1 de 5 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Resultados 7_ Anexo A 1_ OBJETIVO 1.1_ Esta recomendação prescreve
SUMÁRIO Método de Ensaio Folha : 1 de 5 1_ Objetivo 2_ Princípio do método 3_ Definição 4_ Aparelhagem / reagentes 5_ Execução do ensaio 6_ Resultados 7_ Anexo A 1_ OBJETIVO 1.1_ Esta recomendação prescreve
02/05/2016. Normas de laboratório INTRODUÇÃO INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE SEGURANÇA NO LABORATÓRIO:
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE Disciplina: Análise de Alimentos Normas de laboratório INTRODUÇÃO Acidente de trabalho é todo evento: inesperado e indesejável que
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA RIO GRANDE DO NORTE Disciplina: Análise de Alimentos Normas de laboratório INTRODUÇÃO Acidente de trabalho é todo evento: inesperado e indesejável que
1 Extração Líquido-Líquido
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
Ministério da Educação Universidade Federal do Paraná Setor Palotina. Soluções e cálculos de soluções
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula Soluções e cálculos de soluções Prof. Isac G. Rosset Isac G. Rosset -UFPR Mistura vs Composto Mistura Os componentes podem ser
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula Soluções e cálculos de soluções Prof. Isac G. Rosset Isac G. Rosset -UFPR Mistura vs Composto Mistura Os componentes podem ser
Efeito da toxicidade do NaCl na mobilidade do microcrustáceo Daphnia magna
 Efeito da toxicidade do NaCl na mobilidade do microcrustáceo Daphnia magna Inês Dias e Vasco Melro Laboratório de Ecotoxicologia, do Grupo de Disciplinas de Ecologia da Hidrosfera, da Faculdade de Ciências
Efeito da toxicidade do NaCl na mobilidade do microcrustáceo Daphnia magna Inês Dias e Vasco Melro Laboratório de Ecotoxicologia, do Grupo de Disciplinas de Ecologia da Hidrosfera, da Faculdade de Ciências
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata)
 Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE
 ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
TITULAÇÃO ÁCIDO-BASE
 ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases no laboratório. Realizar tecnicamente uma titulação. Seleccionar
Solução aquosa de tiossulfato de sódio 0,100 moldm. Ácido clorídrico concentrado: R: ; S: /37/ Realizar na hotte. Usar luvas.
 REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre ácido clorídrico e o tiossulfato de sódio a diferentes concentrações, através do tempo que demora a formar-se uma determinada
REALIZAÇÃO EXPERIMENTAL Objectivos Avaliar a velocidade da reacção química entre ácido clorídrico e o tiossulfato de sódio a diferentes concentrações, através do tempo que demora a formar-se uma determinada
Análise Volumétrica (Titrimétrica)
 7 (Titrimétrica) Material de Laboratório a) Material Individual (kit): localizado no armário identificado com um número. 1 bureta 25mL 1 proveta 100mL 1 becker 100 ml 1 pipeta volumétrica 10 ml 1 pipeta
7 (Titrimétrica) Material de Laboratório a) Material Individual (kit): localizado no armário identificado com um número. 1 bureta 25mL 1 proveta 100mL 1 becker 100 ml 1 pipeta volumétrica 10 ml 1 pipeta
Cinco gobelés de 50 ml Quatro tubos de ensaio Suporte para tubos de ensaio Cinco conta-gotas Pipeta de transferência Material.
 REALIZAÇÃO EXPERIMENTAL Objectivo Reconhecer que existem reacções químicas incompletas, reversíveis, ou seja, que podem ocorrer nos dois sentidos da reacção (o directo e o inverso). Duração Tempo de realização
REALIZAÇÃO EXPERIMENTAL Objectivo Reconhecer que existem reacções químicas incompletas, reversíveis, ou seja, que podem ocorrer nos dois sentidos da reacção (o directo e o inverso). Duração Tempo de realização
APÊNDICE A - Calibração do Forno de Redução
 APÊNDICE A - Calibração do Forno de Redução A calibração do forno de redução Combustol para o conhecimento da temperatura real em seu centro, foi realizada com base num indicador digital de temperatura,
APÊNDICE A - Calibração do Forno de Redução A calibração do forno de redução Combustol para o conhecimento da temperatura real em seu centro, foi realizada com base num indicador digital de temperatura,
ANÁLISE GRANULOMÉTRICA (Dispersão Total)
 12 ANÁLISE GRANULOMÉTRICA (Dispersão Total) 12.1 Método do densímetro 12.2.1 Princípio Baseia-se na sedimentação das partículas que compõem o solo. Após a adição de um dispersante químico, fixa-se um tempo
12 ANÁLISE GRANULOMÉTRICA (Dispersão Total) 12.1 Método do densímetro 12.2.1 Princípio Baseia-se na sedimentação das partículas que compõem o solo. Após a adição de um dispersante químico, fixa-se um tempo
Concentração de soluções e diluição
 Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
mol / kg de água do mar NaCl 0,4186 MgCl 2 0,0596 Na 2 SO 4 0,02856
 QUESTÕES DE EXAME 5 Física e Química A Questões de provas nacionais realizadas entre 2008 e 2014 organizados por subdomínio e por secção, por ordem cronológica. Os itens estão identificados por data e
QUESTÕES DE EXAME 5 Física e Química A Questões de provas nacionais realizadas entre 2008 e 2014 organizados por subdomínio e por secção, por ordem cronológica. Os itens estão identificados por data e
Reacções de precipitação
 Escola Básica do 2º e 3º ciclo de Santo António Ciências Físico-Química Ano lectivo: 2010/2011 Reacções de precipitação Docente: Eugénia Temtem Relatório elaborado por: Antonela Pereira nº1 Funchal, 28
Escola Básica do 2º e 3º ciclo de Santo António Ciências Físico-Química Ano lectivo: 2010/2011 Reacções de precipitação Docente: Eugénia Temtem Relatório elaborado por: Antonela Pereira nº1 Funchal, 28
AL º ano Separar e purificar. Destilação de uma solução de acetona (propanona) em água
 Projeto Ciência Viva INTRODUÇÃO À QUÍMICA VERDE, COMO SUPORTE DA SUSTENTABILIDADE, NO ENSINO SECUNDÁRIO AL 0.1 10º ano Separar e purificar Destilação de uma solução de acetona (propanona) em água 1. REAGENTES
Projeto Ciência Viva INTRODUÇÃO À QUÍMICA VERDE, COMO SUPORTE DA SUSTENTABILIDADE, NO ENSINO SECUNDÁRIO AL 0.1 10º ano Separar e purificar Destilação de uma solução de acetona (propanona) em água 1. REAGENTES
Bolsistas do subprojeto de Química: Ana Claudia Liz Mariela Matheus Marques Nayara Mendes Gabriela Camila Zanetti
 Bolsistas do subprojeto de Química: Ana Claudia Liz Mariela Matheus Marques Nayara Mendes Gabriela Camila Zanetti Alguns equipamentos e vidrarias comumente utilizados em laboratórios de Química e necessários
Bolsistas do subprojeto de Química: Ana Claudia Liz Mariela Matheus Marques Nayara Mendes Gabriela Camila Zanetti Alguns equipamentos e vidrarias comumente utilizados em laboratórios de Química e necessários
Química. APL 1.6 Funcionamento de um sistema-tampão: titulação ácido forte-base fraca (HCl e Na 2 CO 3 )
 Química APL 1.6 Funcionamento de um sistema-tampão: titulação ácido forte-base fraca (HCl e Na 2 CO 3 ) Luísa Neves, 12ºCT 09 de março de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento..4
Química APL 1.6 Funcionamento de um sistema-tampão: titulação ácido forte-base fraca (HCl e Na 2 CO 3 ) Luísa Neves, 12ºCT 09 de março de 2015 Índice Introdução...2 Material e Reagentes...3 Procedimento..4
Trabalho Prático nº 3. Metais, cor de chamas e solubilidade de sais
 Trabalho Prático nº 3 Metais, cor de chamas e solubilidade de sais 1. Introdução A cor de uma chama é afectada pela presença de um metal, uma vez que o átomo metálico é excitado, e essa cor é característica
Trabalho Prático nº 3 Metais, cor de chamas e solubilidade de sais 1. Introdução A cor de uma chama é afectada pela presença de um metal, uma vez que o átomo metálico é excitado, e essa cor é característica
O LABORATÓRIO DE MICROBIOLOGIA
 O LABORATÓRIO DE MICROBIOLOGIA Instalações Sala de manipulações cores claras, iluminação natural (preferencialmente) s/ correntes de ar. Superfícies de trabalho revestidas por materiais lisos, resistentes,
O LABORATÓRIO DE MICROBIOLOGIA Instalações Sala de manipulações cores claras, iluminação natural (preferencialmente) s/ correntes de ar. Superfícies de trabalho revestidas por materiais lisos, resistentes,
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Classificação das Soluções Aquosas e Coeficiente de Solubilidade
 Classificação das Soluções Aquosas e Coeficiente de Solubilidade 1. (UERJ) O gráfico a seguir, que mostra a variação da solubilidade do dicromato de potássio na água em função da temperatura, foi apresentado
Classificação das Soluções Aquosas e Coeficiente de Solubilidade 1. (UERJ) O gráfico a seguir, que mostra a variação da solubilidade do dicromato de potássio na água em função da temperatura, foi apresentado
Preparo de Reagentes (Soluções)
 Preparo de Reagentes (Soluções) Definições Solução: É uma mistura homogênea composta de dois ou mais componentes que consiste de: Solvente: É o componente da solução que se apresenta em maior quantidade.
Preparo de Reagentes (Soluções) Definições Solução: É uma mistura homogênea composta de dois ou mais componentes que consiste de: Solvente: É o componente da solução que se apresenta em maior quantidade.
MF-420.R-3 - MÉTODO DE DETERMINAÇÃO DE AMÔNIA (MÉTODO DO INDOFENOL).
 MF-420.R-3 - MÉTODO DE DETERMINAÇÃO DE AMÔNIA (MÉTODO DO INDOFENOL). Notas: Aprovada pela Deliberação CECA nº 686, de 25 de julho de 1985. Publicada no DOERJ de 14 de julho de 1985. 1. OBJETIVO O objetivo
MF-420.R-3 - MÉTODO DE DETERMINAÇÃO DE AMÔNIA (MÉTODO DO INDOFENOL). Notas: Aprovada pela Deliberação CECA nº 686, de 25 de julho de 1985. Publicada no DOERJ de 14 de julho de 1985. 1. OBJETIVO O objetivo
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA. Tópicos de Química Experimental. Débora Alvim/ Willian Miguel
 MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
TITULAÇÃO ÁCIDO-BASE. Versão aluno
 ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão aluno O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
ESCOLA SECUNDÁRIA DE S. LOURENÇO EM PORTALEGRE ACTIVIDADE LABORATORIAL QUÍMICA 11º ANO TITULAÇÃO ÁCIDO-BASE Versão aluno O que se pretende: Conhecer processos para neutralizar resíduos de ácidos/bases
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata)
 Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Técnicas de Trabalho com Material Volumétrico
 Universidade Federal de Goiás Instituto de Química Curso Experimental de Transformações Químicas 2010 Prof. Dr. Anselmo (adaptado, Agustina) Técnicas de Trabalho com Material Volumétrico 1 Objetivo Nesta
Universidade Federal de Goiás Instituto de Química Curso Experimental de Transformações Químicas 2010 Prof. Dr. Anselmo (adaptado, Agustina) Técnicas de Trabalho com Material Volumétrico 1 Objetivo Nesta
DETERMINAÇÃO DO TEOR DE CAFEÍNA NUMA BEBIDA ESTIMULANTE
 DETERMIAÇÃO DO TEOR DE CAFEÍA UMA BEBIDA ESTIMULATE 1. OBJECTIVO Utilizar a técnica de extracção descontínua líquido-líquido, para determinar o teor de cafeína numa bebida estimulante. Utilizar o processo
DETERMIAÇÃO DO TEOR DE CAFEÍA UMA BEBIDA ESTIMULATE 1. OBJECTIVO Utilizar a técnica de extracção descontínua líquido-líquido, para determinar o teor de cafeína numa bebida estimulante. Utilizar o processo
DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA
 DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA MATERIAIS Reagentes Carbonato de sódio P.A. (PM= 106) Reagente Folin Ciocalteu Padrão de ácido gálico anidro (PM= 170,2)
DETERMINAÇÃO DO TEOR DE FENÓLICOS TOTAIS (FOLIN-CIOCALTEU) - ESPECTROFOTOMETRIA MATERIAIS Reagentes Carbonato de sódio P.A. (PM= 106) Reagente Folin Ciocalteu Padrão de ácido gálico anidro (PM= 170,2)
POQ 6 Determinação do teor de Lípidos
 POQ 6 Determinação do teor de Lípidos Elaboração: RQ Verificação: DT e RDQ Aprovação: DT e RQ Entidade Emissora: RQ POQ 6 E0 (18-10-2013) 1/7 Historial de Versões Edição Data Motivo da Emissão/Alterações
POQ 6 Determinação do teor de Lípidos Elaboração: RQ Verificação: DT e RDQ Aprovação: DT e RQ Entidade Emissora: RQ POQ 6 E0 (18-10-2013) 1/7 Historial de Versões Edição Data Motivo da Emissão/Alterações
Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas
 Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas CAPÍTULO IX NÚMERO MAIS PROVÁVEL DE COLIFORMES TOTAIS E COLIFORMES TERMOTOLERANTES EM ÁGUA E GELO 1. OBJETIVOS E ALCANCE
Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas CAPÍTULO IX NÚMERO MAIS PROVÁVEL DE COLIFORMES TOTAIS E COLIFORMES TERMOTOLERANTES EM ÁGUA E GELO 1. OBJETIVOS E ALCANCE
Equilíbrio de solubilidade
 Equilíbrio de solubilidade Solubilidade É a quantidade máxima de soluto que se pode dissolver numa certa quantidade de solvente, a uma dada temperatura e pressão. Solubilidade se sais em água: Regra geral
Equilíbrio de solubilidade Solubilidade É a quantidade máxima de soluto que se pode dissolver numa certa quantidade de solvente, a uma dada temperatura e pressão. Solubilidade se sais em água: Regra geral
AULA 3. Soluções: preparo e diluição. Laboratório de Química QUI OBJETIVOS
 AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
Contagem Padrão em Placas. Profa. Leila Larisa Medeiros Marques
 Contagem Padrão em Placas Profa. Leila Larisa Medeiros Marques 1. OBJETIVOS E ALCANCE Estabelecer procedimento para a contagem padrão de microrganismos mesófilos aeróbios estritos e facultativos viáveis.
Contagem Padrão em Placas Profa. Leila Larisa Medeiros Marques 1. OBJETIVOS E ALCANCE Estabelecer procedimento para a contagem padrão de microrganismos mesófilos aeróbios estritos e facultativos viáveis.
ISSN Manual de Soluções e Reagentes da Embrapa Agrobiologia
 0 Documentos Número, 86 ISSN 1517-8498 Março/1999 Manual de Soluções e Reagentes da Embrapa Agrobiologia Empresa Brasileira de Pesquisa Agropecuária Agrobiologia Ministério da Agricultura e do Abastecimento
0 Documentos Número, 86 ISSN 1517-8498 Março/1999 Manual de Soluções e Reagentes da Embrapa Agrobiologia Empresa Brasileira de Pesquisa Agropecuária Agrobiologia Ministério da Agricultura e do Abastecimento
UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO NP EN ANÁLISE GRANULOMÉTRICA
 UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO ANÁLISE GRANULOMÉTRICA MÉTODO DA PENEIRAÇÃO Versão 2 DOCENTE: Engº Elson Almeida 2006 CONSIDERAÇÕES
UNIVERSIDADE DO ALGARVE ESCOLA SUPERIOR DE TECNOLOGIA ÁREA DEPARTAMENTAL DE ENGENHARIA CIVIL LABORATÓRIO ANÁLISE GRANULOMÉTRICA MÉTODO DA PENEIRAÇÃO Versão 2 DOCENTE: Engº Elson Almeida 2006 CONSIDERAÇÕES
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
Química Geral Experimental - Aula 4
 Química Geral Experimental - Aula 4 Título da Prática: Determinação do teor de álcool etílico na gasolina. Objetivos: Determinar o teor de álcool etílico na gasolina Comercial. Determinar o teor de água
Química Geral Experimental - Aula 4 Título da Prática: Determinação do teor de álcool etílico na gasolina. Objetivos: Determinar o teor de álcool etílico na gasolina Comercial. Determinar o teor de água
AULA PRÁTICA Nº / Maio / 2016 Profª Solange Brazaca DETERMINAÇÃO DE CARBOIDRATOS
 AULA PRÁTICA Nº - 08 05 / Maio / 2016 Profª Solange Brazaca FUNDAMENTO: DETERMINAÇÃO DE CARBOIDRATOS Este método baseia-se na propriedade que alguns açúcares apresentam em reduzir o Cu+2 (Íon Cúprico)
AULA PRÁTICA Nº - 08 05 / Maio / 2016 Profª Solange Brazaca FUNDAMENTO: DETERMINAÇÃO DE CARBOIDRATOS Este método baseia-se na propriedade que alguns açúcares apresentam em reduzir o Cu+2 (Íon Cúprico)
MT DEPARTAMENTO NACIONAL DE ESTRADAS DE RODAGEM
 Método de Ensaio Página 1 de 6 RESUMO Este documento, que é uma norma técnica, apresenta o procedimento para a avaliação da durabilidade de agregado pelo emprego de soluções de. Prescreve a aparelhagem,
Método de Ensaio Página 1 de 6 RESUMO Este documento, que é uma norma técnica, apresenta o procedimento para a avaliação da durabilidade de agregado pelo emprego de soluções de. Prescreve a aparelhagem,
Teste Simplificado para Detecção de Coliformes Totais
 NOV 2011 BLH-IFF/NT- 40.11 Rede Nacional de Bancos de Leite Humano PNQBLH Programa Nacional de Qualidade em Bancos de Leite Humano Sede: FIOCRUZ/IFF-BLH Av. Rui Barbosa, 716 Flamengo Rio de Janeiro CEP:
NOV 2011 BLH-IFF/NT- 40.11 Rede Nacional de Bancos de Leite Humano PNQBLH Programa Nacional de Qualidade em Bancos de Leite Humano Sede: FIOCRUZ/IFF-BLH Av. Rui Barbosa, 716 Flamengo Rio de Janeiro CEP:
Síntese do Biodiesel a partir de óleo vegetal Procedimento experimental (adaptado de 1 )
 Síntese do Biodiesel a partir de óleo vegetal Procedimento experimental (adaptado de 1 ) O biodiesel é atualmente um combustível em fase de desenvolvimento no nosso país, estando algumas fábricas já em
Síntese do Biodiesel a partir de óleo vegetal Procedimento experimental (adaptado de 1 ) O biodiesel é atualmente um combustível em fase de desenvolvimento no nosso país, estando algumas fábricas já em
QUI095 - Análise Volumétrica
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUI095 - Análise Volumétrica 2 semestre 2018 Prof. Renato Caamrgo Matos Download aulas: http://www.ufjf.br/nupis/
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUI095 - Análise Volumétrica 2 semestre 2018 Prof. Renato Caamrgo Matos Download aulas: http://www.ufjf.br/nupis/
Lista de Exercício. Professor: Cassio Pacheco Disciplina: Química 2 Ano Data de entrega: 04/03/2016. Concentração Comum
 Professor: Cassio Pacheco Disciplina: Química 2 Ano Data de entrega: 04/03/2016 Lista de Exercício Concentração Comum 1- Num balão volumétrico de 250 ml adicionam-se 2,0g de sulfato de amônio sólido; o
Professor: Cassio Pacheco Disciplina: Química 2 Ano Data de entrega: 04/03/2016 Lista de Exercício Concentração Comum 1- Num balão volumétrico de 250 ml adicionam-se 2,0g de sulfato de amônio sólido; o
Aula 4 PREPARO DE SOLUÇÕES. META Introduzir técnicas básicas de preparo de soluções.
 PREPARO DE SOLUÇÕES META Introduzir técnicas básicas de preparo de soluções. OBJETIVOS Ao final desta aula o aluno deverá: Fornecer conhecimento necessário para o preparo de soluções. Calcular a concentração
PREPARO DE SOLUÇÕES META Introduzir técnicas básicas de preparo de soluções. OBJETIVOS Ao final desta aula o aluno deverá: Fornecer conhecimento necessário para o preparo de soluções. Calcular a concentração
FQE0001 Exp. 04. Físico-Química Experimental. Termoquímica. 1. Introdução
 1. Introdução Termoquímica Termoquímica é o ramo da termodinâmica que estuda o calor trocado entre o sistema e sua vizinhança devido à ocorrência de uma reação química ou transformação de fase. Desta maneira,
1. Introdução Termoquímica Termoquímica é o ramo da termodinâmica que estuda o calor trocado entre o sistema e sua vizinhança devido à ocorrência de uma reação química ou transformação de fase. Desta maneira,
LEQ III Catálise Heterogénea
 LEQ III Catálise Heterogénea SÍNTESE E CARACTERIZAÇÃO DO ZEÓLITO Y SEM image XRD powder pattern and simulated pattern IST, Fevereiro 2019 1 fonte: http://webmineral.com/specimens/faujasite.shtml (Intergrown
LEQ III Catálise Heterogénea SÍNTESE E CARACTERIZAÇÃO DO ZEÓLITO Y SEM image XRD powder pattern and simulated pattern IST, Fevereiro 2019 1 fonte: http://webmineral.com/specimens/faujasite.shtml (Intergrown
AULA PRÁTICA 4 Série de sólidos
 SANEAMENTO AMBIENTAL EXPERIMENTAL TH 758 DHS PPGERHA - UFPR AULA PRÁTICA 4 Série de sólidos 1. Série de sólidos Resíduos ou sólidos são todas as matérias suspensas ou dissolvidas na água, provenientes
SANEAMENTO AMBIENTAL EXPERIMENTAL TH 758 DHS PPGERHA - UFPR AULA PRÁTICA 4 Série de sólidos 1. Série de sólidos Resíduos ou sólidos são todas as matérias suspensas ou dissolvidas na água, provenientes
1. PREPARO DE SOLUÇÕES E TITULAÇÃO
 1. PREPARO DE SOLUÇÕES E TITULAÇÃO I. INTRODUÇÃO Solução é uma mistura homogênea de uma ou mais substâncias. A substância presente em maior quantidade é denominada solvente, e as outras substâncias na
1. PREPARO DE SOLUÇÕES E TITULAÇÃO I. INTRODUÇÃO Solução é uma mistura homogênea de uma ou mais substâncias. A substância presente em maior quantidade é denominada solvente, e as outras substâncias na
