01. (UFSC) O número de oxidação do chalcogênio (O, S, Se, Te, Po) nos compostos H2O2, HMnO4, Na2O4 e F2O são respectivamente:
|
|
|
- Martín Van Der Vinne Azeredo
- 9 Há anos
- Visualizações:
Transcrição
1 Prof Exercícios extras Número de oxidação Aluno : Lista 01 Exercícios Extras Número de oxidação 01. (UFSC) O número de oxidação do chalcogênio (O, S, Se, Te, Po) nos compostos H2O2, HMnO4, Na2O4 e F2O são respectivamente: a) 1, -2, -2, -0,5 b) 1, -2, -0,5, +2 c) 2, -2, -2, -2 d) 0,5, +2, -1, +2 e) 1, -0,5, +1, (UFES) Considere o composto químico fosfato de cálcio, também chamado de ortofosfato de cálcio. Em relação a ele, marque a opção incorreta: (Ca = 40, P = 31, O = 16) a) sua fórmula contém 13 (treze átomos); b) a massa de seu mol é de 310 g; c) o número de oxidação do fósforo é +5; d) o composto é um sal normal; e) o cálcio substitui os dois hidrogênios ionizáveis do ácido de origem. 03. Explique porque a frase d é certa ou errada. 04. (ITA) Dadas as substâncias abaixo, em qual delas o nº de oxidação do manganês é máximo? I. MnO2 II. Mn III. MnSO4 IV. K2MnO4 V. KMnO4 a) I b) II c) II d) IV e) V
2 05. (UEMT) A soma algébrica dos números de oxidação do iodo nas seguintes substâncias: hipoiodito de sódio, iodeto de sódio, iodato de amônio e iodo elementar é: a) 3 b) 4 c) 5 d) 6 e) (UFSE) Calcule o número de oxidação do cloro nos compostos: a) HCl b) HClO c) HClO2 d) Ba(ClO3)2 e) Al(ClO4)3 07. (MACK) Assinale o número de oxidação INCORRETO: a) Li = -1 b) N = +5 c) S = -2 d) Cl = -1 e) Sr = (GV) Os números de oxidação do cromo nos compostos K2Cr2O7, K2CrO4 e Cr2(SO4)3 são respectivamente: a) 6, 4, 3 b) 3, 4, 3 c) 6, 6, 3 d) 3, 3, 3 e) 6, 3, (OSEC) Qual das reações abaixo é uma reação de oxi-redução? a) H3PO4 + NaOH NaH2PO4 + H2O b) CaCO3 CaO + CO2 c) 2 NH3 N2 + 3 H2 d) HNO3 + H2O H3O+ + NO e) AgNO3 + NaCl AgCl + NaNO3
3 Para responder a pergunta 10, considere as seguintes reações químicas: 1. 2 FeSO4 + 2 Ce(SO4)2 + Fe2(SO4)3 + Ce2(SO4)3 2. AgNO3 + NaCl AgCl + NaNO3 3. CuSO4 + 4 NH4OH Cu(NH3)4SO4 + 4 H2O 4. Al(OH)3 + 3 HCl AlCl3 + 3 H2O 5. H2S + 8 HNO3 H2SO4 + 8 NO2 + 4 H2O 10. (FMU) Assinale qual dessas reações químicas é de neutralização: a) 1 b) 2 c) 3 d) 4 e) 5 Resolução: 01. B 02. E 03. Certa. O sal não apresenta H+ nem OH-. Se tivesse H+ seria um sal ácido e OH- um sal básico. 04. E 05. C 06. a) 1 b) +1 c) +3 d) +5 e) A 08. C 09. C 10. D
4 Lista 02- ExercíciosExtra Número de oxidação e oxi-redução. 1. (MACKENZIE-SP) sabendo que o cloro pertence à família dos halogênios, a substância na qual o cloro apresenta número de oxidação máximo é: a) Cl 2 O 5. b) HCl. c) Cl 2 O. d) HClO 4. e) Cl Considere os compostos de fórmulas: NaNO 2 ; H 2 PO 3 ; Ba 2 As 2 O 7 Os Nox dos elementos que pertencem ao grupo 15, presentes nesses compostos, são, respectivamente: a) e + 2. b) + 2, - 4 e - 5. c) + 3, - 2 e - 5. d) e + 3. e) e Os números de oxidação do enxofre nas espécies SO 2 e SO 4 2- são, respectivamente: a) zero e + 4. b) + 1 e 4. c) + 2 e + 8. d) + 4 e + 6. e) 4 e Descobertas recentes da medicina indicam a eficiência do óxido nítrico, NO, no tratamento de determinado tipo de pneumonia. Sendo facilmente oxidado a NO 2,
5 quando preparado em laboratório, o ácido nítrico deve ser recolhido em meio que não contenha oxigênio. Os Nox do nitrogênio no NO e NO 2 são, respectivamente: a) + 3 e + 6. b) + 2 e + 4. c) + 2 e + 2. d) zero e + 4. e) zero e Assinale a alternativa cuja equação química não representa uma reação de oxiredução: a) N 2 + H 2 2NH 3. b) Cl 2 + NaI NaCl + I 2. c) Fe + HCl FeCl 2 + H 2. d) C 2 H 6 O + O 2 CO 2 + H 2 O. e) Na 2 O + HCl NaCl + H 2 O. 6. Na equação representativa de uma reação de oxi-redução: Ni + Cu 2+ Ni 2+ + Cu a) O íon Cu 2+ é o oxidante porque ele é oxidado. b) O íon Cu 2+ é o redutor porque ele é reduzido. c) O Ni é redutor porque ele é oxidado. d) O Ni é o oxidante porque ele é oxidado. e) O Ni é o oxidante e o íon Cu 2+ é o redutor. 7. Na reação de oxi-redução H 2 S + I 2 S + 2HI, as variações dos números de oxidação do enxofre e do iodo são, respectivamente: a) +2 para zero e zero para +1. b) zero para +2 e +1 para zero. c) zero para -2 e -1 para zero. d) zero para -1 e -1 para zero.
6 e) 2 para zero e zero para Para uma reação de óxido-redução: a) o agente redutor sofre redução. b) a substância que perde o elétron é o agente redutor. c) o número de oxidação do agente oxidante aumenta. d) o número de oxidação do agente redutor diminui. e) a substância que perde elétron é o agente oxidante. 9. O elemento X reage com o elemento Z, conforme o processo: Z 3 + X Z 1 + X 2 Nesse processo: a) Z ganha elétrons de X. b) X ganha elétrons de Z. c) X e Z cedem elétrons. d) X e Z perdem elétrons. e) X e Z cedem e ganham elétrons, respectivamente. 10. Tratando-se o fósforo branco (P 4 ) com solução aquosa de ácido nítrico (HNO 3 ) obtêm-se ácido fosfórico e monóxido de nitrogênio, segundo a equação química equilibrada. 3 P HNO H 2 O 12 H 3 PO NO Os agentes oxidante e redutor dessa reação são, respectivamente: a) P 4 e HNO 3. b) P 4 e H 2 O. c) HNO 3 e P 4. d) H 2 O e HNO 3. e) H 2 O e P O ferro galvanizado apresenta-se revestido por uma camada de zinco. Se um objeto desse material for riscado, o ferro ficará exposto às condições do meio
7 ambiente e poderá formar o hidróxido ferroso. Nesse caso, o zinco, por ser mais reativo, regenera o ferro, conforme a reação representada abaixo: Fe(OH) 2 + Zn Zn(OH) 2 + Fe Sobre essa reação pode-se afirmar: a) O ferro sofre oxidação, pois perderá elétrons. b) O zinco sofre oxidação, pois perderá elétrons. c) O ferro sofre redução, pois perderá elétrons. d) O zinco sofre redução, pois ganhará elétrons. e) O ferro sofre oxidação, pois ganhará elétrons. 12. Na reação representada pela equação abaixo, concluímos que todas as afirmações estão corretas, exceto: 2 Na + 2 H 2 O 2 NaOH + H 2 a) O sódio é o agente redutor. b) O íon hidroxila é reduzido. c) O sódio é oxidado. d) A água é o agente oxidante. e) O hidrogênio é reduzido. 13. Em uma reação de oxi-redução, o agente oxidante: a) perde elétrons. b) sofre oxidação. c) aumenta sua carga positiva. d) sofre redução. e) passa a ter carga nula. 14. O processo em que um átomo cede elétron a outro é denominado transformação de oxidoredução, que pode ser identificada na situação seguinte: a) Envelhecimento do ouro. b) Formação de ferrugem.
8 c) Conservação de alimentos. d) Dissolução de comprimidos efervescentes. e) Reação de neutralização entre um ácido e uma base de Arrhenius. Gabarito: 1.(D); 2.(E); 3.(D); 4.(B); 5.(E); 6.(C); 7.(E); 8.(B); 9.(B); 10.(C); 11.(B); 12.(B); 13.(D); 14.(B). Lista 03- ExercíciosExtra Número de oxidação e oxi-redução. 02)(Puc-rio 2003) Indique o número de oxidação de cada elemento nos respectivos compostos, relacionando as colunas: I) Ca em CaCO 3 II) Cl em HCl III) Na em Na 2 SO 4 IV) N em HNO 3 V) O em O 2 ( ) -1 ( ) 0 ( ) +1 ( ) +2 ( ) +5 Marque a opção que corresponde à seqüência correta de cima para baixo a) II, V, III, I, IV. b) II, V, III, IV, I. c) III, IV, II, I, V. d) V, II, I, III, IV. e) V, III, II, I, IV. 03)(Pucmg 2006) O número de oxidação (Nox) de um elemento quantifica seu estado de oxidação. Qual é o Nox de Cr no ânion Cr 2 O 7 2-? a) +3 b) +5 c) +6 d) +7 04)(Pucpr 2001) A água sanitária, água de cândida ou água de lavadeira, é uma solução aquosa de hipoclorito de sódio, utilizada como alvejante. O sal presente nessa solução apresenta na sua estrutura o átomo de cloro com Nox igual a: a) zero b) 1+ c) 1-
9 d) 2+ e) 2-05)(Pucrs 2003) O número de oxidação do átomo de carbono nas estruturas CH 4, HCHO e CO 3 2- é, respectivamente, a) b) c) d) e) )(Uerj 2008) O nitrogênio atmosférico, para ser utilizado pelas plantas na síntese de substâncias orgânicas nitrogenadas, é inicialmente transformado em compostos inorgânicos, por ação de bactérias existentes no solo. No composto inorgânico oxigenado principalmente absorvido pelas raízes das plantas, o número de oxidação do nitrogênio corresponde a: a) 0 b) + 1 c) + 2 d) )(Uff 2004) Uma das principais impurezas que existem nos derivados de petróleo e no carvão mineral é o enxofre. Quando esses combustíveis são utilizados, a queima do enxofre produz SO 2 de cheiro irritável e esse, por sua vez, na atmosfera, reage com o oxigênio e se transforma lentamente no SO 3. Essa reação é acelerada pela presença de poeira na atmosfera. O SO 3 reage com a água da chuva produzindo o H 2 SO 4 que é um ácido forte. Durante esse processo o enxofre passa por diferentes estados de oxidação. Em relação às substâncias SO 2, SO 3 e H 2 SO 4 o número de oxidação do enxofre é, respectivamente: a) + 4, + 6, + 6 b) - 4, + 4, + 6 c) + 2, - 3, 0 d) - 2, + 3, + 6 e) - 4, + 6, 0 08)(Ufpi 2000) Um anti-séptico bucal contendo peróxido de zinco - ZnO 2, suspenso em água é efetivo no tratamento de infecções orais causadas por microorganismos. Indique o número de oxidação do zinco nesta substância. a) -2 b) -1 c) +1 d) +2 e) +4 09)(Ufpr 2008) O nitrogênio (N) é capaz de formar compostos com estados de oxidação que variam de - 3 a + 5. Cinco exemplos das inúmeras moléculas que o N pode formar são apresentados a seguir. Dados os números atômicos do N (= 7), do H (= 1) e do O (= 8), numere a coluna II de acordo com a coluna I.
10 COLUNA I 1. NO 2. N 2 O 3. NH 3 4. N 2 H 4 5. NO 2 COLUNA II ( ) - 2 ( ) - 3 ( ) + 4 ( ) + 2 ( ) + 1 Assinale a alternativa que apresenta a numeração correta da coluna II, de cima para baixo. a) b) c) d) e) )(Ufrrj 2003) Nas substâncias CO 2, KMnO 4, H 2 SO 4, os números de oxidação do carbono, manganês e enxofre são, respectivamente, a) +4, +7, +6. b) +3, +7, +6. c) +4, +6, +6. d) +3, +7, +4. e) +4, +7, )(Ufrs 2007) No ânion tetraborato, B 4 O 7 2-, o número de oxidação do boro é igual a a) 2. b) 3. c) 4. d) 5. e) 7. 12)(Ufsm 2004) Quando uma área com floresta precisa ser encoberta para a formação do lago artificial de uma hidroelétrica, toda a madeira deve ser retirada. Se isso não ocorrer, esse material entra em decomposição, podendo provocar danos nas turbinas, além de crescimento descontrolado da população de algas azuis (cianobactérias) e verdes ('Chlorophyta') e de algumas plantas flutuantes, como 'Eichorniacrassipes', o aguapé ('Angiospermae'), e 'Salviniasp.' ('Pteridophyta'). O caldo formado pela matéria orgânica encoberta pela água das barragens é altamente corrosivo. A decomposição da matéria orgânica em ambiente eutrofizado ocorre de modo anaeróbio e envolve muitas reações químicas. Uma delas é a fermentação da celulose que gera grande quantidade de metano e gás carbônico cujos átomos de carbono possuem, respectivamente, os números de
11 oxidação a) 0 e -4 b) -4 e +4 c) +4 e 0 d) +4 e -4 e) -2 e +2 13)(Ufv 2003) Os números de oxidação do Boro, Iodo e Enxofre nas espécies químicas H 2 BO 3, IO 4 e HSO 4 - são, respectivamente: a) +4, +8, +7 b) +3, +7, +8 c) +3, +7, +6 d) +4, +5, +6 e) +2, +6, +5 14)(Unesp 2008) O nitrogênio pode existir na natureza em vários estados de oxidação. Em sistemas aquáticos, os compostos que predominam e que são importantes para a qualidade da água apresentam o nitrogênio com números de oxidação -3, 0, +3 ou +5. Assinale a alternativa que apresenta as espécies contendo nitrogênio com os respectivos números de oxidação, na ordem descrita no texto. a) NH 3, N 2, NO 2 -, NO 3 -. b) NO 2 -, NO 3 -, NH 3, N 2. c) NO 3 -, NH 3, N 2, NO 2 -. d) NO 2 -, NH 3, N 2, NO 3 -. e) NH 3, N 2, NO 3 -, NO )(Ufsm 2004) As usinas hidroelétricas, que utilizam a água acumulada em represas para fazer funcionar suas turbinas, são responsáveis pela perturbação no ciclo natural das cheias e secas dos rios, pela inundação de áreas de terra cada vez maiores, pela retenção de nutrientes que, se não fosse esse uso, estariam distribuídos mais ou menos uniformemente, ao longo dos rios. A queima de carvão mineral para a geração do vapor d'água que move as turbinas das usinas termoelétricas lança, na atmosfera, além de dióxido de carbono, grandes quantidades de enxofre e óxidos nitrogenados, gases que formam a chuva ácida. As usinas nucleares causam impacto ambiental mesmo na ausência de acidentes, porque retiram a água do mar ou dos rios para resfriar os núcleos de seus geradores, devolvendo-a a uma temperatura bem mais alta. Esse aquecimento afeta os organismos aquáticos, pois o aumento da temperatura deixa a água pobre em oxigênio pela diminuição da solubilidade. Com a diminuição do ph, não há mais proteção da ferragem. No processo de oxidação do ferro, há expansão de volume e conseqüente fragmentação do concreto. As equações que podem representar a formação da ferrugem pela ação do CO 2 e da água são: 1) Fe+CO 2 +H 2 O FeCO 3 +H 2 2) FeCO 3 +CO 2 +H 2 O Fe(HCO 3 ) 2 3) 4Fe(HCO 3 ) 2 +O 2 2(Fe 2 O 3. 2 H 2 O)+8CO 2
12 O número de oxidação do ferro nos compostos Fe(HCO 3 ) 2 e Fe 2 O 3. 2 H 2 O é, respectivamente, a) +1 e +2 b) +1 e +3 c) +2 e +2 d) +2 e +3 e) +3 e +3 GABARITO 02 - A; 03 - C; 04 - B; 05 - B; 06 - D; 07 - A; 08 - D; 09 - B; 10 - A; 11 - B; 12 - B; 13 - C; 14 - A; 15 - D Lista 04- ExercíciosExtra Número de oxidação e oxi-redução. 1) Calcule o número de oxidação da substância MgSiO3 Resolução: Mg Si O x -2 podemos afirmar o Nox do magnésio,porque este pertence a família IIA, o que lhe confere Nox = +2 e o Nox do oxigênio vale = - 2 Assim devemos encontrar o valor do Nox do silício Mg Si O x x -6 = 0 ( moléculas neutras tem Nox = 0 ) para resolver o exercício temos que resolver a equação de 1. Grau +2 +x -6 = 0 +x 4 = 0 +x = 4
13 o Nox do silício nesta molécula vale +4. 2) (Puccamp SP) Descobertas recentes da Medicina indicam a eficiência do óxido nítrico (NO) no tratamento de determinado tipo de pneumonia. Sendo facilmente oxidado pelo oxigênio e NO2, quando preparado em laboratório, o ácido nítrico deve ser recolhido em meio que não contenha O2. Os números de oxidação do nitrogênio no NO e NO2 são, respectivamente: a) + 3 e + 6. b) + 2 e + 4. c) + 2 e + 2. d) zero e + 4. e) zero e + 2. Resolução: Alternativa b Lembre-se que a soma dos Nox na substância deve dar igual a zero e que o Nox do oxigênio é -2. Assim, temos: 3) Determine os números de oxidação para cada elemento das espécies químicas abaixo: a) HBr b) ClO4- c) H2O2 d) NaCl e) MnBr2
14 f) Na2S2O3 Resolução: a) HBr H = +1 ; Br = -1 b) ClO4- Cl = +7 ; O = -2 c) H2O2 H =+1; O = -1 d) NaCl Na = +1; Cl = -1 e) MnBr2 Mn = +2; Br = -1 f) Na2S2O3 Na = +1; S = +2; O = -2 4) O enxofre é um sólido amarelo encontrado livre na natureza em regiões onde ocorrem fenômenos vulcânicos. As suas variedades alotrópicas são o rômbico e o monoclínico. Esse elemento participa de várias substâncias e íons, tais como: S8, H2S, SO2, H2SO4, H2SO3, SO3, SO42- e Al2(SO4)3. Determine os Nox do enxofre em cada uma dessas espécies químicas. Resolução: S8: Nox = 0 H2S: Nox = -2 SO2: Nox = +4 H2SO4: Nox = +6 H2SO3: Nox = +4
15 SO3: Nox = +6 SO42-: Nox = +6 Al2(SO4)3: Nox = +6 5) (Uerj 2008) O nitrogênio atmosférico, para ser utilizado pelas plantas na síntese de substâncias orgânicas nitrogenadas, é inicialmente transformado em compostos inorgânicos, por ação de bactérias existentes no solo. No composto inorgânico oxigenado principalmente absorvido pelas raízes das plantas, o número de oxidação do nitrogênio corresponde a: a) 0 b) + 1 c) + 2 d) + 5 6) (Pucrs 2003) O número de oxidação do átomo de carbono nas estruturas CH 4, HCHO e CO 3 2- é, respectivamente, a) b) c) d) e) ) (Ufrs 2007) No ânion tetraborato, B 4 O 7 2-, o número de oxidação do boro é igual a a) 2. b) 3. c) 4. d) 5. e) 7. 8) (Unesp 2008) O nitrogênio pode existir na natureza em vários estados de oxidação. Em sistemas aquáticos, os compostos que predominam e que são importantes para a qualidade da água apresentam o nitrogênio com números de oxidação -3, 0, +3 ou +5. Assinale a alternativa que apresenta as espécies contendo nitrogênio com os respectivos números de oxidação, na ordem descrita no texto.
16 a) NH 3, N 2, NO 2 -, NO 3 -. b) NO 2 -, NO 3 -, NH 3, N 2. c) NO 3 -, NH 3, N 2, NO 2 -. d) NO 2 -, NH 3, N 2, NO 3 -. e) NH 3, N 2, NO 3 -, NO ) (Ufsm 2004) As usinas hidroelétricas, que utilizam a água acumulada em represas para fazer funcionar suas turbinas, são responsáveis pela perturbação no ciclo natural das cheias e secas dos rios, pela inundação de áreas de terra cada vez maiores, pela retenção de nutrientes que, se não fosse esse uso, estariam distribuídos mais ou menos uniformemente, ao longo dos rios. A queima de carvão mineral para a geração do vapor d'água que move as turbinas das usinas termoelétricas lança, na atmosfera, além de dióxido de carbono, grandes quantidades de enxofre e óxidos nitrogenados, gases que formam a chuva ácida. As usinas nucleares causam impacto ambiental mesmo na ausência de acidentes, porque retiram a água do mar ou dos rios para resfriar os núcleos de seus geradores, devolvendo-a a uma temperatura bem mais alta. Esse aquecimento afeta os organismos aquáticos, pois o aumento da temperatura deixa a água pobre em oxigênio pela diminuição da solubilidade. Com a diminuição do ph, não há mais proteção da ferragem. No processo de oxidação do ferro, há expansão de volume e conseqüente fragmentação do concreto. As equações que podem representar a formação da ferrugem pela ação do CO 2 e da água são: 1) Fe+CO 2 +H 2 O FeCO 3 +H 2 2) FeCO 3 +CO 2 +H 2 O Fe(HCO 3 ) 2 3) 4Fe(HCO 3 ) 2 +O 2 2(Fe 2 O 3. 2 H 2 O)+8CO 2 O número de oxidação do ferro nos compostos Fe(HCO 3 ) 2 e Fe 2 O 3. 2 H 2 O é, respectivamente, a) +1 e +2 b) +1 e +3 c) +2 e +2 d) +2 e +3 e) +3 e +3 10)(Puc-rio 2003) Indique o número de oxidação de cada elemento nos respectivos compostos, relacionando as colunas:
17 I) Ca em CaCO 3 II) Cl em HCl III) Na em Na 2 SO 4 IV) N em HNO 3 V) O em O 2 ( ) -1 ( ) 0 ( ) +1 ( ) +2 ( ) +5 Marque a opção que corresponde à seqüência correta de cima para baixo a) II, V, III, I, IV. b) II, V, III, IV, I. c) III, IV, II, I, V. d) V, II, I, III, IV. e) V, III, II, I, IV. 11)(UFPB 2008) Nos feldspatos alcalinos, os átomos de oxigênio possuem estado de oxidação 2. Assim, é correto afirmar que, no feldspato de fórmula KAlSi 3 O 8, os elementos K, Al e Si possuem, respectivamente, os seguintes estados de oxidação: a)+1, +3,+4 b)+2, +3, -3 c)-2, +2, +3 d)+1, -3, +4 e)+1, +3, +2
18 12) (UFPB 2008) No Sulfato de cálcio (CaSO 4 ), os átomos de oxigênio apresentam estado de oxidação 2 e o Ca, estado de oxidação +2. A partir dessas informações, é correto afirmar: a)o íon Ca+2 possui configuração eletrônica 1s 2 2s 2 2p 6 3s 2 3p 2 b)o íon Ca+2 possui 20 prótons e 20 elétrons. c)o íon O 2 possui 8 prótons e 6 elétrons. d)o íon O 2 possui configuração eletrônica 1s 2 2s 2 2p 4. e)os elétrons mais energéticos do O 2 possuem números quânticos, principal e secundário, iguais a 2 e 1, respectivamente. 13)(MACKENZIE-SP) sabendo que o cloro pertence à família dos halogênios, a substância na qual o cloro apresenta número de oxidação máximo é: a) Cl 2 O 5. b) HCl. c) Cl 2 O. d) HClO 4. e) Cl 2. 14) O processo em que um átomo cede elétron a outro é denominado transformação de oxidorredução que pode ser identificada na situação seguinte: a) Envelhecimento do ouro. b) Formação de ferrugem. c) Conservação de alimentos. d) Dissolução de comprimidos efervescentes. e) Reação de neutralização entre um ácido e uma base de Arrhenius.
19 15)O elemento X reage com o elemento Z, conforme o processo: Z 3 + X Z 1 + X 2 Nesse processo: a) Z ganha elétrons de X. b) X ganha elétrons de Z. c) X e Z cedem elétrons. d) X e Z perdem elétrons. e) X e Z cedem e ganham elétrons, respectivamente. 16) Na reação de oxi-redução H 2 S + I 2 S + 2HI, as variações dos números de oxidação do enxofre e do iodo são, respectivamente: a) +2 para zero e zero para +1. b) zero para +2 e +1 para zero. c) zero para -2 e -1 para zero. d) zero para -1 e -1 para zero. e) 2 para zero e zero para ) Assinale a alternativa cuja equação química não representa uma reação de oxiredução: a) N 2 + H 2 2NH 3. b) Cl 2 + NaI NaCl + I 2. c) Fe + HCl FeCl 2 + H 2. d) C 2 H 6 O + O 2 CO 2 + H 2 O. e) Na 2 O + HCl NaCl + H 2 O.
20 Gabarito: 5) D 6) B 7) B 8) A 9) D 10) A 11) A 12) E 13) D 14) B 15) B 16) E 17) E
1) Faça o balanceamento das equações abaixo:
 PROFESSORA: GIOVANA CARABALLO MELATTI DATA: / /2015 COMPONENTE CURRICULAR: QUÍMICA LISTA DE EXERCÍCIOS DE SALA ALUNO: LISTA DE EXERCÍCIOS REVISÃO 1) Faça o balanceamento das equações abaixo: a) C 2 H 6
PROFESSORA: GIOVANA CARABALLO MELATTI DATA: / /2015 COMPONENTE CURRICULAR: QUÍMICA LISTA DE EXERCÍCIOS DE SALA ALUNO: LISTA DE EXERCÍCIOS REVISÃO 1) Faça o balanceamento das equações abaixo: a) C 2 H 6
Estequiometria. Prof a. Dr a. Flaviana Tavares Vieira
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
http://www.rumoaoita.com / - Material escrito por: Marlos Cunha (ITA T-12) Métodos de Balanceamento
 Métodos de Balanceamento Conteúdo Introdução... 1 Método das tentativas... 1 Método algébrico... 1 Método do íon-elétron... 2 Método da oxi-redução... 3 Auto oxi-redução... 3 Balanceamento dependendo do
Métodos de Balanceamento Conteúdo Introdução... 1 Método das tentativas... 1 Método algébrico... 1 Método do íon-elétron... 2 Método da oxi-redução... 3 Auto oxi-redução... 3 Balanceamento dependendo do
Química Geral 3º ANO
 Química Geral 3º ANO Teoria de Arrhenius Teoria Ácido-Base Teoria de Arrhenius Teoria Ácido-Base Ácido são substâncias que, dissolvidas em água, se ionizam liberando, na forma de cátions, exclusivamente
Química Geral 3º ANO Teoria de Arrhenius Teoria Ácido-Base Teoria de Arrhenius Teoria Ácido-Base Ácido são substâncias que, dissolvidas em água, se ionizam liberando, na forma de cátions, exclusivamente
De onde vêm as lágrimas?
 De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
Professora Sonia - Química para o Vestibular Questões Resolvidas Hidrólise Salina (com respostas e resoluções no final)
 Questões Resolvidas Hidrólise Salina (com respostas e resoluções no final) 01. (Uftm) Em soluções aquosas de acetato de sódio, o íon acetato sofre hidrólise: 3 l 3 CH COO (aq) + H O( ) CH COOH (aq) + OH
Questões Resolvidas Hidrólise Salina (com respostas e resoluções no final) 01. (Uftm) Em soluções aquosas de acetato de sódio, o íon acetato sofre hidrólise: 3 l 3 CH COO (aq) + H O( ) CH COOH (aq) + OH
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014
 RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
PROFESSOR: FELIPE ROSAL DISCIPLINA: QUÍMICA CONTEÚDO: PRATICANDO AULA 1
 PROFESSOR: FELIPE ROSAL DISCIPLINA: QUÍMICA CONTEÚDO: PRATICANDO AULA 1 2 NÚMERO DE OXIDAÇÃO ( Nox ) É o número que mede a CARGA REAL ou APARENTE de uma espécie química 3 OXIDAÇÃO É a perda de elétrons
PROFESSOR: FELIPE ROSAL DISCIPLINA: QUÍMICA CONTEÚDO: PRATICANDO AULA 1 2 NÚMERO DE OXIDAÇÃO ( Nox ) É o número que mede a CARGA REAL ou APARENTE de uma espécie química 3 OXIDAÇÃO É a perda de elétrons
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
FÓRMULAS ESTRUTURAIS DOS ÁCIDOS
 FÓRMULAS ESTRUTURAIS DOS ÁCIDOS EXERCÍCIOS DE APLICAÇÃO 01 Escreva as fórmulas estruturais dos ácidos: a) HBr b) HClO 3 c) HNO 3 d) H 2 SO 3 e) H 3 AsO 4 f) H 4 P 2 O 7 02 Retirando-se os hidrogênios ligados
FÓRMULAS ESTRUTURAIS DOS ÁCIDOS EXERCÍCIOS DE APLICAÇÃO 01 Escreva as fórmulas estruturais dos ácidos: a) HBr b) HClO 3 c) HNO 3 d) H 2 SO 3 e) H 3 AsO 4 f) H 4 P 2 O 7 02 Retirando-se os hidrogênios ligados
 Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
TIPOS DE REAÇÕES QUÍMICAS MATERIAL RETIRADO PARCIALMENTE OU NA INTEGRA DE LISTAS DE EXERCÍCIOS ENCONTRADAS NA INTERNET
 TIPOS DE REAÇÕES QUÍMICAS MATERIAL RETIRADO PARCIALMENTE OU NA INTEGRA DE LISTAS DE EXERCÍCIOS ENCONTRADAS NA INTERNET 1. Unifor-CE O metal potássio reage vigorosamente com água, produzindo hidrogênio
TIPOS DE REAÇÕES QUÍMICAS MATERIAL RETIRADO PARCIALMENTE OU NA INTEGRA DE LISTAS DE EXERCÍCIOS ENCONTRADAS NA INTERNET 1. Unifor-CE O metal potássio reage vigorosamente com água, produzindo hidrogênio
O X I D A Ç Ã O E R E D U Ç Ã O
 O X I D A Ç Ã O E R E D U Ç Ã O PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto OXIDAÇÃO E REDUÇÃO www.agamenonquimica.com 2 OXIDAÇÃO E REDUÇÃO INTRODUÇÃO Colocando-se uma lâmina de zinco dentro
O X I D A Ç Ã O E R E D U Ç Ã O PROF. AGAMENON ROBERTO < 2010 > Prof. Agamenon Roberto OXIDAÇÃO E REDUÇÃO www.agamenonquimica.com 2 OXIDAÇÃO E REDUÇÃO INTRODUÇÃO Colocando-se uma lâmina de zinco dentro
As questões de 31 a 34 referem-se ao texto abaixo.
 QUÍMICA As questões de 31 a 34 referem-se ao texto abaixo. Em diversos países, o aproveitamento do lixo doméstico é quase 100%. Do lixo levado para as usinas de compostagem, após a reciclagem, obtém-se
QUÍMICA As questões de 31 a 34 referem-se ao texto abaixo. Em diversos países, o aproveitamento do lixo doméstico é quase 100%. Do lixo levado para as usinas de compostagem, após a reciclagem, obtém-se
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
S Nox total = zero. Nº de oxidação (Nox) Regras para determinar o Nox. AULA 11 Oxidação e Redução
 AULA 11 Oxidação e Redução Nº de oxidação (Nox) é a carga que surge quando os elementos estão combinados NaCl Æ Na + Cl - (sódio doou 1 e - e o cloro recebeu 1e - ) H 2 Æ H H zero Quando a ligação for
AULA 11 Oxidação e Redução Nº de oxidação (Nox) é a carga que surge quando os elementos estão combinados NaCl Æ Na + Cl - (sódio doou 1 e - e o cloro recebeu 1e - ) H 2 Æ H H zero Quando a ligação for
ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS QUESTÕES É OBRIGATÓRIO
 IX Olimpíada Capixaba de Química 2011 Prova do Grupo II 2 a série do ensino médio Fase 02 Aluno: Idade: Instituição de Ensino: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS
IX Olimpíada Capixaba de Química 2011 Prova do Grupo II 2 a série do ensino médio Fase 02 Aluno: Idade: Instituição de Ensino: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS
U N I V E R S I D A D E F E D E R A L D E M I N A S G E R A I S SÓ ABRA QUANDO AUTORIZADO.
 U N I V E R S I D A D E F E D E R A L D E M I N A S G E R A I S QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco
U N I V E R S I D A D E F E D E R A L D E M I N A S G E R A I S QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco
São partículas que atravessam o filtro, mas não são dissolvidas
 O que existe na água do mar? 1. materiais sólidos ou particulados 2. colóides 3. materiais dissolvidos 1. materiais sólidos ou particulados A definição de particulado é operacional. Todo material com >
O que existe na água do mar? 1. materiais sólidos ou particulados 2. colóides 3. materiais dissolvidos 1. materiais sólidos ou particulados A definição de particulado é operacional. Todo material com >
IONIZAÇÃO DOS ÁCIDOS NOMENCLATURA DOS ÂNIONS
 IONIZAÇÃO DOS ÁCIDOS NOMENCLATURA DOS ÂNIONS EXERCÍCIOS DE APLICAÇÃO 01 Escrever a equação de ionização (total) dos ácidos abaixo em solução aquosa, nomeando seu respectivo ânion. a) HCl b) HBrO 3 c) H
IONIZAÇÃO DOS ÁCIDOS NOMENCLATURA DOS ÂNIONS EXERCÍCIOS DE APLICAÇÃO 01 Escrever a equação de ionização (total) dos ácidos abaixo em solução aquosa, nomeando seu respectivo ânion. a) HCl b) HBrO 3 c) H
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
+1 2 Nox +1 2 Carga Nox +7 8 Carga
 01 Cl 2 Cl Nox = 0 Nox = 1 Cl O +1 2 Nox +1 2 Carga Cl O 4 +7 2 Nox +7 8 Carga Resposta: Respectivamente zero, 1, +1, +7. 1 02 a) NH 4 NO 3 NH 4 + cátion + NO 3 ânion N H 4 + 3 +1 Nox 3 +4 Carga N O 3
01 Cl 2 Cl Nox = 0 Nox = 1 Cl O +1 2 Nox +1 2 Carga Cl O 4 +7 2 Nox +7 8 Carga Resposta: Respectivamente zero, 1, +1, +7. 1 02 a) NH 4 NO 3 NH 4 + cátion + NO 3 ânion N H 4 + 3 +1 Nox 3 +4 Carga N O 3
PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS
 3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
ASSUNTO: OXIDAÇÃO E REDUÇÃO
 1 I. INTRODUÇÃO: CONCEITO DE OXI-REDUÇÃO O fenômeno da óxido-redução é muito importante no mundo que nos cerca e está presente nos processos que permitem a manutenção da vida. Tanto a fotossíntese: 6 CO
1 I. INTRODUÇÃO: CONCEITO DE OXI-REDUÇÃO O fenômeno da óxido-redução é muito importante no mundo que nos cerca e está presente nos processos que permitem a manutenção da vida. Tanto a fotossíntese: 6 CO
Determinação do número de oxidação (NOX)
 Determinação do número de oxidação (NOX) EXERCÍCIOS DE APLICAÇÃO 01 (UFSCAR-SP) Os números de oxidação do enxofre em H 2S, S 8 e Na 2SO 3 são, respectivamente, a) +2, -8 e -4. b) -2, zero, e +4. c) zero,
Determinação do número de oxidação (NOX) EXERCÍCIOS DE APLICAÇÃO 01 (UFSCAR-SP) Os números de oxidação do enxofre em H 2S, S 8 e Na 2SO 3 são, respectivamente, a) +2, -8 e -4. b) -2, zero, e +4. c) zero,
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas.
 A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza
 Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
ELETROQUÍMICA (Parte II)
 ELETROQUÍMICA (Parte II) I ELETRÓLISE A eletrólise é um processo de oxirredução não espontâneo, em que a passagem da corrente elétrica em uma solução eletrolítica (solução com íons), produz reações químicas.
ELETROQUÍMICA (Parte II) I ELETRÓLISE A eletrólise é um processo de oxirredução não espontâneo, em que a passagem da corrente elétrica em uma solução eletrolítica (solução com íons), produz reações químicas.
Lista I de exercícios de estequiometria e balanceamento de equações Química Geral e Experimental I Prof. Hamilton Viana
 1. O iso-octano é um combustível automotivo. A combustão desse material ocorre na fase gasosa. Dados a massa molar do iso-octano igual a 114g/mol, o volume molar de gás nas "condições ambiente" igual a
1. O iso-octano é um combustível automotivo. A combustão desse material ocorre na fase gasosa. Dados a massa molar do iso-octano igual a 114g/mol, o volume molar de gás nas "condições ambiente" igual a
Prof. Rafa - Química Cálculo Estequiométrico
 Prof. Rafa - Química Cálculo Estequiométrico Lista de exercícios 01. (UFBA) Hidreto de sódio reage com água, dando hidrogênio, segundo a reação: NaH + H 2 O NaOH + H 2 Para obter 10 mols de H 2, são necessários
Prof. Rafa - Química Cálculo Estequiométrico Lista de exercícios 01. (UFBA) Hidreto de sódio reage com água, dando hidrogênio, segundo a reação: NaH + H 2 O NaOH + H 2 Para obter 10 mols de H 2, são necessários
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
 CaO + H2O Ca(OH)2 3 H2 + 1 N2 2 NH3 3 H2 + 1 N2 2 NH3 + 01) A equação refere-se à transformação de ozônio em oxigênio comum, representada pela equação: 2 O3 3 O2 Os números 2 e 3 que aparecem no lado esquerdo
CaO + H2O Ca(OH)2 3 H2 + 1 N2 2 NH3 3 H2 + 1 N2 2 NH3 + 01) A equação refere-se à transformação de ozônio em oxigênio comum, representada pela equação: 2 O3 3 O2 Os números 2 e 3 que aparecem no lado esquerdo
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
Química. Resolução das atividades complementares. Q53 Ácidos de Arrhenius
 Resolução das atividades complementares 4 Química Q53 Ácidos de Arrhenius p 35 1 (UFRGS-RS) Admitindo-se 100% de ionização para o ácido clorídrico em solução diluída, pode-se afirmar que essa solução não
Resolução das atividades complementares 4 Química Q53 Ácidos de Arrhenius p 35 1 (UFRGS-RS) Admitindo-se 100% de ionização para o ácido clorídrico em solução diluída, pode-se afirmar que essa solução não
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
7- (PUCCAMP) Examine as equações químicas a seguir: I- 2CrO 4
 OXIRREDUÇÃO 1- Se X, Y e Q apresentam número de oxidação máximo nas espécies químicas XO 4 2-, MgYO 3 e H 3 QO 4, então pertencem, respectivamente, à família dos: A) Metais Alcalinos, Carbono e Nitrogênio.
OXIRREDUÇÃO 1- Se X, Y e Q apresentam número de oxidação máximo nas espécies químicas XO 4 2-, MgYO 3 e H 3 QO 4, então pertencem, respectivamente, à família dos: A) Metais Alcalinos, Carbono e Nitrogênio.
1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)?
 EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
Polaridade de moléculas
 Polaridade de moléculas 01. (Ufscar) É molécula polar: a) C 2 H 6. b) 1,2-dicloroetano. c) CH 3 Cl. d) p-diclorobenzeno. e) ciclopropano. 02. (Mackenzie) As fórmulas eletrônicas 1, 2 e 3 a seguir, representam,
Polaridade de moléculas 01. (Ufscar) É molécula polar: a) C 2 H 6. b) 1,2-dicloroetano. c) CH 3 Cl. d) p-diclorobenzeno. e) ciclopropano. 02. (Mackenzie) As fórmulas eletrônicas 1, 2 e 3 a seguir, representam,
COMENTÁRIO DA PROVA DE QUÍMICA EQUIPE DE QUÍMICA DO CURSO POSITIVO
 COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
Leis Ponderais e Cálculo Estequiométrico
 Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Gabarito de Química Frente 2
 Gabarito de Química Frente 2 Módulo 05 01. E Calculo do nox: 1) HNO 3 1 + X + 3 x (- 2) = 0 X= + 5 +1 2 X 2) HNO 2 1 + Y + 2 x (- 2) = 0 Y= + 3 +1 Y 2 3) NH 3 Z + 3 x (+1) = 0 Z = - 3 Z 02.A +1 Para calcular
Gabarito de Química Frente 2 Módulo 05 01. E Calculo do nox: 1) HNO 3 1 + X + 3 x (- 2) = 0 X= + 5 +1 2 X 2) HNO 2 1 + Y + 2 x (- 2) = 0 Y= + 3 +1 Y 2 3) NH 3 Z + 3 x (+1) = 0 Z = - 3 Z 02.A +1 Para calcular
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
Química Atomística Profª: Bruna Villas Bôas. Exercícios
 NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
QUÍMICA - 3 o ANO MÓDULO 13 SAIS
 QUÍMICA - 3 o ANO MÓDULO 13 SAIS Ácido ídrico eto oso ito ico ato Sal nome do ácido de origem eto ito ato nome do cátion da base de origem +y B x +x A y Como pode cair no enem O etanol é considerado um
QUÍMICA - 3 o ANO MÓDULO 13 SAIS Ácido ídrico eto oso ito ico ato Sal nome do ácido de origem eto ito ato nome do cátion da base de origem +y B x +x A y Como pode cair no enem O etanol é considerado um
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
Gabarito Química - Grupo A. 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor
 VESTIB LAR Gabarito Química - Grupo A 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Muitos álcoois, como o butanol (C 4 H 10 O), têm importância comercial como solventes e matériasprimas na produção industrial
VESTIB LAR Gabarito Química - Grupo A 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Muitos álcoois, como o butanol (C 4 H 10 O), têm importância comercial como solventes e matériasprimas na produção industrial
UFSC. Química (Amarela) 31) Resposta: 43. Comentário
 UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
Professor: José Tiago Pereira Barbosa
 Professor: José Tiago Pereira Barbosa Química Orgânica Inorgânica Compostos que possuem átomos de Carbono Compostos que não possuem átomos de Carbono* *Alguns compostos contendo carbono são estudados
Professor: José Tiago Pereira Barbosa Química Orgânica Inorgânica Compostos que possuem átomos de Carbono Compostos que não possuem átomos de Carbono* *Alguns compostos contendo carbono são estudados
Química. Resolução das atividades complementares. Q49 Polaridade das moléculas
 Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução: 0,86ºC. x = 0,5 mol etanol/kg acetona. 0,5 mol 1000 g de acetona. 200 g de acetona. y = 0,1 mol de etanol. 1 mol de etanol (C 2 H 6 O) 46 g
 (ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
(ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
ÁCIDOS. Função Inorgânica
 ÁCIDOS Função Inorgânica LEMBRANDO CONCEITOS: PH POTENCIAL HIDROGENIÔNICO É a medida de acidez de uma solução aquosa, cuja escala de medidas vai de 0 a 14. ALGUNS VALORES DE PH: Substância ph Coca-cola
ÁCIDOS Função Inorgânica LEMBRANDO CONCEITOS: PH POTENCIAL HIDROGENIÔNICO É a medida de acidez de uma solução aquosa, cuja escala de medidas vai de 0 a 14. ALGUNS VALORES DE PH: Substância ph Coca-cola
c) NH4OH. d) H2SO4. 4) Qual a classificação correta das moléculas NaOH, NaCl e HCl? a) Ácido, base e sal b) Sal, base e ácido
 Funções e reações inorgânicas - Exercícios 1) (UFPA) Considerando a equação química: Cl2O7 + 2 NaOH 2 NaClO4 + H2O os reagentes e produtos pertencem, respectivamente, às funções: a) óxido, base, sal e
Funções e reações inorgânicas - Exercícios 1) (UFPA) Considerando a equação química: Cl2O7 + 2 NaOH 2 NaClO4 + H2O os reagentes e produtos pertencem, respectivamente, às funções: a) óxido, base, sal e
Regras para cálculo do nox
 SÉRiE Rumo ao ITA Nº 02 ENSiN PRÉ-UNIVERSITÁRI PRFESSR(a) ALuN(a) SÉRGI MATS SEDE Nº TC TuRma TuRN DaTa / / QUÍMICA Número de xidação Número de oxidação (nox) ou estado de oxidação é a real ou imaginária
SÉRiE Rumo ao ITA Nº 02 ENSiN PRÉ-UNIVERSITÁRI PRFESSR(a) ALuN(a) SÉRGI MATS SEDE Nº TC TuRma TuRN DaTa / / QUÍMICA Número de xidação Número de oxidação (nox) ou estado de oxidação é a real ou imaginária
Olimpíada Brasileira de Química - 2009
 A Olimpíada Brasileira de Química - 2009 MODALIDADE A ( 1º e 2º anos ) PARTE A - QUESTÕES MÚLTIPLA ESCOLHA 01. O gás SO 2 é formado na queima de combustíveis fósseis. Sua liberação na atmosfera é um grave
A Olimpíada Brasileira de Química - 2009 MODALIDADE A ( 1º e 2º anos ) PARTE A - QUESTÕES MÚLTIPLA ESCOLHA 01. O gás SO 2 é formado na queima de combustíveis fósseis. Sua liberação na atmosfera é um grave
O interesse da Química é analisar as...
 O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
OSASCO-COLÉGIO DA POLÍCIA MILITAR
 OSASCO-COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo 1º Bimestre/2015 Disciplinas: Química 2ª série EM Nome do aluno Nº Turma A lista de exercícios abaixo, consta de 33 questões diversas,
OSASCO-COLÉGIO DA POLÍCIA MILITAR ASSESSORIA TÉCNICA Processo Avaliativo 1º Bimestre/2015 Disciplinas: Química 2ª série EM Nome do aluno Nº Turma A lista de exercícios abaixo, consta de 33 questões diversas,
Tabel e a l P rió dica
 Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos
 Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
PROBLEMAS AMBIENTAIS INVERSÃO TÉRMICA INVERSÃO TÉRMICA 14/02/2014. Distribuição aproximada dos principais poluentes do ar de uma cidade (SP)
 PROBLEMAS AMBIENTAIS Distribuição aproximada dos principais poluentes do ar de uma cidade (SP) Liga-se com a hemoglobina impedindo o O2 de ser conduzido INVERSÃO TÉRMICA *Inversão térmica é um fenômeno
PROBLEMAS AMBIENTAIS Distribuição aproximada dos principais poluentes do ar de uma cidade (SP) Liga-se com a hemoglobina impedindo o O2 de ser conduzido INVERSÃO TÉRMICA *Inversão térmica é um fenômeno
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
Colégio FAAT Ensino Fundamental e Médio
 Colégio FAAT Ensino Fundamental e Médio Conteúdo: Pilhas e baterias Eletrólise Recuperação do 4 Bimestre disciplina Química 2ºano Lista de exercícios 1- Na pilha Al/ Al 3+ // Cu 2+ / Cu é correto afirmar
Colégio FAAT Ensino Fundamental e Médio Conteúdo: Pilhas e baterias Eletrólise Recuperação do 4 Bimestre disciplina Química 2ºano Lista de exercícios 1- Na pilha Al/ Al 3+ // Cu 2+ / Cu é correto afirmar
P2 - PROVA DE QUÍMICA GERAL - 11/10/08
 P2 - PROVA DE QUÍMICA GERAL - 11/10/08 Nome: Gabarito Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes: R 8,314 J mol -1 K -1 0,0821
P2 - PROVA DE QUÍMICA GERAL - 11/10/08 Nome: Gabarito Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes: R 8,314 J mol -1 K -1 0,0821
Ciências da Natureza e Matemática
 1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 3 CEDAE Acompanhamento Escolar 1.(UFSCAR-SP) Os números de oxidação do enxofre em H 2 S, S 8 e Na 2 SO 3 são, respectivamente, a) +2, -8 e
1 CEDAE Acompanhamento Escolar 2 CEDAE Acompanhamento Escolar 3 CEDAE Acompanhamento Escolar 1.(UFSCAR-SP) Os números de oxidação do enxofre em H 2 S, S 8 e Na 2 SO 3 são, respectivamente, a) +2, -8 e
Sobre as substâncias representadas pelas estruturas I e II, é INCORRETO afirmar:
 8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
TC Revisão 2 Ano Termoquímica e Cinética Prof. Alexandre Lima
 TC Revisão 2 Ano Termoquímica e Cinética Prof. Alexandre Lima 1. Em diversos países, o aproveitamento do lixo doméstico é quase 100%. Do lixo levado para as usinas de compostagem, após a reciclagem, obtém-se
TC Revisão 2 Ano Termoquímica e Cinética Prof. Alexandre Lima 1. Em diversos países, o aproveitamento do lixo doméstico é quase 100%. Do lixo levado para as usinas de compostagem, após a reciclagem, obtém-se
Oxirredução. O professor recomenda: Estude pelos seguintes livros/páginas sobre a oxirredução e faça os exercícios! 26/10/2011
 Oxirredução O professor recomenda: Estude pelos seguintes livros/páginas sobre a oxirredução e faça os exercícios! Shriver Ed 4 Cap.4 p.164-190 Atkins & Jones 1 ED Cap. 12 p. 603-635 Brown Cap. 20 p. 721-754
Oxirredução O professor recomenda: Estude pelos seguintes livros/páginas sobre a oxirredução e faça os exercícios! Shriver Ed 4 Cap.4 p.164-190 Atkins & Jones 1 ED Cap. 12 p. 603-635 Brown Cap. 20 p. 721-754
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 3ª Etapa 2014 Disciplina: QUÍMICA Série: 1ª Professora: Maria Luiza Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 3ª Etapa 2014 Disciplina: QUÍMICA Série: 1ª Professora: Maria Luiza Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
Química Oxi-Redeução Balanceamento de Equações Médio [20 Questões]
![Química Oxi-Redeução Balanceamento de Equações Médio [20 Questões] Química Oxi-Redeução Balanceamento de Equações Médio [20 Questões]](/thumbs/56/37976688.jpg) Química Oxi-Redeução Balanceamento de Equações Médio [20 Questões] 01 - (ITA SP) Uma camada escura é formada sobre objetos de prata expostos a uma atmosfera poluída contendo compostos de enxofre. Esta
Química Oxi-Redeução Balanceamento de Equações Médio [20 Questões] 01 - (ITA SP) Uma camada escura é formada sobre objetos de prata expostos a uma atmosfera poluída contendo compostos de enxofre. Esta
3ª Série / Vestibular. As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar que, na reação:
 3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
3ª Série / Vestibular 01. I _ 2SO 2(g) + O 2(g) 2SO 3(g) II _ SO 3(g) + H 2O(l) H 2SO 4(ag) As equações (I) e (II), acima, representam reações que podem ocorrer na formação do H 2SO 4. É correto afirmar
Lista de exercícios de Química Correção da Revisão para a 2ª Avaliação de Química: Pilhas
 Nome: Bimestre: 3º Ano / série: 2ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 1. Considere o esquema a seguir e responda: Lista de exercícios de Química
Nome: Bimestre: 3º Ano / série: 2ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 1. Considere o esquema a seguir e responda: Lista de exercícios de Química
Prova de Química Resolvida Segunda Etapa Vestibular UFMG 2011 Professor Rondinelle Gomes Pereira
 QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
ELETRODO OU SEMIPILHA:
 ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
Pág. 1. COMISSÃO PERMANENTE DE SELEÇÃO - COPESE PRÓ-REITORIA DE GRADUAÇÃO - PROGRAD CONCURSO VESTIBULAR 2009 2ª Fase PROVA DE QUÍMICA
 Questão 1: As bebidas alcoólicas contêm etanol e podem ser obtidas pela destilação do álcool (ex. whiskey e vodka) ou pela fermentação de uma variedade de produtos como frutas e outros vegetais (ex. vinho
Questão 1: As bebidas alcoólicas contêm etanol e podem ser obtidas pela destilação do álcool (ex. whiskey e vodka) ou pela fermentação de uma variedade de produtos como frutas e outros vegetais (ex. vinho
QUÍMICA. 3. (FCC BA) A reação abaixo pode ser classificada como endotérmica ou exotérmica? Justifique H2(g) + ½ O2(g) H2O(g) + 242kJ
 QUÍMICA Prof. Arthur LISTA DE EXERCÍCIOS - 2.8: TERMOQUÍMICA 1. (UFMG-MG) O gás natural (metano) é um combustível utilizado, em usinas termelétricas, na geração de eletricidade, a partir da energia liberada
QUÍMICA Prof. Arthur LISTA DE EXERCÍCIOS - 2.8: TERMOQUÍMICA 1. (UFMG-MG) O gás natural (metano) é um combustível utilizado, em usinas termelétricas, na geração de eletricidade, a partir da energia liberada
PROVA DE QUÍMICA 2 o BIMESTRE DE 2012 PROF. MARCOS
 PROVA DE QUÍMICA 2 o BIMESTRE DE 2012 PROF. MARCOS Boa Prova NOME N o 1 a SÉRIE A compreensão do enunciado faz parte da questão. Não faça perguntas ao examinador. A prova deve ser feita com caneta azul
PROVA DE QUÍMICA 2 o BIMESTRE DE 2012 PROF. MARCOS Boa Prova NOME N o 1 a SÉRIE A compreensão do enunciado faz parte da questão. Não faça perguntas ao examinador. A prova deve ser feita com caneta azul
ESTEQUIOMETRIA. Prof. João Neto
 ESTEQUIOMETRIA Prof. João Neto 1 Lei de Lavoisier Leis Ponderais Lei de Dalton Lei de Proust 2 Fórmula molecular Fórmula mínima Tipos de Fórmulas Fórmula eletrônica ou de Lewis Fórmula Centesimal Fórmula
ESTEQUIOMETRIA Prof. João Neto 1 Lei de Lavoisier Leis Ponderais Lei de Dalton Lei de Proust 2 Fórmula molecular Fórmula mínima Tipos de Fórmulas Fórmula eletrônica ou de Lewis Fórmula Centesimal Fórmula
LISTA DE EXERCÍCIOS 1º ANO
 Questão 1 Questão 2 Questão 3 Questão 4 Química GABARITO a) I) Fe 2 O 3 (s)+3h 2 SO 4 (aq) Fe 2 (SO 4 (aq)+3h 2 O II) 2Al(OH (s)+3h 2 SO 4 (aq) Al 2 (SO 4 (aq)+6h 2 O IIICaO(s)+2H 3 PO 4 (aq) Ca 3 (PO
Questão 1 Questão 2 Questão 3 Questão 4 Química GABARITO a) I) Fe 2 O 3 (s)+3h 2 SO 4 (aq) Fe 2 (SO 4 (aq)+3h 2 O II) 2Al(OH (s)+3h 2 SO 4 (aq) Al 2 (SO 4 (aq)+6h 2 O IIICaO(s)+2H 3 PO 4 (aq) Ca 3 (PO
X -2(3) X -2 x (4) X - 6 = -1 X 8 = -1 X = 5 X = 7
 2001 1. - Uma camada escura é formada sobre objetos de prata exposta a uma atmosfera poluída contendo compostos de enxofre. Esta camada pode ser removida quimicamente envolvendo os objetos em questão com
2001 1. - Uma camada escura é formada sobre objetos de prata exposta a uma atmosfera poluída contendo compostos de enxofre. Esta camada pode ser removida quimicamente envolvendo os objetos em questão com
Introdução. Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo.
 Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Química - Grupo J - Gabarito
 - Gabarito 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Informe a que volume deve ser diluído com água um litro de solução de um ácido fraco HA 0.10 M, de constante de ionização extremamente pequena (K
- Gabarito 1 a QUESTÃO: (2,0 pontos) Avaliador Revisor Informe a que volume deve ser diluído com água um litro de solução de um ácido fraco HA 0.10 M, de constante de ionização extremamente pequena (K
Ocorrência das Reações
 Ocorrência das Reações Efervescência Mudança de Cor Ocorrência das Reações Formação de Precipitado Reação x Equações Químicas Classificação 1. De acordo com a complexibilidade Adição ou síntese ou composição:
Ocorrência das Reações Efervescência Mudança de Cor Ocorrência das Reações Formação de Precipitado Reação x Equações Químicas Classificação 1. De acordo com a complexibilidade Adição ou síntese ou composição:
Final 8 de Maio de 2010
 Final 8 de Maio de 2010 Prova Teórica Nome:.... Escola:....... Pergunta Total Átomo, elemento e núcleo Contar os átomos Massa, moles e concentrações Equações Químicas Classificação teórica Classificação
Final 8 de Maio de 2010 Prova Teórica Nome:.... Escola:....... Pergunta Total Átomo, elemento e núcleo Contar os átomos Massa, moles e concentrações Equações Químicas Classificação teórica Classificação
A) Escreva a equação que representa a semi-reação de redução e seu respectivo potencial padrão.
 QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS. Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS
 As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS Em função dessas propriedades podemos agrupar as substâncias
As substâncias químicas podem ser agrupadas de acordo com suas PROPRIEDADES COMUNS Estas propriedades comuns são chamadas de PROPRIEDADES FUNCIONAIS Em função dessas propriedades podemos agrupar as substâncias
21814. (Ufg) Observando a tira, responda:
 17054. (Unesp) As baterias dos automóveis são cheias com solução aquosa de ácido sulfúrico. Sabendo-se que essa solução contém 38% de ácido sulfúrico em massa e densidade igual a 1,29g/cm, pergunta-se:
17054. (Unesp) As baterias dos automóveis são cheias com solução aquosa de ácido sulfúrico. Sabendo-se que essa solução contém 38% de ácido sulfúrico em massa e densidade igual a 1,29g/cm, pergunta-se:
Introdução. Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix
 Introdução Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix Introdução Conceitos de oxidação e redução 1 - Ganho ou perda de oxigênio
Introdução Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix Introdução Conceitos de oxidação e redução 1 - Ganho ou perda de oxigênio
Reações em Soluções Aquosas
 Reações em Soluções Aquosas Classificação Reações sem transferência de elétrons: Reações de precipitação; Reações de neutralização. Reações com transferência de elétrons: Reações de oxirredução. Reações
Reações em Soluções Aquosas Classificação Reações sem transferência de elétrons: Reações de precipitação; Reações de neutralização. Reações com transferência de elétrons: Reações de oxirredução. Reações
CONCEITOS MODERNOS DE ÁCIDOS E BASES
 CONCEITOS MODERNOS DE ÁCIDOS E BASES Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 01 Na reação segundo a equação: EXERCÍCIOS DE APLICAÇÃO 1 1 1 3 2 2 4 NH H O NH OH a) Qual o doador de
CONCEITOS MODERNOS DE ÁCIDOS E BASES Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 01 Na reação segundo a equação: EXERCÍCIOS DE APLICAÇÃO 1 1 1 3 2 2 4 NH H O NH OH a) Qual o doador de
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE
 LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
Ácido. Base. Classifique as substâncias abaixo. HClO 4 (aq) H + (aq) + ClO 4- (aq) NaOH(aq) Na + (aq) + OH - (aq)
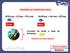 Classifique as substâncias abaixo HClO 4 (aq) H + (aq) + ClO 4- (aq) NaOH(aq) Na + (aq) + OH - (aq) Ácido Base Conceito de ácido e base de Arrhenius Restrito ao meio aquoso Classifique as substâncias abaixo
Classifique as substâncias abaixo HClO 4 (aq) H + (aq) + ClO 4- (aq) NaOH(aq) Na + (aq) + OH - (aq) Ácido Base Conceito de ácido e base de Arrhenius Restrito ao meio aquoso Classifique as substâncias abaixo
UFJF CONCURSO VESTIBULAR 2011-2 GABARITO DA PROVA DISCURSIVA DE QUÍMICA
 UFJF CNCURS VESTIBULAR 2011-2 GABARIT DA PRVA DISCURSIVA DE QUÍMICA Questão 1 Sabe-se que compostos constituídos por elementos do mesmo grupo na tabela periódica possuem algumas propriedades químicas semelhantes.
UFJF CNCURS VESTIBULAR 2011-2 GABARIT DA PRVA DISCURSIVA DE QUÍMICA Questão 1 Sabe-se que compostos constituídos por elementos do mesmo grupo na tabela periódica possuem algumas propriedades químicas semelhantes.
MECANISMOS BÁSICOS DE CORROSÃO
 Centro Universitário de Brasília Disciplina: Química Tecnológica Geral Professor: Edil Reis MECANISMOS BÁSICOS DE CORROSÃO No estudo dos processos corrosivos devem ser sempre consideradas as variáveis
Centro Universitário de Brasília Disciplina: Química Tecnológica Geral Professor: Edil Reis MECANISMOS BÁSICOS DE CORROSÃO No estudo dos processos corrosivos devem ser sempre consideradas as variáveis
Lista de exercícios sobre funções inorgânicas.
 Lista de exercícios sobre funções inorgânicas. 1. X é uma substância gasosa nas condições ambientes. Quando liquefeita, praticamente não conduz corrente elétrica, porém forma solução aquosa que conduz
Lista de exercícios sobre funções inorgânicas. 1. X é uma substância gasosa nas condições ambientes. Quando liquefeita, praticamente não conduz corrente elétrica, porém forma solução aquosa que conduz
NOX EXERCÍCIOS QUÍMICA PROF- LEONARDO. 01)Quais são os números de oxidação do iodo nas substâncias l 2, Nal, NalO 4 e Al I 3?
 NOX EXERCÍCIOS QUÍMICA PROF- LEONARDO 01)Quais são os números de oxidação do iodo nas substâncias l 2, Nal, NalO 4 e Al I 3? 02. O número de oxidação do manganês no permanganato de potássio (KMnO4) é:
NOX EXERCÍCIOS QUÍMICA PROF- LEONARDO 01)Quais são os números de oxidação do iodo nas substâncias l 2, Nal, NalO 4 e Al I 3? 02. O número de oxidação do manganês no permanganato de potássio (KMnO4) é:
Aluno(a): Instituição de Ensino: Município: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO DAS QUESTÕES É OBRIGATÓRIO
 IX Olimpíada Capixaba de Química 2011 Prova do Grupo I 1 a série do ensino médio Fase 01 Aluno(a): Instituição de Ensino: Município: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO
IX Olimpíada Capixaba de Química 2011 Prova do Grupo I 1 a série do ensino médio Fase 01 Aluno(a): Instituição de Ensino: Município: Coordenador da Instituição de Ensino: ATENÇÃO: O DESENVOLVIMENTO TEÓRICO
