Isolamento do Limoneno
|
|
|
- Lara Monteiro Farinha
- 7 Há anos
- Visualizações:
Transcrição
1 Isolamento do Limoneno 01) Destilação por arraste à vapor, destilar todo material orgânico (até que se destile apenas água) 02) Para assegurar que o destilado apresente uma única fase, coletar algumas gotas do destilado em tubo de ensaio, se for observado duas fases, continue destilando. Transferir 30 ml de óleo de laranja para balão de 250 ml 03) Adicionar 30ml de n-hexano 04) Transferir para funil de separação 05) Lavar o frasco com pequenas porções de n-hexano e adicionar ao funil. 06) Agitar o funil cuidadosamente, para separação das fases Destilado ( 2 fases) Fase aquosa H 2 O, limoneno e traços de n-hexano 07) Extrair com 20 ml de n- hexano, coletando no erlenmeyer (A), fase orgânica. Fase Orgânica (Limoneno, n-hexano e traços de H 2 0) Recolher no Erlenmeyer (A)
2 Fase Orgânica (Limoneno, n-hexano e traços de H 2 O) Fase aquosa H 2 O, limonemo e traços de n-hexano Fase Orgânica contida no Erlenmeyer (A) com as três extrações. (Limineno, n-hexano e traços de H 2 0) Repetir procedimento 07 08) Adicionar agente secante (Na 2 SO 4 ) no erlenmeyer (A). 09) Guardar em geladeira o erlenmeyer arrolhado até a próxima aula.
3 SEMINÁRIO DE QUÍMIA ORGÂNIA EXPERIMENTAL EXTRAÇÃO E PURIFIAÇÃO DO LIMONENO Evaldo ésar de Souza Mota Sandro Moreno Barrionuevo Milena Elias Teixeira Ana Paula Álvares Ricardo Martini Allan Hollandy Hollanda
4 I-OBJETIVO: Extrair o Limoneno do óleo de laranja e purificá-lo através da destilação fracionada. II-INTRODUÇÃO: Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica que tem servido à humanidade como farmacologia, ingredientes de perfumes, preservativos, temperos e várias outras utilidades. Os componentes voláteis são geralmente isolados de plantas por destilação à vapor a pressão atmosférica. A planta é normalmente dividida finamente ou misturada para liberar os componentes voláteis de sua estrutura celular e o vapor é então introduzido para condensar os componentes orgânicos voláteis com a água. Se a fonte é facilmente penetrada, como é o caso com folhas, pétalas de flor e brotos, gramas e ervas, a destilação à vapor é usada sem pretexto de materiais vegetais. A mistura de componentes orgânicos voláteis são obtidos de plantas e são imiscíveis em água e conhecido como essências. Os odores das plantas é devido à essências. Essências têm sido isoladas de uma larga variedade de plantas, mas constituída somente de uma pequena porcentagem da composição total da planta. Óleo de alcaravia, por exemplo, é obtido das sementes de alcaravia, mas constituem somente 3 a 7% do peso total da semente; óleo de rosa é obtido somente 0.04% de rendimento das pétalas e brotos de rosas. Ambos, óleo de rosa e alcaravia, são usados em ingredientes de perfume. Os maiores constituintes das essências são os terpenos e outros derivados oxigenados. Terpenos são estruturas compostas de unidades de isopreno combinado na forma de head-to-tail. Limoneno, o qual é mais largamente distribuído cíclico terpeno das plantas, é o principal ingrediente do óleo de laranja (90 a 95%) e é achado no óleo de limão, óleo de alcaravia, e em muitas outras essências. FÓRMULA DO LIMONENO:
5 III-TÉNIAS UTILIZADAS NA EXPERIÊNIA: Destilação é o processo de vaporização de uma substância, condensação de vapor e coleta do condensado em outro recipiente. Esta técnica é usada para a separação de uma mistura quando os componentes têm pontos de ebulição diferentes. Este é o principal método de purificação de um líquido. Existem quatro tipos de métodos de destilação: destilação simples, destilação à vácuo ( destilação à pressão reduzida), destilação fracionada e destilação por arraste à vapor. Na experiência de extração e purificação do limoneno a partir do óleo de laranja, serão utilizadas as técnicas de destilação fracionada e por arraste à vapor. PONTO DE EBULIÇÃO: Quando um líquido é aquecido, a pressão de vapor do líquido aumenta até se igualar a pressão aplicada ( geralmente à pressão atmosférica). Nesse ponto, o líquido entrará em ebulição. O ponto normal de ebulição é medido à 760 mmhg (1 atm). Quando a pressão aplicada é menor que 1 atm, o vapor de pressão necessário para a ebulição também é menor, e o líquido entra em ebulição numa temperatura menor. O ponto de ebulição é alterado de acordo com a pressão, por isso é importante que se conheça a pressão barométrica, se a destilação for realizada num nível significativamente acima ou abaixo do nível do mar. Devido à temperatura observada durante a destilação, pode ser diferente da temperatura do ponto de ebulição do líquido, deve-se efetuar a correção do ponto de ebulição, através da seguinte equação: ΔT = (760 Pobs)( Tobs + 273) DESTILAÇÃO FRAIONADA: Evidentemente, por repetidas destilações, combinando e recombinando destilações fracionadas e condensadas, poderá separar uma mistura de benzeno e tolueno em seus componentes puros. ontudo, o destilado poderá ser um componente de um ponto de ebulição baixo, benzeno (puro), ou um componente de ponto de ebulição elevado, o tolueno. A destilação fracionada é simplesmente uma técnica para realizar uma série completa destas pequenas separações em uma operação. Em princípio, uma coluna de destilação fracionada proporciona uma grande superfície para o intercâmbio de calor, nas condições de equilíbrio, entre o vapor ascendente e o condensado descendente. Isto possibilita uma série completa de evaporações e condensações parciais ao longo da coluna.
6 DESTILAÇÃO POR ARRASTE À VAPOR: Fundamentos: Esta destilação é uma técnica para a separação de substâncias insolúveis em água e ligeiramente voláteis de outros produtos não voláteis, misturados à elas. O arraste à vapor possibilita a purificação adequada de muitas substâncias com pontos de ebulição elevados, frente à destilações de baixa temperatura. Esta técnica é particularmente útil quando a substância em questão ferve acima de 100 graus, na pressão atmosférica, e se decompõe em um ponto de ebulição abaixo deste. Nesses casos, substitui para a destilação à vácuo. ontudo, pode-se dizer que a destilação de uma mistura de líquidos imiscíveis em quantidades relativas em peso dos líquidos que escorrem no coletor, são diretamente proporcionais : 1- Às tensões de vapor dos líquidos à temperatura de destilação; 2- À seus pesos moleculares. Logo, a mistura se destilará a uma temperatura constante, contanto que exista, pelo menos, cada um dos componentes. Isto constitue a base de uma purificação e de uma separação de substâncias por arraste à vapor. Aplicações: Para que uma substância insolúvel destile em quantidade apreciável, deverá ter uma tensão de vapor entre 5-10 milímetros a 100 graus. A destilação em corrente de produtos resinosos também é muito útil na separação de compostos orgânicos facilmente voláteis de : 1- Misturas aquosas que têm sais inorgânicos; 2- Outros compostos orgânicos que não são, apreciavelmente, voláteis em arraste à vapor. Se uma destilação por arraste à vapor, em fase insolúvel em água, está formada por dois componentes, haverá duas fases distintas (uma aquosa e uma orgânica), que destilarão segundo os princípios da destilação por arraste à vapor, numa relação molar das duas fases no destilado e na mesma que existe entre as tensões de vapor das duas fases. Então, os componentes da fase orgânica destilam, respectivamente, segundo os princípios da destilação ordinária. Assim, o destilado é mais rico que o resíduo do componente mais volátil. A maioria dos compostos orgânicos que se arrastam à vapor não são completamente insolúveis em água, especialmente na temperatura de destilação. Isto diminui a eficácia calculada do processo. A adição de cloreto de sódio para saturar a fase aquosa, pode diminuir a solubilidade do composto orgânico na fase aquosa e diminuir, também, a tensão de vapor respectiva à tensão de vapor da fase orgânica.
7 IV-PARTE EXPERIMENTAL: UIDADOS A TOMAR OM AS SUBSTÂNIAS: n-hexano: pode provocar sintomas após excessível exposição como: delírios, náuseas, dor de cabeça, fraquezas musculares, irritação nos olhos e nariz, dermatites, pneumonia química, tonturas. Limoneno: irrita a pele, é um sensibilizador e é explosivo. PRIMEIROS SOORROS: Pulmões: Remova da exposição, descanse e mantenha aquecido. Pele: Encharcar a pele com água e depois lave com sabão. Remover as roupas contaminadas e arejá-las antes da reutilização. Todavia se o contato for muito pronunciado procure atendimento médico. Boca: Lave vigorosamente com água. Procure atendimento médico. Olhos: Irrigar os olhos minunciosamente com água. Procurar cuidados médicos nos casos severos. DADOS: Tabela 1: onstantes das substâncias envolvidas na reação. Substância Fórmula Peso molecular (g/mol) Ponto de ebulição (º) Ponto de fusão (º) Densidade (g/cm 3 ) Solubilidade em água n-hexano 6 H 14 86, / -95 0,660 Insolúvel Sulfato de Sódio anidro Na 2 SO 4 142, ,7 Solúvel limoneno 10 H ,24 175, Insolúvel 176,5 água H 2 O 18, ,00 Solvente universal
8 FLUXOGRAMA DO PROEDIMENTO: A) Destilação por arraste a vapor ( isolamento) : Transferir 30 ml de óleo de laranja para balão de 250 ml Montar o sistema de arraste a vapor Destilar todo o material orgânico (até que se destile apenas água) oletar gotas do destilado em tubo de ensaio. Se for observado duas fases continue destilando.
9 B ) Destilação Fracionada ( purificação) : Montar um sistema de destilação fracionada Ligar a manta elétrica e elevar a temperatura gradualmente quando a mistura entrar em ebulição Após o início, manter a temperatura constante Anotar a temperatura quando a primeira gota for coletada e a cada 2 ml(primeira fração) Ler a temperatura a cada 10 gotas
10 DISUSSÃO: Figura 1:Esboço do gráfico T x V. TEMPERATURA (º) fração 2 fração 3 fração 1 VOLUME (ml) ANÁLISE: Experiência: Após a destilação por arraste a vapor é adicionado o n-hexano pois o limoneno é mais solúvel neste do que em água. Portanto ao adicionar o n- hexano obtém-se maior quantidade de limoneno já isolado. Gráfico: Observa-se, pelo gráfico, que na primeira fração a temperatura se mantém constante pois têm-se apenas um componente ( n-hexano ) e este tem temperatura de ebulição por volta de 69º e é menor que a do limoneno. A fração 2 apresenta uma grande variação de temperatura por se tratar de uma mistura. Na terceira fração a temperatura se mantém constante pois trata-se do limoneno que tem temperatura de ebulição por volta de 175º.
11 BIBLIOGRAFIA: 1.Brewster, R.O.; Vanderwef,.: McEven, W.E. Utilized Experiments in Organic hemistry, 4th edition, New York, D. Van Nostrand, Pavia, D.L.; Lampman, G.M.; Jr. Kriz, G.S. Introduction to Laboratory Techniques, 2nd edition, Philadelphia, Saunders ollege Publishing, Doyle, M.P.; Mungall, W.S. Experimental Organic hemistry, New York, John Wiley & Sons, Inc
12 I-Introdução Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis das plantas denominadas óleos essenciais, são responsáveis por suas essências e aromas, muitos dos quais apreciados desde a antiguidade. Os óleos essenciais são usados principalmente devido a seus odores e aroma agradáveis em perfumes, e como aromatizantes em alimentos. Podem ser empregados também como medicamentos (cânfora e eucalipto), como repelentes de insetos (citronela) e por sua ação antibacteriana e anti-fungicida. Os componentes voláteis são geralmente isolados de uma planta por destilação a vapor sob pressão atmosférica. A planta é moída ou triturada para liberação de seus componentes voláteis de sua estrutura celular. Os óleos essenciais (imiscíveis em água) co-destilam com a água à medida que o vapor é introduzido no sistema. A técnica de destilação por arraste a vapor permite separar os componentes voláteis de materiais não voláteis, a uma temperatura abaixo de 100 0, o que oferece o meio de isolamento de óleos essenciais, sem o risco de decompô-los termicamente. Os óleos essenciais tem sido isolados de uma grande variedade de plantas, mas constituem somente uma pequena porcentagem da constituição total da planta. O óleos de rosa, por exemplo, é obtido em apenas 0,04% do peso das pétalas de rosas. O óleo de laranja, constitui não mais do que 1% dos pesos das cascas de laranjas (variedade valença). Os principais constituintes dos óleos essenciais são os terpenos e seus derivados oxigenados. Pode-se imaginar os terpenos como contituídos por duas ou mais unidades 5, conhecidas como unidades isoprënicas, combinadas cabeça-cauda. OU UNIDADE ISOPRÊNIA (ABEÇA) (AUDA) (ABEÇA) (AUDA)
13 Usando linhas tracejadas para separar as unidades isoprênicas, pode-se ver que o limoneno tem duas dessas unidades: Uma forma enantiomérica do limoneno é responsável pelo odor da laranja e o outro enantiômero pelo odor do limão. II- Técnicas utilizadas na experiência. Destilação é o processo de vaporização de uma substância, condensação de vapor e coleta do condensado em outro recipiente. Esta técnica é usada para separação de uma mistura quando os componentes tem pontos de ebulição diferentes. Este é o principal método de purificação de um líquido.existem quatro tipos de métodos de destilação: simples, à vácuo (destilação à pressão reduzida), fracionada e por arraste a vapor. Na experiência de extração e purificação do limoneno a partir do óleo de laranja, serão utilizadas as técnicas de destilação fracionada e arraste a vapor. Ponto de ebulição Quando um líquido é aquecido, a pressão de vapor do líquido aumenta até se igualar a pressão aplicada (geralmente a pressão atmosférica). Neste ponto o líquido entrará em ebulição. O ponto normal de ebulição é medido a 760mm de Hg (1 atmosfera). Quando a pressão aplicada é menor que uma atmosfera, o vapor de pressão necessário para a ebulição também é menor, e o líquido entra em ebulição numa temperatura menor. O ponto de ebulição é alterado de acordo com a pressão, por isso é importante que se conheça a pressão barométrica, se a destilação for realizada num nível significativamente acima ou abaixo do nível do mar. Devido a temperatura observada durante a destilação, pode ser diferente da temperatura do ponto de ebulição do líquido, deve se efetuar a correção do ponto de ebulição, atavés da seguinte equação:
14 ΔT= 0,00012 (760-Pobs) (Tobs +273) Destilação Fracionada Utilizada na separação de líquidos miscíveis entre si, mesmo aqueles de pontos de ebulição próximos. Para entendermos a destilação fracionada utilizaremos o diagrama da composição-temperatura do sistema benzeno-tolueno. (Figura 1) Quando aquecemos uma solução de 20 moles% de benzeno (80 moles% de tolueno). A 101,6 0 corresponde ao ponto L 1, o líquido entra em ebulição. A composição do vapor resultante desta ebulição, nesta temperatura, é de 38 moles% de benzeno (62 moles% de tolueno), ponto V 1, portanto consideravelmente mais rico em benzeno que a solução inicial. Portanto jamais poderia separar totalmente, através de uma destilação simples, uma mistura molar de 20% de benzeno e 80% de tolueno. Porém, se condensássemos estes vapores e voltássemos a repetir a destilação, teríamos o líquido correspondente ao ponto L 2 e cujos vapores corresponderiam ao ponto V 2. Se repetíssemos a condensação destes vapores, teríamos progressivamente mais benzeno e menos tolueno até se chegar a completa separação das duas substãncias. Imaginemos, agora, um dispositivo que permita ao aparelho repetir sucessivamente as destilações, de modo que os vapores contendo uma mistura dos líquidos componentes do produto inicial voltem a ser redestilados, e que somente seja permitido sair do aparelho, a uma dada temperatura, o líquido mais volátil e puro- teremos assim um aparelho de destilação fracionada. Este aparelho é o mesmo da destilação simples com adaptação de um dispositivo chamado coluna de fracionamento, disposto entre o condensador e o balão que, neste caso, é simples não possuindo na sua parte superior, o tubo de desprendimento. A coluna de fracionamento consta de um tubo longo, adaptado pela extremidade inferior ao balão, contendo na extremidade superior um tubo de desprendimento lateral que deverá ser ajustado ao condensador. Pela abertura superior é introduzido um termômetro, cujo bulbo deverá ficar à altura da saída do tubo de desprendimento. Internamente ao tubo longo, colocam-se pequenos cilindros de vidro ou porcelana, dispostos irregularmente, que age como pequenos condensadores de refluxo para mistura de vapores. Há outros tipos de colunas de fracionamento, Vigreux (fig. B) que tem uma série de fendas para aumentar a superfície interna; a de Yung (fig. ) que possue uma espiral interna de vidro ou metal enrolado em torno de
15 uma haste, e finalmente a coluna de pratos (fig. D) que contém pequenas prateleiras funcionando como condensadores de refluxo para a mistura de vapores. Destilação por arraste a vapor Empregada para destilar substâncias que se decompõem nas proximidades de seus pontos de ebulição e que são insolúveis em água ou nos seus vapores de arraste. Esta operação baseia-se no fato de que, numa mistura de líquidos imiscíveis, o ponto de ebulição será a temperatura na qual a soma das pressões parciais dos vapores é igual a da atmosfera, o que constitui uma decorrência da lei das pressões parciais de Dalton. Se, em geral, o arraste se faz com vapor de água, a destilação, a pressão atmosférica, resultará na separação do componente de ponto de ebulição mais alto, a uma temperatura inferior a Por outro lado, quando uma mistura de dois líquidos imiscíveis é destilada, o ponto de ebulição da mistura permanece constante até que um dos componentes tenha sido separado, já que a pressão total do vapor independe das quantidades relativas dos componentes. O ponto de ebulição, a partir daí, eleva-se rapidamente, até atingir o do líquido remanescente. O vapor que se separa de tal mistura contém os componentes na mesma proporção, que suas pressões de vapor relativas. Por meio de cálculos simples e aplicando as leis dos gases, podemos estabelecer a proporção dos vapores em função de seus pesos moleculares e das suas pressões parciais. P T = P A + P B B (1) E a composição do vapor: Na Pa = (2) Nb Pb onde: Na e Nb são números de moles das substâncias da fase de vapor. omo: Wa Wb Na = enb = Ma Nb
16 Onde: W: massa em gramas da substância em dado volume da fase de vapor M: massa molecular da substância Então: Wa Wb = MaNa MbNb = MaPa (3) MbPb Ou seja, as massas relativas de dois componentes de uma mistura de fase de vapor são idênticas as massas relativas do destilado, isto é, as massas dos dois líquidos sendo recolhidos num recipiente são diretamente proporcionais as suas pressões de vapor e a suas massas moleculares. A equação (3) indica que, quanto menor MaPa tanto maior é o valor de Wb e daí a grande aplicação da destilação de arraste a vapor nos processos industriais para separação de compostos de elevada massa molecular e de baixa pressão de vapor O aparelho para destilação com arraste de vapor (fig.2) de um balão de destilação comum, no qual se introduz um tubo longo de segurança. O tubo de desprendimento lateral se comunica por uma tubulação de vidro, em forma de L a um balão de duas bocas. Este, por sua vez, se conecta a um refrigerante de Leibig. O tubo de segurança destina-se a manter o equilíbrio da pressão interna do sistema. No balão de destilação coloca-se o líquido que deverá fornecer vapor para arraste, geralmente água. O aquecimento deste balão (contendo pedras de ebulição em seu interior) pode ser feito por bico de Búnsen ou por aquecedor elétrico. No balão intermediário de duas saídas, coloca-se a mistura de líquidos, da qual se vai destilar um ou mais componentes. O aquecimento deste deverá ser feito apenas inicialmente, até que se estabeleça o equilíbrio com a temperatura do vapor oriundo do primeiro balão, voltar a aquecê-lo de modo a manter a continuidade da destilação Nota: 1) Se quiser controlar a temperatura, substituir o balão de 2 bocas por um de 3 bocas e colocar o termômetro na boca intermediária.
17 TEMPERATURA ( º) FRAÇÃO 1 FRAÇÃO 2 FRAÇÃO 3 VOLUME DESTILADO (ml) Figura 1: Esboço do gráfico da temperatura pelo volume destilado para a destilação fracionada.
Isolamento de compostos orgânicos voláteis de fontes naturais
 I-Introdução Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis das plantas denominadas óleos essenciais, são responsáveis por suas essências e aromas, muitos dos quais
I-Introdução Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis das plantas denominadas óleos essenciais, são responsáveis por suas essências e aromas, muitos dos quais
Isolamento de compostos orgânicos voláteis de fontes naturais
 Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
DESTILAÇÃO Lei de Raoult
 DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
DESTILAÇÃO Operação que consiste na separação de líquidos de suas eventuais misturas, por passagem de vapor e posterior condensação com retorno ao estado líquido, com auxílio de calor e/ou por redução
Isolamento de compostos orgânicos voláteis de fontes naturais
 Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
Parte II. Meneah Renata Talita
 Extração e Purificação do Limoneno Parte II Meneah Renata Talita Objetivo da prática Isolar e Purificar o Limoneno a partir de uma fase orgânica contendo n-hexano, limoneno, traços de substâncias voláteis
Extração e Purificação do Limoneno Parte II Meneah Renata Talita Objetivo da prática Isolar e Purificar o Limoneno a partir de uma fase orgânica contendo n-hexano, limoneno, traços de substâncias voláteis
(8) Isolamento e Purificação do Limoneno II
 UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP (8) Isolamento e Purificação do Limoneno II Discentes: Grupo XIX Andrezza Fernandes Chagas Júlia Pinto Piccoli Profº. Dr. José Eduardo
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP (8) Isolamento e Purificação do Limoneno II Discentes: Grupo XIX Andrezza Fernandes Chagas Júlia Pinto Piccoli Profº. Dr. José Eduardo
Extração e Purificação do Limoneno. Parte arte I Ana Carolina Faria Barrozo Daniele Bueno dos Santos
 Extração e Purificação do Limoneno Parte arte I Ana arolina Faria Barrozo Daniele Bueno dos Santos 1 Apresentação Óleos essenciais Terpenos Limoneno Destilação por arraste de vapor Extração com solvente
Extração e Purificação do Limoneno Parte arte I Ana arolina Faria Barrozo Daniele Bueno dos Santos 1 Apresentação Óleos essenciais Terpenos Limoneno Destilação por arraste de vapor Extração com solvente
Isolamento de compostos orgânicos voláteis de fontes naturais
 Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
Isolamento de compostos orgânicos voláteis de fontes naturais Os componentes voláteis de plantas constituem uma enorme riqueza da Química Orgânica. Eles são utilizados na farmacologia, ingredientes de
Extração e Purificação do Limoneno Parte II
 Confira o Título do experimento na apostila. Extração e Purificação do Limoneno Parte II Docentes: Prof. Dr. José Eduardo de Oliveira Prof. Dr. Humberto M. S. Milagre Prof.ª Dr.ª Isabele R. Nascimento
Confira o Título do experimento na apostila. Extração e Purificação do Limoneno Parte II Docentes: Prof. Dr. José Eduardo de Oliveira Prof. Dr. Humberto M. S. Milagre Prof.ª Dr.ª Isabele R. Nascimento
Destilação fracionada. Destilação por arraste à vapor. Extração
 ISOLAMENTO DE COMPOSTOS ORGÂNICOS VOLÁTEIS DE FONTES NATURAIS OBJETIVO isolar e purificar o limoneno do óleo de laranja TÉCNICAS UTILIZADAS Destilação fracionada Extração Limoneno CH3 H2C CH3 1-metil-4
ISOLAMENTO DE COMPOSTOS ORGÂNICOS VOLÁTEIS DE FONTES NATURAIS OBJETIVO isolar e purificar o limoneno do óleo de laranja TÉCNICAS UTILIZADAS Destilação fracionada Extração Limoneno CH3 H2C CH3 1-metil-4
Extração do Limoneno. Integrantes do grupo: Diego Souza, Jefferson Honorio, Marcelo Tangerina
 Extração do Limoneno Integrantes do grupo: Diego Souza, Jefferson Honorio, Marcelo Tangerina Quem é o Limoneno? O Limoneno ( IUPAC: : 1-metil1 metil-4-isopropenilciclohex- 1-eno ) é uma substância química:
Extração do Limoneno Integrantes do grupo: Diego Souza, Jefferson Honorio, Marcelo Tangerina Quem é o Limoneno? O Limoneno ( IUPAC: : 1-metil1 metil-4-isopropenilciclohex- 1-eno ) é uma substância química:
Propriedades dos reagentes e solventes utilizados
 DESTILAÇÃO POR ARRASTE À VAPOR Propriedades dos reagentes e solventes utilizados Densidade (g/cm 3 ) nomenclatura fórmula Mol (g/mol) pf (ºC) pe (ºC) toxidade solubilidade Propriedades físicas 0,8402 1-metil-4
DESTILAÇÃO POR ARRASTE À VAPOR Propriedades dos reagentes e solventes utilizados Densidade (g/cm 3 ) nomenclatura fórmula Mol (g/mol) pf (ºC) pe (ºC) toxidade solubilidade Propriedades físicas 0,8402 1-metil-4
Parte II. Meneah Renata Talita
 Extração e Purificação do Limoneno Parte II Meneah Renata Talita Objetivo da prática Isolar e Purificar o Limoneno a partir de uma fase orgânica contendo n-hexano, limoneno, traços de substâncias voláteis
Extração e Purificação do Limoneno Parte II Meneah Renata Talita Objetivo da prática Isolar e Purificar o Limoneno a partir de uma fase orgânica contendo n-hexano, limoneno, traços de substâncias voláteis
Seminário de Química Orgânica Experimental n 7. Destilação Fracionada do Sistema Limoneno - Hexano
 Seminário de Química Orgânica Experimental n 7 Destilação Fracionada do Sistema Limoneno - Hexano Responsáveis: Prof. Dr. José Eduardo de Oliveira (docente) Profª. Amanda Coelho Danuello (docente) Rafael
Seminário de Química Orgânica Experimental n 7 Destilação Fracionada do Sistema Limoneno - Hexano Responsáveis: Prof. Dr. José Eduardo de Oliveira (docente) Profª. Amanda Coelho Danuello (docente) Rafael
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP
 UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 7 -Isolamento e Purificação do Limoneno I André Marques de Andrade Guilherme Condutta Júlio Cesar de Bianchi Sobrinho Murilo de Souza
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 7 -Isolamento e Purificação do Limoneno I André Marques de Andrade Guilherme Condutta Júlio Cesar de Bianchi Sobrinho Murilo de Souza
Extração e Purificação do Limoneno Parte II
 Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Seminário de Química Orgânica Experimental n 7. Destilação Fracionada do Sistema Limoneno - Hexano
 Seminário de Química Orgânica Experimental n 7 Destilação Fracionada do Sistema Limoneno - Hexano Responsáveis: Prof. Dr. José Eduardo de Oliveira (docente) Profª. Amanda Coelho Danuello (docente) Rafael
Seminário de Química Orgânica Experimental n 7 Destilação Fracionada do Sistema Limoneno - Hexano Responsáveis: Prof. Dr. José Eduardo de Oliveira (docente) Profª. Amanda Coelho Danuello (docente) Rafael
Preparação do cloreto de t-butila. Carina de Freitas Vellosa Daiane Cristina Romanini
 Preparação do cloreto de t-butila Carina de Freitas Vellosa Daiane Cristina Romanini Técnicas e Materiais Utilizados Funil de separação: serve para extrair duas soluções imiscíveis. A fase orgânica pode
Preparação do cloreto de t-butila Carina de Freitas Vellosa Daiane Cristina Romanini Técnicas e Materiais Utilizados Funil de separação: serve para extrair duas soluções imiscíveis. A fase orgânica pode
EXTRAÇÃO E PURIFICAÇÃO DO LIMONENO (PARTE II) Andressa Baruco Coelho Susel Taís Soares
 EXTRAÇÃO E PURIFICAÇÃO DO LIMONENO (PARTE II) Andressa Baruco Coelho Susel Taís Soares DESTILAÇÃO : Simples Por arraste a vapor `A pressão reduzida Fracionada DESTILAÇÃO `A PRESSÃO REDUZIDA Destina-se
EXTRAÇÃO E PURIFICAÇÃO DO LIMONENO (PARTE II) Andressa Baruco Coelho Susel Taís Soares DESTILAÇÃO : Simples Por arraste a vapor `A pressão reduzida Fracionada DESTILAÇÃO `A PRESSÃO REDUZIDA Destina-se
Extração e Purificação do Limoneno Parte II
 Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Extração e Purificação do Limoneno Parte II Alan Cesar Pilon Andrey Pinheiro Técnicas para extração e purificação do Limoneno Extração com Solvente Destilação por arraste de vapor Destilação Fracionada
Prof. Dr. José Eduardo de Oliveira Adriana Teixeira Machado Marcela Dias da Silva Matheus Gibbin Zanzini
 Prof. Dr. José Eduardo de Oliveira Adriana Teixeira Machado Marcela Dias da Silva Matheus Gibbin Zanzini Filtração Fonte de aquecimento Destilação Correção do ponto de ebulição OBJETIVO: Remover impurezas
Prof. Dr. José Eduardo de Oliveira Adriana Teixeira Machado Marcela Dias da Silva Matheus Gibbin Zanzini Filtração Fonte de aquecimento Destilação Correção do ponto de ebulição OBJETIVO: Remover impurezas
Destilação fracionada. Destilação por arraste à vapor. Extração
 ISOLAMENTO DE COMPOSTOS ORGÂNICOS VOLÁTEIS DE FONTES NATURAIS OBJETIVO isolar e purificar o limoneno do óleo de laranja TÉCNICAS UTILIZADAS Destilação fracionada Extração Limoneno CH3 H2C CH3 1-metil-4
ISOLAMENTO DE COMPOSTOS ORGÂNICOS VOLÁTEIS DE FONTES NATURAIS OBJETIVO isolar e purificar o limoneno do óleo de laranja TÉCNICAS UTILIZADAS Destilação fracionada Extração Limoneno CH3 H2C CH3 1-metil-4
Seminário de Química Orgânica Experimental. Destilação Fracionada do Sistema Limoneno - Hexano
 Seminário de Química Orgânica Experimental Destilação Fracionada do Sistema Limoneno - Hexano Docente: Prof. Dr. José Eduardo de Oliveira Discentes: Bruno Diegolo Gerson Matiuzzi Josiel José Limoneno O
Seminário de Química Orgânica Experimental Destilação Fracionada do Sistema Limoneno - Hexano Docente: Prof. Dr. José Eduardo de Oliveira Discentes: Bruno Diegolo Gerson Matiuzzi Josiel José Limoneno O
8-Extração e Purificação do Limoneno II
 Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 8-Extração e Purificação do Limoneno II
Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 8-Extração e Purificação do Limoneno II
Química Orgânica Experimental
 Química Orgânica Experimental Docentes: Alunos: -Prof. Dr. José Eduardo de Oliveira -Nicole Savioli Scaravelli -Profª. Drª. Isabele Rodrigues -Murilo Pinese Nascimento -Prof. Dr. Humberto Marcio Santos
Química Orgânica Experimental Docentes: Alunos: -Prof. Dr. José Eduardo de Oliveira -Nicole Savioli Scaravelli -Profª. Drª. Isabele Rodrigues -Murilo Pinese Nascimento -Prof. Dr. Humberto Marcio Santos
EXTRAÇÃO DE PRINCÍPIOS DE FONTES NATURAIS DANIEL THOMAZ WEVERTON CAMPOS NOZELA
 EXTRAÇÃO DE PRINCÍPIOS DE FONTES NATURAIS DANIEL THOMAZ WEVERTON CAMPOS NOZELA OBJETIVO: Extração e purificação do limoneno INTRODUÇÃO : Sabe-se desde a antiguidade que os constituintes odoríferos de uma
EXTRAÇÃO DE PRINCÍPIOS DE FONTES NATURAIS DANIEL THOMAZ WEVERTON CAMPOS NOZELA OBJETIVO: Extração e purificação do limoneno INTRODUÇÃO : Sabe-se desde a antiguidade que os constituintes odoríferos de uma
EXPERIMENTOS DE QUIMICA ORGANICA I(QUI 127, QUI 186 E QUI 214) EXPERIMENTO 7 TÉCNICAS DE EXTRAÇÃO
 EXPERIMENTO 7 TÉCNICAS DE EXTRAÇÃO 1.1. Fundamentação teórica A extração é um processo de separação de compostos que consiste em transferir uma substância da fase na qual essa se encontra (dissolvida ou
EXPERIMENTO 7 TÉCNICAS DE EXTRAÇÃO 1.1. Fundamentação teórica A extração é um processo de separação de compostos que consiste em transferir uma substância da fase na qual essa se encontra (dissolvida ou
Destilação Fracionada do Sistema Limoneno-Hexano
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Instituto de Química do Campus de Araraquara Destilação Fracionada do Sistema Limoneno-Hexano Docentes: Prof. Dr. José Eduardo de Oliveira Profa.
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Instituto de Química do Campus de Araraquara Destilação Fracionada do Sistema Limoneno-Hexano Docentes: Prof. Dr. José Eduardo de Oliveira Profa.
Destilação Fracionada e Misturas Azeotrópicas
 1. Introdução Destilação Fracionada e Misturas Azeotrópicas O ponto de ebulição normal de uma mistura binária líquida é a temperatura na qual a pressão de vapor total da mistura é igual a 1 atm. Ou seja,
1. Introdução Destilação Fracionada e Misturas Azeotrópicas O ponto de ebulição normal de uma mistura binária líquida é a temperatura na qual a pressão de vapor total da mistura é igual a 1 atm. Ou seja,
Destilação Fracionada e Misturas Azeotrópicas
 1. Introdução Destilação Fracionada e Misturas Azeotrópicas O ponto de ebulição normal de uma mistura binária líquida é a temperatura na qual a pressão de vapor total da mistura é igual a 1 atm. Ou seja,
1. Introdução Destilação Fracionada e Misturas Azeotrópicas O ponto de ebulição normal de uma mistura binária líquida é a temperatura na qual a pressão de vapor total da mistura é igual a 1 atm. Ou seja,
PREPARAÇÃO E PURIFICAÇÃO DO ACETATO DE ISOPENTILA. Daniela Gonçalves Dias Jeniffer Biin Huoy Lin Renato Oyadomari Abe
 PREPARAÇÃO E PURIFICAÇÃO DO ACETATO DE ISOPENTILA Daniela Gonçalves Dias Jeniffer Biin Huoy Lin Renato Oyadomari Abe Reação de Esterificação Os ácidos carboxílicos reagem com álcoois produzindo ésteres
PREPARAÇÃO E PURIFICAÇÃO DO ACETATO DE ISOPENTILA Daniela Gonçalves Dias Jeniffer Biin Huoy Lin Renato Oyadomari Abe Reação de Esterificação Os ácidos carboxílicos reagem com álcoois produzindo ésteres
PURIFICAÇÃO DO ACETATO DE ISOPENTILA (PARTE 2)
 PURIFICAÇÃO DO ACETATO DE ISOPENTILA (PARTE 2) Docentes: Prof. Dr. José Eduardo de Oliveira Profª. Drª. Angela Regina Araújo Discentes: Pâmela Botassim Reinoso Paula Rodrigues Dias Introdução Os ésteres
PURIFICAÇÃO DO ACETATO DE ISOPENTILA (PARTE 2) Docentes: Prof. Dr. José Eduardo de Oliveira Profª. Drª. Angela Regina Araújo Discentes: Pâmela Botassim Reinoso Paula Rodrigues Dias Introdução Os ésteres
Ana Elisa Comanini Ana Karla Agner Felipe Gollino
 Ana Elisa Comanini Ana Karla Agner Felipe Gollino 2º ano Bacharelado 2008 Filtração Remover impurezas sólidas de um líquido ou de uma solução Coletar um produto sólido de uma solução na qual ele tenha
Ana Elisa Comanini Ana Karla Agner Felipe Gollino 2º ano Bacharelado 2008 Filtração Remover impurezas sólidas de um líquido ou de uma solução Coletar um produto sólido de uma solução na qual ele tenha
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR
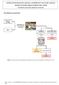 EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
EXTRAÇÃO DO ÓLEO DE LARANJA A PARTIR DAS CASCAS DE LARANJA DESTILAÇÃO POR ARRASTAMENTO DE VAPOR Procedimento experimental adaptado de J. H. Beatty 1 Procedimento experimental Figura 1. Esquema resumo do
Seminário de química orgânica Experimental I Destilação fracionada do limoneno. Edvan Ferreira de Oliveira Letícia Naomi Higa
 Seminário de química orgânica Experimental I Destilação fracionada do limoneno Edvan Ferreira de Oliveira Letícia Naomi Higa *Introdução *Destilação *Explicação da destilação fracionada *Coluna de fracionamento
Seminário de química orgânica Experimental I Destilação fracionada do limoneno Edvan Ferreira de Oliveira Letícia Naomi Higa *Introdução *Destilação *Explicação da destilação fracionada *Coluna de fracionamento
PURIFICAÇÃO DO ÉTER ETÍLICO PARTE 2. Instituição, alunos que irão proferir, curso, ano, professores e estagiários docentes
 PURIFICAÇÃO DO ÉTER ETÍLICO PARTE 2 Instituição, alunos que irão proferir, curso, ano, professores e estagiários docentes ASSUNTOS ABORDADOS: Filtração Fontes de aquecimento Ponto de Ebulição Destilação
PURIFICAÇÃO DO ÉTER ETÍLICO PARTE 2 Instituição, alunos que irão proferir, curso, ano, professores e estagiários docentes ASSUNTOS ABORDADOS: Filtração Fontes de aquecimento Ponto de Ebulição Destilação
Unidade 1: Destilação
 Universidade de São Paulo Instituto de Química de São Carlos Laboratório de Cromatografia (CROMA) Unidade 1: Destilação Prof. Fernando Lanças Destilação Processo de vaporização de uma substância, condensando
Universidade de São Paulo Instituto de Química de São Carlos Laboratório de Cromatografia (CROMA) Unidade 1: Destilação Prof. Fernando Lanças Destilação Processo de vaporização de uma substância, condensando
6 Preparação e Purificação do Acetato de Isopentila (parte II)
 UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 6 Preparação e Purificação do Acetato de Isopentila (parte II) Discentes: Grupos IX e XXIV Camila Francisconi Lima Marcus Massahiro Sinzato
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 6 Preparação e Purificação do Acetato de Isopentila (parte II) Discentes: Grupos IX e XXIV Camila Francisconi Lima Marcus Massahiro Sinzato
Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1)
 Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
EXPERIÊNCIA 02 DESTILAÇÃO
 EXPERIÊNCIA 02 DESTILAÇÃO 1- INTRODUÇÃO Destilação é uma técnica utilizada, geralmente, para remover um solvente, purificar um líquido ou para separar os componentes de uma mistura de líquidos, ou ainda
EXPERIÊNCIA 02 DESTILAÇÃO 1- INTRODUÇÃO Destilação é uma técnica utilizada, geralmente, para remover um solvente, purificar um líquido ou para separar os componentes de uma mistura de líquidos, ou ainda
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL
 DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO FRACIONADA DE UMA SOLUÇÃO evaporações
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO FRACIONADA DE UMA SOLUÇÃO evaporações
Diagrama de Fases de Misturas
 Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases de Misturas Diagramas de pressão de vapor Diagramas de Temperatura x Composição Equilíbrios líquido líquido Equilíbrios sólido líquido Diagrama
Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases de Misturas Diagramas de pressão de vapor Diagramas de Temperatura x Composição Equilíbrios líquido líquido Equilíbrios sólido líquido Diagrama
Físico-Química I. Profa. Dra. Carla Dalmolin. Diagrama de Fases. Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras
 Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Sistemas Binários O equilíbrio de fases de sistemas com dois componentes
Físico-Química I Profa. Dra. Carla Dalmolin Diagrama de Fases Físico-Química, cap. 5: Transformações Físicas de Substâncias Puras Sistemas Binários O equilíbrio de fases de sistemas com dois componentes
Química Orgânica Experimental
 Química Orgânica Experimental Destilação Simples para Purificação do Cloreto de Terc-butila e do Acetato de Isopentila Discentes: Ana Carolina Boni Eliana Alves Arxer Fernanda Maciel Barbosa Gubbiotti
Química Orgânica Experimental Destilação Simples para Purificação do Cloreto de Terc-butila e do Acetato de Isopentila Discentes: Ana Carolina Boni Eliana Alves Arxer Fernanda Maciel Barbosa Gubbiotti
Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1)
 Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL
 DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO DE UMA MISTURA HETEROGÊNEA P =
DESTILAÇÃO POR ARRASTE DE VAPOR DE ÁGUA DO ÓLEO DE CRAVO E EXTRAÇÃO QUIMICAMENTE ATIVA DO EUGENOL Principais componentes do óleo de cravo obtidos pelo arraste DESTILAÇÃO DE UMA MISTURA HETEROGÊNEA P =
Preparação do Acetato de Isopentila. Leonardo Lataro Paim Rodrigo Putvinskis
 Preparação do Acetato de Isopentila Leonardo Lataro Paim Rodrigo Putvinskis Objetivo: Preparação e isolamento do acetato de isopentila (reação de esterificação) O Acetato de Isopentila é um éster conhecido
Preparação do Acetato de Isopentila Leonardo Lataro Paim Rodrigo Putvinskis Objetivo: Preparação e isolamento do acetato de isopentila (reação de esterificação) O Acetato de Isopentila é um éster conhecido
4- Purificação do Éter Etílico II
 Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 4- Purificação do Éter Etílico II Discentes:
Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 4- Purificação do Éter Etílico II Discentes:
Extração e Purificação do Limoneno I
 Extração e Purificação do Limoneno I Química Orgânica Experimental Prof. Dr. José Eduardo de Oliveira Prof. Drª. Ângela Regina Araújo Rafael Pedroso de Morais Samira Nascimento Stain Estagiários: Andressa
Extração e Purificação do Limoneno I Química Orgânica Experimental Prof. Dr. José Eduardo de Oliveira Prof. Drª. Ângela Regina Araújo Rafael Pedroso de Morais Samira Nascimento Stain Estagiários: Andressa
4.2. Separação dos componentes de misturas homogéneas
 4.2. Separação dos componentes de misturas homogéneas Separação dos componentes de misturas homogéneas Os componentes das misturas homogéneas podem ser separados por processos físicos de separação. Usam-se
4.2. Separação dos componentes de misturas homogéneas Separação dos componentes de misturas homogéneas Os componentes das misturas homogéneas podem ser separados por processos físicos de separação. Usam-se
Purificação do Éter Etílico II
 Purificação do Éter Etílico II Ponto de Ebulição O ponto de ebulição de um líquido l pode ser definido como a temperatura na qual sua pressão de vapor é igual a a pressão externa exercida sobre qualquer
Purificação do Éter Etílico II Ponto de Ebulição O ponto de ebulição de um líquido l pode ser definido como a temperatura na qual sua pressão de vapor é igual a a pressão externa exercida sobre qualquer
EXPERIÊNCIA 05 PREPARAÇÃO DE UM AROMATIZANTE ARTIFICIAL: ACETATO DE ISOAMILA
 EXPERIÊNCIA 05 PREPARAÇÃO DE UM AROMATIZANTE ARTIFICIAL: ACETATO DE ISOAMILA 1- INTRODUÇÃO Ésteres são compostos amplamente distribuídos na natureza. Os ésteres simples tendem a ter um odor agradável,
EXPERIÊNCIA 05 PREPARAÇÃO DE UM AROMATIZANTE ARTIFICIAL: ACETATO DE ISOAMILA 1- INTRODUÇÃO Ésteres são compostos amplamente distribuídos na natureza. Os ésteres simples tendem a ter um odor agradável,
4 Purificação do Éter Etílico II
 Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 4 Purificação do Éter Etílico II Discentes:
Química Orgânica Experimental I Bacharelado 2009 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel 4 Purificação do Éter Etílico II Discentes:
Preparação do acetato de isopentila
 Preparação do acetato de isopentila I - Introdução Neste experimento, será preparado um éster, acetato de isopentila. Este éster é frequentemente chamado de óleo de banana, uma vez que possui odor característico
Preparação do acetato de isopentila I - Introdução Neste experimento, será preparado um éster, acetato de isopentila. Este éster é frequentemente chamado de óleo de banana, uma vez que possui odor característico
Destilação simples vs fracionada
 Destilação simples vs fracionada Comparar a eficiência da purificação por destilação simples vs fracionada de uma mistura cicloexano/tolueno na proporção 50:50 v/v!! Constantes físicas! Tolueno: bp = 110,6
Destilação simples vs fracionada Comparar a eficiência da purificação por destilação simples vs fracionada de uma mistura cicloexano/tolueno na proporção 50:50 v/v!! Constantes físicas! Tolueno: bp = 110,6
LISTA DE EXERCÍCIOS 4. Equilíbrio de Misturas Líquidas Binárias com o Vapor
 DEPARTAMENTO DE FÍSICO-QUÍMICA DISCIPLINA QUI 03310 FÍSICO-QUÍMICA II-B INTRODUÇÃO LISTA DE EXERCÍCIOS 4 Equilíbrio de Misturas Líquidas Binárias com o Vapor Na presente unidade, será examinado o comportamento
DEPARTAMENTO DE FÍSICO-QUÍMICA DISCIPLINA QUI 03310 FÍSICO-QUÍMICA II-B INTRODUÇÃO LISTA DE EXERCÍCIOS 4 Equilíbrio de Misturas Líquidas Binárias com o Vapor Na presente unidade, será examinado o comportamento
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a macroescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
Éter etílico (parte II)
 Éter etílico (parte II) Solventes orgânicos de diferentes graus de pureza comercialmente disponíveis; Seleção do grau de pureza: condicionada à finalidade de seu emprego, à sua disponibilidade e à seu
Éter etílico (parte II) Solventes orgânicos de diferentes graus de pureza comercialmente disponíveis; Seleção do grau de pureza: condicionada à finalidade de seu emprego, à sua disponibilidade e à seu
Destilação simples vs fracionada
 Destilação simples vs fracionada Comparar a eficiência da purificação por destilação simples vs fracionada de uma mistura cicloexano/tolueno na proporção 50:50 v/v Constantes físicas índice de refração
Destilação simples vs fracionada Comparar a eficiência da purificação por destilação simples vs fracionada de uma mistura cicloexano/tolueno na proporção 50:50 v/v Constantes físicas índice de refração
PREPARAÇÃO DO ACETATO DE ISOPENTILA
 Química Orgânica Experimental I PREPARAÇÃO DO ACETATO DE ISOPENTILA Armando Ferreira Gameiro Jr. Janaína Leme do Amaral Introdução: Os ácidos carboxílicos reagem com álcoois na presença de ácidos minerais
Química Orgânica Experimental I PREPARAÇÃO DO ACETATO DE ISOPENTILA Armando Ferreira Gameiro Jr. Janaína Leme do Amaral Introdução: Os ácidos carboxílicos reagem com álcoois na presença de ácidos minerais
SEMINÁRIO DE QUÍMICA ORGÂNICA EXPERIMENTAL I
 SEMINÁRIO DE QUÍMICA ORGÂNICA EXPERIMENTAL I SUBSTITUIÇÃO NUCLEOFÍLICA ALIFÁTICA Profs: José Eduardo Leonardo Pezza Alunos: Bruno Ricardo Vilachã Ferreira Carla Cavalca de Araujo Carlos Mateus Soares de
SEMINÁRIO DE QUÍMICA ORGÂNICA EXPERIMENTAL I SUBSTITUIÇÃO NUCLEOFÍLICA ALIFÁTICA Profs: José Eduardo Leonardo Pezza Alunos: Bruno Ricardo Vilachã Ferreira Carla Cavalca de Araujo Carlos Mateus Soares de
PREPARAÇÃO DO ACETATO DE ISOPENTILA (PARTE II)
 Universidade Estadual Paulista Júlio de Mesquita Filho Instituto de Química-UNESP Química Orgânica Experimental PREPARAÇÃO DO ACETATO DE ISOPENTILA (PARTE II) Docentes:Profª. Drª. Marcia Nasser Lopes Prof.
Universidade Estadual Paulista Júlio de Mesquita Filho Instituto de Química-UNESP Química Orgânica Experimental PREPARAÇÃO DO ACETATO DE ISOPENTILA (PARTE II) Docentes:Profª. Drª. Marcia Nasser Lopes Prof.
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 )
 SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
SÍNTESE DO 1-BROMOBUTANO Procedimento experimental a microescala (adaptado de Williamson, Minard & Masters 1 ) Introdução O 1-bromobutano é um halogeneto alquílico primário (alquilo primário) e, por isso,
1 Extração Líquido-Líquido
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Departamento de Química _ Extração Líquido-Líquido Disciplina: Práticas de Química Orgânica Materiais e Reagentes Mesa
Purificação do Éter etílico II: Destilação do Éter etílico
 Purificação do Éter etílico II: Destilação do Éter etílico Filtrado Éter, pequena quantidade de água, CaCl 2, Fe2(SO 4 ) 3, FeSO 4, H 2 SO 4 Filtrar o éter em papel pregueado, recebendo o filtrado em um
Purificação do Éter etílico II: Destilação do Éter etílico Filtrado Éter, pequena quantidade de água, CaCl 2, Fe2(SO 4 ) 3, FeSO 4, H 2 SO 4 Filtrar o éter em papel pregueado, recebendo o filtrado em um
Destilação Fracionada (água e acetona)
 Destilação Fracionada (água e acetona) INTRODUÇÃO: A destilação fracionada serve para separar uma mistura homogênea composta por dois líquidos, com ponto de ebulição próximos. Quando se destila uma mistura
Destilação Fracionada (água e acetona) INTRODUÇÃO: A destilação fracionada serve para separar uma mistura homogênea composta por dois líquidos, com ponto de ebulição próximos. Quando se destila uma mistura
Prof. José Valter SEPARAÇÃO DE MISTURAS
 1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
1 EXTRAÇÃO COM SOLVENTES simples e múltipla
 UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 1 EXTRAÇÃO COM SOLVENTES simples e múltipla Discente: Juliana Rodrigues Profº. Dr. José Eduardo de Oliveira Prof o. Dr. Leonardo Pezza
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 1 EXTRAÇÃO COM SOLVENTES simples e múltipla Discente: Juliana Rodrigues Profº. Dr. José Eduardo de Oliveira Prof o. Dr. Leonardo Pezza
Isolamento e Purificação de Produtos Naturais : Extração de Limoneno do óleo da Laranja.
 Isolamento e Purificação de Produtos Naturais : Extração de Limoneno do óleo da Laranja. Docentes: Prof. Dr. José Eduardo de Oliveira Prof. Dr. Humberto M. S. Milagre Prof a. Dra. Isabele R. Nascimento
Isolamento e Purificação de Produtos Naturais : Extração de Limoneno do óleo da Laranja. Docentes: Prof. Dr. José Eduardo de Oliveira Prof. Dr. Humberto M. S. Milagre Prof a. Dra. Isabele R. Nascimento
Orgânica Experimental I Éter Etílico Seco II. 2 ano Bachalerado Ana Sofia Denise Daré Juliana Greb
 Orgânica Experimental I Éter Etílico Seco II 2 ano Bachalerado Ana Sofia Denise Daré Juliana Greb Tópicos Abordados Filtração Papel Pregueado Tipos de Filtração Destilações Comportamento de misturas Azeótropos
Orgânica Experimental I Éter Etílico Seco II 2 ano Bachalerado Ana Sofia Denise Daré Juliana Greb Tópicos Abordados Filtração Papel Pregueado Tipos de Filtração Destilações Comportamento de misturas Azeótropos
4 PURIFICAÇÃO DO ÉTER ETÍLICO II
 UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 4 PURIFICAÇÃO DO ÉTER ETÍLICO II Discentes: Grupo X Bruno Estevam Amantéa Thiago Holanda de Abreu Profº. Dr. José Eduardo de Oliveira
UNIVERSIDADE ESTADUAL PAULISTA Instituto de Química ARARAQUARA / SP 4 PURIFICAÇÃO DO ÉTER ETÍLICO II Discentes: Grupo X Bruno Estevam Amantéa Thiago Holanda de Abreu Profº. Dr. José Eduardo de Oliveira
RECRISTALIZAÇÃO e PURIFICAÇÃO da ACETANILIDA
 RECRISTALIZAÇÃO e PURIFICAÇÃO da ACETANILIDA INTRODUÇÃO A RECRISTALIZAÇÃO consiste na dissolução de uma substância sólida num solvente, a quente, e depois, por resfriamento, obtém-se novamente o estado
RECRISTALIZAÇÃO e PURIFICAÇÃO da ACETANILIDA INTRODUÇÃO A RECRISTALIZAÇÃO consiste na dissolução de uma substância sólida num solvente, a quente, e depois, por resfriamento, obtém-se novamente o estado
CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS. Síntese II (Alaranjado II) Benzeno Nitrobenzeno Anilina Ácido Sulfanilico Alaranjado II
 CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS Síntese II (Alaranjado II) Benzeno Nitrobenzeno Anilina Ácido Sulfanilico Alaranjado II 1- OBTENÇÃO DO NITROBENZENO Reagentes: -Ácido nítrico
CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS Síntese II (Alaranjado II) Benzeno Nitrobenzeno Anilina Ácido Sulfanilico Alaranjado II 1- OBTENÇÃO DO NITROBENZENO Reagentes: -Ácido nítrico
Extração da Cafeína a partir de saquinhos de chá
 Universidade Estadual Paulista Júlio de Mesquita Filho UESP Instituto de Química Campus Araraquara Extração da Cafeína a partir de saquinhos de chá Andressa Somensi H 3 C C H 3 C H 3 1 bjetivos: Isolamento
Universidade Estadual Paulista Júlio de Mesquita Filho UESP Instituto de Química Campus Araraquara Extração da Cafeína a partir de saquinhos de chá Andressa Somensi H 3 C C H 3 C H 3 1 bjetivos: Isolamento
CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS
 CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS Síntese I ( p-red) Nitrobenzeno Anilina Acetanilida p-nitro Acetanilida p-nitro Anilina p-red 1- OBTENÇÃO DA ANILINA -Estanho -Àcido clorídrico
CURSO PRÁTICO QUI 328 e 128 SÍNTESE DE COMPOSTOS ORGÂNICOS Síntese I ( p-red) Nitrobenzeno Anilina Acetanilida p-nitro Acetanilida p-nitro Anilina p-red 1- OBTENÇÃO DA ANILINA -Estanho -Àcido clorídrico
Recristalização da Acetanilida
 Recristalização da Acetanilida Reação de formação da acetanilida O NH 2 + CH 3 CH 3 C C O O O NaAc/HAc H N C CH 3 + CH 3 C O O H Anilina Anidrido Acético Acetanilida Acido acético H + CH 3 COO - CH 3 COOH
Recristalização da Acetanilida Reação de formação da acetanilida O NH 2 + CH 3 CH 3 C C O O O NaAc/HAc H N C CH 3 + CH 3 C O O H Anilina Anidrido Acético Acetanilida Acido acético H + CH 3 COO - CH 3 COOH
4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico
 NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
NP 4023 Síntese do éster etílico do ácido 2-cicclopentanona carboxílico a partir do éster dietílico do ácido adípico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202,2) (23,0) (46,1) (156,2) Classificação Tipos
2008 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila
 28 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila Classificação Tipos de reações e classes de substâncias Reação de carbonila de ácidos
28 Esterificação do ácido propiônico com 1-butanol via catálise ácida para a obtenção do éster propanoato de butila Classificação Tipos de reações e classes de substâncias Reação de carbonila de ácidos
A. Recuperação de n-hexano e de diclorometano a partir de resíduo constituído de mistura de n-hexano e diclorometano
 A. Recuperação de n-hexano e de diclorometano a partir de resíduo constituído de mistura de n-hexano e diclorometano Objetivo: Recuperar diclorometano e n-hexano de misturas de n-hexano/diclorometano.
A. Recuperação de n-hexano e de diclorometano a partir de resíduo constituído de mistura de n-hexano e diclorometano Objetivo: Recuperar diclorometano e n-hexano de misturas de n-hexano/diclorometano.
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA. Tópicos de Química Experimental. Débora Alvim/ Willian Miguel
 MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
MATERIAIS BÁSICOS DO LABORATÓRIO DE QUÍMICA Tópicos de Química Experimental Débora Alvim/ Willian Miguel BÉQUER OU BECHER É de uso geral em laboratório: Serve para fazer reações entre soluções Dissolver
DESTILAÇÃO A VAPOR DE FILMES ASFÁLTICOS
 DESTILAÇÃO A VAPOR DE FILMES ASFÁLTICOS C D T - CENTRO DE DESENVOLVIMENTO TECNOLÓGICO Setembro de 2014 DESIGNAÇÃO - ARTERIS T- 255-92 09/2014 T 255 pg1 - Centro de Desenvolvimento Tecnológico -ARTERIS
DESTILAÇÃO A VAPOR DE FILMES ASFÁLTICOS C D T - CENTRO DE DESENVOLVIMENTO TECNOLÓGICO Setembro de 2014 DESIGNAÇÃO - ARTERIS T- 255-92 09/2014 T 255 pg1 - Centro de Desenvolvimento Tecnológico -ARTERIS
EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA)
 INSTITUTO DE QUÍMICA ARARAQUARA QUÍMICA ORGÂNICA EXPERIMENTAL EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA) Prof. Dr. José Eduardo de Oliveira Prof. Dr. Leonardo Pezza Profª Juliana Rodrigues Grupo 6 Michelle
INSTITUTO DE QUÍMICA ARARAQUARA QUÍMICA ORGÂNICA EXPERIMENTAL EXTRAÇÃO POR SOLVENTES (QUIMICAMENTE ATIVA) Prof. Dr. José Eduardo de Oliveira Prof. Dr. Leonardo Pezza Profª Juliana Rodrigues Grupo 6 Michelle
Diagramas de Fase. Objetivos:
 1 Diagramas de Fase Objetivos: Interpretar diagramas de fases de substâncias puras Deslocamento da fronteira entre as fases Interpretar diagramas de fases de compostos Diagramas de misturas líquidas Diagramas
1 Diagramas de Fase Objetivos: Interpretar diagramas de fases de substâncias puras Deslocamento da fronteira entre as fases Interpretar diagramas de fases de compostos Diagramas de misturas líquidas Diagramas
Separação de misturas
 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
SUBSTÂNCIAS E MISTURAS
 Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
Universidade de São Paulo Instituto de Química de São Carlos Departamento de Físico-Química SUBSTÂNCIAS E MISTURAS Prof. Dr. Edson Antonio Ticianelli edsont@iqsc.usp.br Monitor: Dr. Wanderson Oliveira
Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1)
 Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
Universidade Estadual Paulista Julio de Mesquita Filho Instituto de Química Isolamento de Substâncias naturais: Extração do limoneno do óleo de laranja-destilação por arraste de vapor (Parte 1) Jorge Ferreira
Acetato de Isopentila I
 Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel Acetato de Isopentila I Discentes: Grupo 24 André Paulesini Iagalo Renan Moraes Pioli Índice
Profª. Amanda Coelho Danuello Prof. Dr. Leonardo Pezza Prof. Dr. José Eduardo de Oliveira Msc. Rodrigo Sequinel Acetato de Isopentila I Discentes: Grupo 24 André Paulesini Iagalo Renan Moraes Pioli Índice
Recristalização da Acetanilida
 Recristalização da Carolina Cavasin Leandro Lílian Cristine I. Guevara Caroline Oliveira da Rocha Mariana Emídia Silva Cabral Docentes: José Eduardo de Oliveira Juliana Rodrigues Leonardo Pezza , o que
Recristalização da Carolina Cavasin Leandro Lílian Cristine I. Guevara Caroline Oliveira da Rocha Mariana Emídia Silva Cabral Docentes: José Eduardo de Oliveira Juliana Rodrigues Leonardo Pezza , o que
Preparação do t-butila Reação SN1. Ana Carolina Boni Glaucio de Oliveira Testoni Susilaine Maira Savassa
 Preparação do t-butila Reação SN1 Ana Carolina Boni Glaucio de Oliveira Testoni Susilaine Maira Savassa Qual a utilidade do cloreto de t-butila? Usado na síntese orgânica como agente alquilante; Solvente;
Preparação do t-butila Reação SN1 Ana Carolina Boni Glaucio de Oliveira Testoni Susilaine Maira Savassa Qual a utilidade do cloreto de t-butila? Usado na síntese orgânica como agente alquilante; Solvente;
DESTILAÇÃO SIMPLES E FRACIONADA
 UNIVERSIDADE TIRADENTES UNIT GRADUAÇÃO EM ENGENHARIA DE PETRÓLEO DISCIPLINA DE QUÍMICA ORGÂNICA Erico Barreto Silva Gabriel Nascimento Ayres Batista Ivo da Silva Almeida Juliana Toze Leonardo Silva Moura
UNIVERSIDADE TIRADENTES UNIT GRADUAÇÃO EM ENGENHARIA DE PETRÓLEO DISCIPLINA DE QUÍMICA ORGÂNICA Erico Barreto Silva Gabriel Nascimento Ayres Batista Ivo da Silva Almeida Juliana Toze Leonardo Silva Moura
Atividade prática Métodos de separação: destilação simples Parte 4
 Atividade prática Métodos de separação: destilação simples Parte 4 9º ano do Ensino Fundamental / 1º ano do Ensino Médio Objetivo Vivenciar os principais métodos de separação de misturas, de modo a compreender
Atividade prática Métodos de separação: destilação simples Parte 4 9º ano do Ensino Fundamental / 1º ano do Ensino Médio Objetivo Vivenciar os principais métodos de separação de misturas, de modo a compreender
PROCESSOS QUÍMICOS DE SEPARAÇÃO
 Unidades de Operação da Indústria Química PROCESSOS QUÍMICOS DE SEPARAÇÃO Prof. Iara Santos Industria Química Matéria Prima Converte Produtos Úteis à Humanidade Celulose (madeira) em Papel Argila e Areia
Unidades de Operação da Indústria Química PROCESSOS QUÍMICOS DE SEPARAÇÃO Prof. Iara Santos Industria Química Matéria Prima Converte Produtos Úteis à Humanidade Celulose (madeira) em Papel Argila e Areia
IQ-UFG. Curso Experimental de Química Geral e Inorgânica. Prof. Dr. Anselmo
 IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
IQ-UFG Curso Experimental de Química Geral e Inorgânica Aula 02 Reconhecimento de Vidrarias e Introdução às Técnicas de Laboratório Prof. Dr. Anselmo Vidrarias e equipamentos usuais em laboratórios de
EXTRAÇÃO COM SOLVENTES (transp. 1)
 EXTRAÇÃO COM SOLVENTES (transp. 1) Usado para separar e isolar determinadas substâncias encontradas em misturas complexas. As substâncias em geral são solúveis em água. Ao se adicionar um solvente não
EXTRAÇÃO COM SOLVENTES (transp. 1) Usado para separar e isolar determinadas substâncias encontradas em misturas complexas. As substâncias em geral são solúveis em água. Ao se adicionar um solvente não
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Química Orgânica Experimental I BAC CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS
 Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
Química Orgânica Experimental I BAC - 2009 CRITÉRIOS PARA CORREÇÃO DOS PRÉ-RELATÓRIOS E RELATÓRIOS Além do aqui solicitado para os Pré-Relatórios, devem ser apresentados os itens correspondentes a cada
RECRISTALIZAÇÃO e. PURIFICAÇÃO da ACETANILIDA. Jaqueline Nicola Thaís Rosa
 RECRISTALIZAÇÃO e PURIFICAÇÃO da ACETANILIDA Jaqueline Nicola Thaís Rosa INTRODUÇÃO O produto obtido de uma reação química, na maioria das vezes, encontra-se no estado impuro, e é necessário purificá-lo.
RECRISTALIZAÇÃO e PURIFICAÇÃO da ACETANILIDA Jaqueline Nicola Thaís Rosa INTRODUÇÃO O produto obtido de uma reação química, na maioria das vezes, encontra-se no estado impuro, e é necessário purificá-lo.
QFL1423 Química Orgânica Experimental
 QFL1423 Química Orgânica Experimental Aula 2 Técnicas Básicas em Química Orgânica Prof. Dr. Leandro H. Andrade (Sala 11 Bloco zero) leandroh@iq.usp.br Prof. Dr. Reinaldo C. Bazito (Sala 811 B8I) bazito@iq.usp.br
QFL1423 Química Orgânica Experimental Aula 2 Técnicas Básicas em Química Orgânica Prof. Dr. Leandro H. Andrade (Sala 11 Bloco zero) leandroh@iq.usp.br Prof. Dr. Reinaldo C. Bazito (Sala 811 B8I) bazito@iq.usp.br
PURIFICAÇÃO DE SOLVENTES ÉTER ETÍLICO. Prof. Dr. José Eduardo de Oliveira
 PURIFICAÇÃO DE SOLVENTES ÉTER ETÍLICO Docentes: Profa. Dr. Isabele R. Nascimento Prof. Dr. Humberto Marcio Santos Milagre Prof. Dr. José Eduardo de Oliveira Integrantes: Renan Diego Zanetti Samir Prioto
PURIFICAÇÃO DE SOLVENTES ÉTER ETÍLICO Docentes: Profa. Dr. Isabele R. Nascimento Prof. Dr. Humberto Marcio Santos Milagre Prof. Dr. José Eduardo de Oliveira Integrantes: Renan Diego Zanetti Samir Prioto
